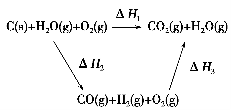-
煤燃烧后的主要产物是CO、CO2。
(1)已知: ①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.3kJ·mol-1
②C(s)+2H2O(g)=CO2(g)+2H2(g) △H2=+90.0kJ·mol-1
③CO2(g)+H2(g) = CO(g)+H2O(g) △H3=________。
⑵以CO2为原料可制备甲醇:CO2(g)+3H2(g)=CH3OH(g) + H2O(g) △H =-49.0 kJ·mol-1,向1 L的恒容密闭容器中充入1 mol CO2 (g)和3 mol H2(g),测得CO2 (g)和CH3OH(g)浓度随时间的变化如图1所示。

①0〜8 min内,以氢气表示的平均反应速率v(H2)=_____mol • L-1• min-1。
②在一定条件下,体系中CO2的平衡转化率(a)与L和X的关系如图2所示,L和X分别表示温度或压强。X表示的物理量是______(填“温度”或“压强”),L1____(填“〉”或“ <”)L2。
(3)向一体积为20 L的恒容密闭容器中通入1 mol CO2发生反应:2 CO2(g) 2CO(g)+ O2 (g),在不同温度下各物质的体积分数变化如图3所示。
2CO(g)+ O2 (g),在不同温度下各物质的体积分数变化如图3所示。
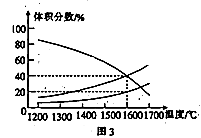
1600℃时反应达到平衡,则此时反应的平衡常数K=_______。
-
(1)已知: C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ/mol
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= ____ ___kJ/mol。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH
①下列情形不能说明该反应已达到平衡状态的是_______(填序号)。
A.每消耗1 mol CO的同时生成2molH2
B.混合气体总物质的量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
②CO的平衡转化率(α)与温度、压强的关系如图所示。A、B两点的平衡常数K(A)_______K(B)(填“>”、“=”或“<”,下同);由图判断ΔH _____0。

③某温度下,将2.0 mol CO和6.0 molH2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25 mol/L,则CO的转化率= ,此温度下的平衡常数K= (保留二位有效数字)。
(3)工作温度650℃的熔融盐燃料电池,用煤炭气(CO、H2)作负极反应物,空气与CO2的混合气体为正极反应物,催化剂镍作电极,用一定比例的Li2CO3和Na2CO3低熔点混合物作电解质。负极的电极反应式为:CO+H2-4e-+2CO32-=3CO2+H2O;则该电池的正极反应式为 。
-
已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H1
CO2(g)+H2(g) △H1
②CH4(g)+H2O(g) CO(g)+3H2(g) △H2
CO(g)+3H2(g) △H2
下列推断正确的是
A. 若CO的燃烧热为△H3,则H2的燃烧热为△H3−△H1
B. 反应CH4(g)+ CO2(g) 2CO(g)+2H2(g)的△H=△H2−△H1
2CO(g)+2H2(g)的△H=△H2−△H1
C. 若反应②的反应物总能量低于生成物总能量,则△H2<0
D. 若等物质的量CO和H2完全燃烧生成气态产物时前者放热更多,则△H1>0
-
已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H1
CO2(g)+H2(g) △H1
②CH4(g)+H2O(g) CO(g)+3H2(g) △H2
CO(g)+3H2(g) △H2
下列推断正确的是
A. 若CO的燃烧热为△H3,则H2的燃烧热为△H3−△H1
B. 反应CH4(g)+ CO2(g) 2CO(g)+2H2(g)的△H=△H2−△H1
2CO(g)+2H2(g)的△H=△H2−△H1
C. 若反应②的反应物总能量低于生成物总能量,则△H2<0
D. 若等物质的量CO和H2完全燃烧生成气态产物时前者放热更多,则△H1>0
-
已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H1
CO2(g)+H2(g) △H1
②CH4(g)+H2O(g) CO(g)+3H2(g) △H2
CO(g)+3H2(g) △H2
下列推断正确的是
A. 若CO的燃烧热为△H3,则H2的燃烧热为△H3−△H1
B. 反应CH4(g)+ CO2(g) 2CO(g)+2H2(g)的△H=△H2−△H1
2CO(g)+2H2(g)的△H=△H2−△H1
C. 若反应②的反应物总能量低于生成物总能量,则△H2<0
D. 若等物质的量CO和H2完全燃烧生成气态产物时前者放热更多,则△H1>0
-
已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H1
CO2(g)+H2(g) △H1
②CH4(g)+H2O(g) CO(g)+3H2(g) △H2
CO(g)+3H2(g) △H2
下列推断正确的是
A. 若CO的燃烧热为△H3,则H2的燃烧热为△H3−△H1
B. 反应CH4(g)+ CO2(g) 2CO(g)+2H2(g)的△H=△H2−△H1
2CO(g)+2H2(g)的△H=△H2−△H1
C. 若反应②的反应物总能量低于生成物总能量,则△H2<0
D. 若等物质的量CO和H2完全燃烧生成气态产物时前者放热更多,则△H1>0
-
(创新预测题)将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:_____________________________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出如图循环图

并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
请分析:甲、乙两同学观点正确的是________(填“甲”或“乙”);判断的理由是
_______________________________________________________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点______________________________________________________
-
将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:_______________________________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出如图循环图
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
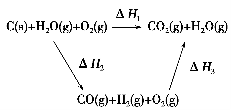
请分析:甲、乙两同学观点正确的是________(填“甲”或“乙”);判断的理由是________________________________________________________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点___________________________________________________。
-
合成氨需要的原料气氢气主要来自水煤气,水煤气的主要成分:CO、H2、CO2,其中一种制取方法是用炽热的炭和水蒸气反应制得。
C(s)+H2O(g) CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
(1)该反应的K值表达式为 。
(2)体积不变的条件下,下列措施中有利于提高CO产率的是 (填字母)。
A.升高温度 B.降低压强 C.增加C用量 D.通入H2
(3)某温度下,四种容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格①和②。
| 容器编号 | c(H2O)/mol/L | c(CO)/mol/L | c(H2)/mol/L | V正、V逆比较 |
| Ⅰ | 0.06 | 0.60 | 0.10 | V正=V逆 |
| Ⅱ | 0.06 | 0.50 | 0.40 | ① |
| Ⅲ | 0.12 | 0.40 | 0.80 | V正<V逆 |
| Ⅳ | 0.12 | 0.30 | ② | V正=V逆 |
(4)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。平衡时水蒸气的转化率为 ;向该容器中补充amol炭,水蒸气的转化率将(填“增大”、“减小”、“不变”),再补充amol水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为 。
(5)已知:①C(s)+ O2(g)=CO(g);△H=-110.5kJ/mol
O2(g)=CO(g);△H=-110.5kJ/mol
②CO(g)+ O2(g)=CO2(g);△H=-283.0kJ/mol
O2(g)=CO2(g);△H=-283.0kJ/mol
③H2(g)+ O2(g)=H2O(g);△H=-241.8kJ/mol
O2(g)=H2O(g);△H=-241.8kJ/mol
那么,将2.4g炭完全转化为水蒸气,然后再燃烧,整个过程△H= kJ/mol。
-
已知:CH3—CH===CH2+HBr→CH3—CHBr—CH3(主要产物),1mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下图所示的一系列变化。

(1)A的化学式:________,A的结构简式:________。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出C、D、E、H物质的结构简式:
C____________________,D____________________,
E____________________,H____________________。
(4)写出D→F反应的化学方程式___________________。

2CO(g)+ O2 (g),在不同温度下各物质的体积分数变化如图3所示。