-
A、B、C是短周期非金属元素,核电荷数依次增大。A元素原子核外有三种不同的能级且各个能级所填充的电子数相同,C是地壳中含量最多的元素。D、E是第四周期元素,其中E元素的核电荷数为29。D原子核外未成对电子数在同周期中最多。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物易液化的原因是 ;
(3)已知A、C形成的化合物分子甲会造成温室效应,l mol甲中含有π键的数目为 ;
(4)基态D原子的外围电子排布式为 。DO2Cl2熔点:-96 .5℃,沸点: 117℃,则固态DO2Cl2属于 晶体。

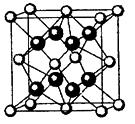
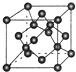
(5)E的氢化物的晶胞结构如图所示,其化学式是 。
-
原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29。
用元素符号或化学式回答下列问题:
(1)Y在周期表中的位置为__________________。
(2)已知YZ2+与XO2互为等电子体,则1mol YZ2+中含有π键数目为___________。
(3)X、Z与氢元素可形成化合物XH2Z,XH2Z分子中X的杂化方式为_________________。
(4)E原子的核外电子排布式为__________;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该价态的化学式为____________。
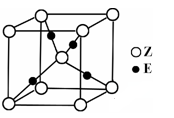
(5)氧元素和钠元素能够形成化合物F,其晶胞结构如图所示(立方体晶胞),晶体的密度为ρg··cm-3,列式计算晶胞的边长为a=______________cm(要求列代数式)。
-
(10分)X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,M含有未成对电子数最多的元素。请回答下列问题。
(1)Y、Z、W的电负性由小到大的顺序为______________。(用元素符号表示)
(2)M原子的外围电子排布式为________。
(3)X2W2分子中W原子轨道的杂化类型为________。
(4)Z与W可形成的一种ZW3-阴离子,与其互为等电子体的阴离子为_______(任写一种,)。
(5)MCl3能与Z、W的氢化物形成配位数为6的配合物,且相应两种配体的物质的量之比为2∶1,氯离子全部位于外界。则该配合物的化学式为_______。
-
X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,M含有未成对电子数最多的元素。请回答下列问题。
(1)Y、Z、W的第一电离能由大到小的顺序为______________。(用元素符号表示)
(2)M原子的外围电子排布式为________。
(3) X2W2分子中W原子轨道的杂化类型为________。
(4)Z与W可形成的一种ZW3-阴离子,与其互为等电子体的阴离子为_______(任写一种)。
(5)MCl3能与Z、W的氢化物形成配位数为6的配合物,且相应两种配体的物质的量之比为2∶1,氯离子全部位于外界。则该配合物的化学式为_______。
-
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);基态D原子的价电子排布式为______________________。
(2)A的最高价氧化物分子中,其中心原子采取________杂化;BC3-的立体构型为________(用文字描述)。
(3)1 mol AB-中含有的π键个数为________。
(4)化合物CH3COO[Cu(NH3)3·CO]中与Cu+形成配离子的配体为____________(填化学式)。
(5) CH3COOH中C原子杂化轨道类型为_________________。
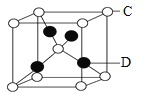
(6)元素D与元素C形成一种化合物其晶胞结构如图所示,该化合物的化学式为______.
-
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);基态D原子的电子排布式为_____。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取________杂化;BC 的立体构型为________(用文字描述)。
的立体构型为________(用文字描述)。
(3)1 mol AB-中含有的π键个数为________,电子式为__________。
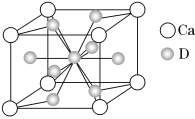
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比________。
(5)镍元素的原子价电子排布式为_____________________.
镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________________(填数值);氢在合金中的密度为_____________。(写出表达式即可)
-
X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素。
(1)N元素在周期表中的位置是______,M的基态原子的价层电子排布图为_____。
(2)Y、D、E三种元素的电负性从大到小的排列顺序为________,第一电离能从大到小的排列顺序为_______。(均用元素符号表示)。
(3)由X、D两种元素按原子个数比为2:1组成的化合物,其中心原子的杂化方式为__________,该化合物属于___________分子(填“极性”或“非极性”)。
(4)金属镍粉在化合物YE气流中轻微加热,生成无色挥发性液态Ni(YE)4,呈四面体构型。423K时,Ni(YE)4分解为Ni和YE,从而制得高纯度的Ni粉。试推测:该液态物质易溶于下列______中(填字母)。
A.水 B.硫酸镍溶液 C.苯 D.四氯化碳
(5)某盐中含NE42-离子,是一种水处理剂,加入稀硫酸后快速生成黄色溶液并释放出一种无色无味的气体,请写出该反应的离子方程式___________________。
-
X、Y、Z、W、Q、R为原子序数依次增大的前四周期元素。其相关信息如下表:
| 元素代号 | 相关信息 |
| X | 原子核外电子总数与周期序数相等 |
| Y | 原子核外电子占3个不同能级,且每个能级上排布的电子数相同 |
| Z | 最简单气态氢化物能使湿润的红色石蕊试纸变蓝 |
| W | 原子的L电子层上有2对成对电子 |
| Q | 元素的最高正价与最低负价的代数和为6 |
| R | 单质是日常生活中用途最广、用量最大的金属材料 |
请回答下列问题:
(1)基态R原子的核外电子排布式为________,R与YW易形成配合物R(YW)5,在R(YW)5中R 的化合价为_________。
(2)Y、Z、W三种元素的电负性由小到大的顺序为_________(用元素符号表示)。
(3)基态Q原子的最高能层具有的原子轨道数为________。
(4)下列关于Y2X2的说法中正确的是______(填字母)。
A. Y2X2中的所有原子都满足8电子稳定结构
B.每个Y2X2分子中σ键和π键数目之比为1:1
C. Y2X2是由极性键和非极性键构成的非极性分子
D. Y2X2的分子构型为直线形
(5)ZQ3中心原子的杂化轨道类型为______,其分子空间构型为_______。
-
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期,B元素含有3个能级,且每个能级所含的电子数相同;DD的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
(1)用元素符号表示B、C、D三种元素的第一电离能由低到高的顺序________________;
(2)F离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点,向F的硫酸盐溶液中通入过量C与A形成的气体N,反应现象为________________,反应的离子方程式为__________、______;
(2)B单质的一种同素异形体的晶胞如图所示,若晶体的密度为ρg/cm3,阿伏加德罗常数的值为NA,则晶体中最近的两个原子之间的距离为________________;
-
按要求回答以下问题:
(1)X、Y、Z 是短周期非金属元素,核电荷数依次增大。X原子外围电子排布为ns2np2,Z是地壳中含量最多的元素。W、Q是第四周期元素,其中Q元素的核电荷数为29。W原子核外未成对电子数在同周期中最多。
①Y元素在周期表中的位置为______________ ;其轨道表示式为_________________。
②X、Y、Z元素的第一电离能由大到小的顺序为_________________(用元素符号作答),X与Z形成三原子分子的电子式为___________(用相关的化学用语作答)。
③Y的氢化物沸点_______Z的氢化物的沸点(填“ >”“<”或 “=”)。
④基态W原子的外围电子排布式为 。
⑤Q的氢化物的晶胞结构如图所示,其化学式是 。
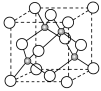
(2)过渡元素在生活、生产和科技等方面有广泛的用途。

①应用于合成氨反应的催化剂(铁)的表面上存在氮原子,上图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则图示铁颗粒表面上氮原子与铁原子的个数比为________。
②现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是______。(填序号)
| 元素 | Mn | Fe |
| 电离能 | | |
| (kJ·mol-1) | | |
| I1 | 717 | 759 |
| I2 | 1 509 | 1561 |
| I3 | 3 248 | 2 957 |
A.PFS中铁显+3价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由上表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
③铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
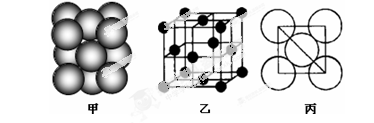
晶胞中铂(Pt)原子的配位数数为为 。








