-
已知某些化学键的键能数据如下:
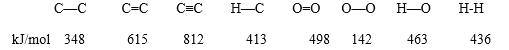
(1)通过比较C—C 和 C=C 的键能大小,简要说明为什么烯烃易发生加成反应而烷烃不能?______ 。
(2)利用键能数据可判断反应 2H2 + O2 → 2 H2O 为 放热反应, 计算每生成 1 mol H2O 所放出的热量为_____________ kJ。
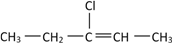
(3)若某有机物的结构简式如下: 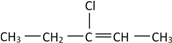 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
(4)将硫酸铜白色固体溶于水得到蓝色的溶液,原因是生成了一种配合离子,其结构简式为: ___________(标明配位键),向该溶液中加入过量稀氨水得深蓝色溶液,其离子方程式为 _________ 。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是_________________________________。
-
烟气脱硝技术是烟气治理的发展方向和研究热点。
(1)用NH3选择性脱除氮氧化物,有如下反应:
6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
| 化学键 | NO中的氮氧键 | N-H | N N N | O-H |
| 键能(kJ·mol-1) | a | b | c | d |
则该反应的ΔH=__kJ·mol-1。
(2)在汽车尾气的净化装置中CO和NO发生反应:2NO(g)+2CO(g) N2(g)+2CO(g) ΔH=-746.8kJ·mol-1。
N2(g)+2CO(g) ΔH=-746.8kJ·mol-1。
实验测得:v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)
①达平衡后,仅升高温度,k正增大的倍数__k逆增大的倍数(填“>”或“<”或“=”)。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡,CO的转化率为50%,则 =__。
=__。
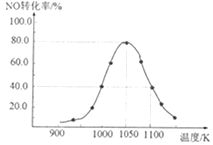
(3)现利用反应除去汽车尾气中的NOx:C(s)+2NO(g) N2(g)+CO2(g) ΔH=-34.0kJ·mol-1。在密闭容器中发生该反应,催化反应相同时间,测得不同温度下NO的转化率a(NO)随温度的变化如图所示。由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是__。
N2(g)+CO2(g) ΔH=-34.0kJ·mol-1。在密闭容器中发生该反应,催化反应相同时间,测得不同温度下NO的转化率a(NO)随温度的变化如图所示。由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是__。
(4)以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
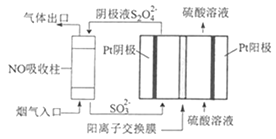
①阴极区的电极反应式为__。
②NO吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为__mL。
-
Ⅰ.现有反应CO(g)+2H2(g) CH3OH(g)过程中能量变化如下图所示,写出该反应的热化学方程式 ;
CH3OH(g)过程中能量变化如下图所示,写出该反应的热化学方程式 ;
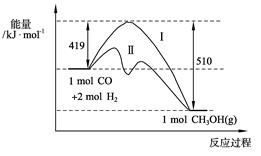
已知该反应中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 465 | 413 |
则C≡O中的键能为 KJ·mol-1;图中曲线Ⅱ表示 (填反应条件)的能量变化。
Ⅱ. Li—SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S +SO2。
请回答下列问题:
(1)电池的负极发生的电极反应为 ;
(2)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2S O3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式 ;
O3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式 ;
-
二甲醚( )是一种应用前景广阔的清洁燃科,以CO和氢气为原料生产二甲醚主要发生以下三个反应:
)是一种应用前景广阔的清洁燃科,以CO和氢气为原料生产二甲醚主要发生以下三个反应:
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | 
| 
| C≡O | H-O | C-H |
| 
| 436 | 343 | 1076 | 465 | 413 |
由上述数据计算 __________________________________;
__________________________________;
(2)该工艺的总反应为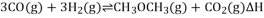 ,该反应
,该反应 _______________,化学平衡常数
_______________,化学平衡常数 ______________________(用含
______________________(用含 的代数式表示);
的代数式表示);
(3)下列措施中,能提高 产率的有______________________________;
产率的有______________________________;
A.分离出二甲醚 B.升高温度 C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。该工艺中反应③的发生提高了 的产率,原因是___________________________。
的产率,原因是___________________________。
(5)以 通入
通入 的反应器中,一定条件下发生反应:
的反应器中,一定条件下发生反应: 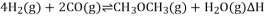 ,其
,其 的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是____________________;
的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是____________________;
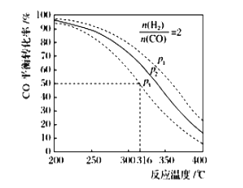
A.该反应的
B.若在 和
和 时反应达到平衡,则CO的转化率小于50%
时反应达到平衡,则CO的转化率小于50%
C.若在 和
和 时反应达到平衡, 氢气的转化率等于50%
时反应达到平衡, 氢气的转化率等于50%
D.若在 和
和 时,起始时
时,起始时 ,则达平衡时CO的转化率大于50%
,则达平衡时CO的转化率大于50%
E.若在 和
和 时,反应达平衡后保持温度和压强不变,再充入
时,反应达平衡后保持温度和压强不变,再充入 和
和 ,则平衡时二甲醚的体积分数增大
,则平衡时二甲醚的体积分数增大
(6)某温度下,将 和
和 充入容积为
充入容积为 的密闭容器中,发生反应:
的密闭容器中,发生反应: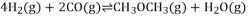 ,反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数
,反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数 ____________________________。
____________________________。
-
已知2NH3(g)+3Cl3(g)=N2(g)+6HCl(g)ΔH,已知反应的相关的化学键键能数据如下:
| 化学键 | Cl-Cl | N-H | N≡N | H-Cl | O-H |
| E/(kJ·mol-1) | 242.7 | 390.8 | 946 | 431.8 | 463 |
由此计算△H为
A.+463.9kJ·mol-1 B.-463.9kJ·mol-1
C.+231.95kJ·mol-1 D.-231.95kJ·mol-1
-
从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。已知键能数据如下表:
| 化学键 | N≡N | N—H | H—H |
| 键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g)  2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
A. 551 B. 437 C. 558 D. 160
-
从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。
已知键能数据如下表:
| 化学键 | N≡N | N—H | H—H |
| 键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g)  2NH3(g);△H=-93kJ·mol-1。试根据表中所列键能数据计算b数值:
2NH3(g);△H=-93kJ·mol-1。试根据表中所列键能数据计算b数值:
A. 551 B. 437 C. 558 D. 160
-
从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。已知键能数据如下表:
| 化学键 | N≡N | N—H | H—H |
| 键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g)  2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
A. 551 B. 437 C. 558 D. 160
-
从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。已知键能数据如下表:
| 化学键 | N≡N | N—H | H—H |
| 键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g)  2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
A. 551 B. 437 C. 558 D. 160
-
从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。已知键能数据如下表:
| 化学键 | N≡N | N—H | H—H |
| 键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g)  2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
2NH3(g);△H= —93kJ·mol-1。试根据表中所列键能数据计算b数值:
A. 551 B. 437 C. 558 D. 160
 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________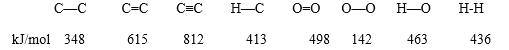
 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________


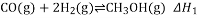
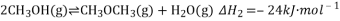
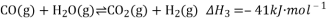
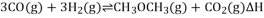 ,该反应
,该反应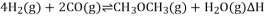 ,其
,其
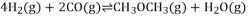 ,反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数
,反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数