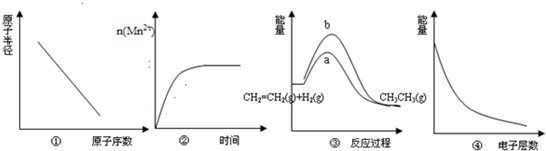
A.图①表示IA族元素原子半径的变化规律
B.图②表示10mL0.01mol•L-1KMnO4酸性溶液与过量的0.1mol•L-1H2C2O4溶液混合时,n(Mn2+)随时间的变化
C.图③中a、b曲线分别表示反应:CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0在使用和未使用催化剂时,反应过程中的能量变化
D.图④表示核外电子能量与电子层数的关系
高三化学选择题中等难度题

高三化学选择题中等难度题

高三化学选择题中等难度题查看答案及解析

高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
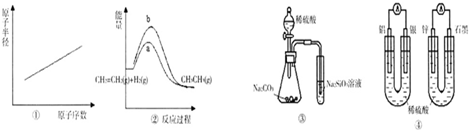
下列各表述与示意图一致的是
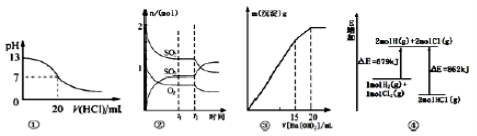
A.图①表示25℃时,用0.1mol/L盐酸滴定20mL0.1mol/LNaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线
B.图②表示一定条件下进行的反应2SO2(g)+O2(g)2SO3(g)△H<O各成分的物质的量变化.t2时刻改变的条件可能是降低温度或缩小容器体积
C.图③表示某明矶溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(0H)2溶液体积的关系,在加入20mL溶液时铝离子恰好沉淀完全
D.图④表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=+183kJ/mol
高三化学选择题困难题查看答案及解析
下列各表述与示意图一致的是

A.图①表示25℃时,用0.1mol/L盐酸滴定20mL0.1mol/LNaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线
B.图②表示一定条件下进行的反应2SO2(g)+O2(g)2SO3(g)△H<O各成分的物质的量变化.t2时刻改变的条件可能是降低温度或缩小容器体积
C.图③表示某明矶溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(0H)2溶液体积的关系,在加入20mL溶液时铝离子恰好沉淀完全
D.图④表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=+183kJ/mol
高三化学单选题中等难度题查看答案及解析

高三化学选择题中等难度题查看答案及解析
下列各表述与示意图不一致的是

A.图①表示5 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
B.图②中曲线表示反应2SO2(g)+O2(g)2SO3(g) △H<0正、逆反应的平衡常数K随温度的变化
C.图③表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
D.I2在KI溶液中存在I2(aq)+I-(aq)I3-(aq)的平衡,c(I3-)与温度T的关系如图④,若反应进行到状态C时,一定有V(正)>V(逆)
高三化学单选题困难题查看答案及解析
常温下,向10mL0.1mol·L-1KCl溶液和10mL0.1mol·L-1K2CrO4溶液中分别滴加0.1mol·L-1AgNO3溶液。滴加过程中pM[表示-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为砖红色沉淀,下列说法不合理的是
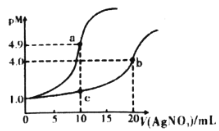
A.bc所在曲线对应K2CrO4溶液
B.常温下,Ksp(Ag2CrO4)<Ksp(AgCl)
C.溶液中c(Ag+)的大小:a点>b点
D.用0.1mol·L-1AgNO3标准液滴定上述KCl、K2CrO4溶液时,Cl-先沉淀
高三化学单选题中等难度题查看答案及解析
如图所示表示一些元素原子半径规律性的变化示意图。由此图不能得出下列结论的是(不考虑稀有气体元素)

A.当电子层数相同时,核电荷数越小,原子半径越大
B.当最外层电子数相同时,质子数越多,原子半径越大
C.r(F-)<r(Cl-)<r(Br-)<r(I-),r(K+)>r(Na+)>r(Mg2+)>r(Al3+)
D.原子电子层数越多,对应的原子半径越大
高三化学单选题中等难度题查看答案及解析
25℃时,向 10mL 0.01 mol/L NaCN 溶液中逐滴滴加 10mL0.01 mol/L 的盐酸,其 pH 变化曲线如图所示。下列溶液中的关系一定正确的是(忽略体积微小变化)
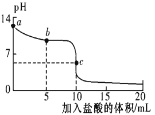
A.a 点溶液的 pH ≥12
B.b 点的溶液:c(CN-)> c(Cl-)>c(HCN )
C.pH =7 的溶液:c(Na+)+ c(H+) =c(Cl-)+ c(CN-)
D.c 点的溶液:c(CN-)+c(HCN ) +c(Cl-)=0.01 mol/L
高三化学单选题中等难度题查看答案及解析