-
硅是信息技术的关键材料,在工业中可利用镁制取硅:2Mg(过量)+SiO2 2MgO+Si,2Mg+Si
2MgO+Si,2Mg+Si Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体;③Mg在加热时能与CO2、N2反应。
Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体;③Mg在加热时能与CO2、N2反应。
I.如图是实验室进行Mg与SiO2反应的裝置:
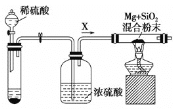
(1)盛放稀硫酸的装置为_________________,由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用_________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示为 ①____________________; ②_________________。
II.利用如图装置(量气管“0”刻度在刻度线的最上方)可测定生成物的纯度。
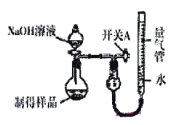
(3)实验开始前应先_________________。
(4)若取样品Wg加入5mLNaOH(足量)充分反应。反应前量气管液面读数为V1mL,反应后为V2mL(实验数据均转化为标准状况下),则样品的纯度为____________________。(写出计算式,不化简)。
(5)若反应结束时读数前未调节量气装置两边液面高度相平(右边的液面高于左边液面),则会导致实验结果______(填“偏高”、“偏低”或“无影响”)。
-
硅是信息技术的关键材料,在工业中可利用镁制取硅:2Mg(过量)+SiO2 2MgO+Si,2Mg+Si
2MgO+Si,2Mg+Si Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体。
Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体。
I.如图是实验室进行Mg与SiO2反应的裝置:
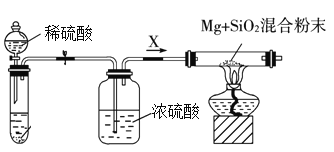
(1)盛放稀硫酸的装置为____,由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用___(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)当反应开始后,移走酒精灯反应能继续进行,其原因是_________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示为①___________;②_____________。
II.利用如图装置(量气管“0”刻度在刻度线的最上方)可测定生成物的纯度。
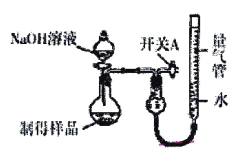
(4)实验开始前应先__________。
(5)若取样品Wg加入5mLNaOH(足量)充分反应。反应前量气管液面读数为V1mL,反应后为V2mL(实验数据均转化为标准状况下),则样品的纯度为_____(写出计算式,不化简)。
(6)若反应结束时读数前未调节量气装置两边液面高度相平(右边的液面高于左边液面),则会导致实验结果_________(填“偏高”、“偏低”或“无影响”)。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
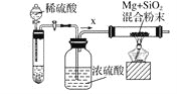
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
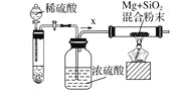
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
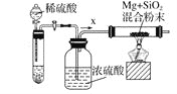
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
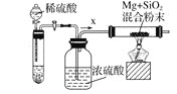
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
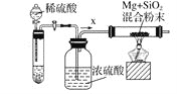
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
-
工业上通常利用SiO2和碳反应来制取硅,写出反应的化学方程式___________。工业上还可以利用镁制取硅,反应为2Mg+SiO2=2MgO+Si,同时会发生副反应:2Mg + Si=Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
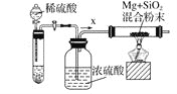
(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 _______________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①________________,②_________________。
2MgO+Si,2Mg+Si
Mg2Si(副反应),查资料得:①Mg2Si遇盐酸迅速反应生成SiH4(硅烷);②SiH4在常温下是一种不稳定易分解、易自燃的气体。











