-
燃煤和汽车尾气是造成空气污染产生雾霾的原因之一。消除汽车尾气是减少城市空气污染的热点研究课题。
(1)已知:①N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②CO(g)+1/2 O2(g)=CO2 (g) △H=-283kJ·mol-1
则汽车尾气中NO和CO在催化转化器中相互反应成无污染的气体的热化学方程式是__________。
(2)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
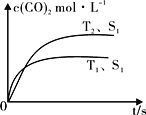
已知当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程的变化曲线_____________。
(3)在一定温度下,将2.0mol NO、2.4mol气体CO 通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如右图所示:
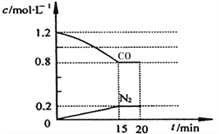
①有害气体NO的转化率为________, 0~15min NO的平均速率v(NO)=______mol/(L·min)。(保留两位有效数字)
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是________(选填序号)。
a.缩小容器体积b.增加CO的量 c.降低温度 d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将___________移动(选填“向左”、“向右”或“不”),移动后在达到平衡时的平衡常数的值是____________(保留两位有效数字)。
-
燃煤和汽车尾气是造成空气污染产生雾霾的原因之一。消除汽车尾气是减少城市空气污染的热点研究课题。
(1)已知:①N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②CO(g)+1/2 O2(g)=CO2 (g) △H=-283kJ·mol-1
则汽车尾气中NO和CO在催化转化器中相互反应成无污染的气体的热化学方程式是__________。
(2)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。

已知当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程的变化曲线_____________。
(3)在一定温度下,将2.0mol NO、2.4mol气体CO 通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如右图所示:
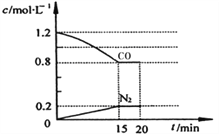
①有害气体NO的转化率为________, 0~15min NO的平均速率v(NO)=______mol/(L·min)。(保留两位有效数字)
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是________(选填序号)。
a.缩小容器体积b.增加CO的量 c.降低温度 d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将___________移动(选填“向左”、“向右”或“不”),移动后在达到平衡时的平衡常数的值是____________(保留两位有效数字)。
-
机动车尾气和燃煤产生的烟气是目前城市空气污染的重要原因之一。NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
2NO(g)+2CO(g) 2CO2(g)+N2(g) ∆H= -a kJ·mol-1
2CO2(g)+N2(g) ∆H= -a kJ·mol-1
(1)CO可用于炼铁,已知:
①Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H= + 489.0 kJ/mol
②C(s)+CO2(g)=2CO(g)△H= + 172.5 kJ/mol
则CO还原Fe2O3的热化学方程式为_____________________
(2)在一定温度下,将1.2 mol NO、1.0 mol CO气体通入到固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示。
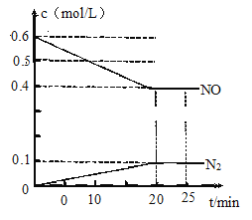
0~20 min CO2的平均速率v(CO2)=____________,CO的转化率为____________
(3)下列能够说明该反应已经达到平衡的是__________
a.该容器内压强不再改变
b.上述反应的焓变∆H不变
c. v(NO)=2v(N2)
d.混合气体的密度不再变化
(4)若保持反应体系的温度不变,20 min时再向容器中充CO、CO2各0.2mol,化学平衡将_________(填“逆向”“正向”或“不”)移动。重新达到平衡后,该反应的化学平衡常数为_________(结果保留两位有效数字)
(5)工业上用氨水将SO2转化为(NH4)2SO3,再氧化为(NH4)2SO4。已知25℃时,0.05mol/L(NH4)2SO4溶液的pH=a,则c(NH ):c(NH3·H2O)=__________用含a的代数式表示,已知NH3·H2O的电离常数为Kb=1.7×10-5)。
):c(NH3·H2O)=__________用含a的代数式表示,已知NH3·H2O的电离常数为Kb=1.7×10-5)。
-
汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应:N2(g) + O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
(1)已知H2或CO可以催化还原NO以达到消除污染的目的。N2(g) + O2(g) = 2NO(g) △H= +180.5 kJ·mol-1,2H2(g) + O2(g) = 2H2O(l) △H=-571.6 kJ·mol-1,则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是_________________________,判断该反应自发进行的条件:_______________(填“高温自发”或“低温自发”)。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2NO(g) + 2CO(g) 2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
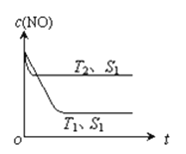
①则该反应的△H___0(填“>”或“<”)。
②若催化剂的表面积S1>S2 ,在该图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线___。
(3)某小组往一恒温恒压容器充入9mol N2和23mol H2模拟合成氨反应,图C为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图.若体系在T2、60MPa下达到平衡.
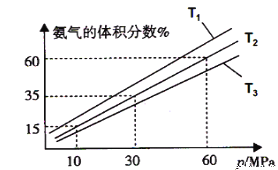
①能判断N2(g)+3H2(g)⇌2NH3(g)达到平衡的是___(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(N2)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②此时N2的平衡分压为_________MPa.(分压=总压×物质的量分数)。计算出此时的平衡常数Kp=__________(用平衡分压代替平衡浓度计算,结果保留2位有效数字)。
-
(12分)2014年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如下图所示。据此判断:
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如下图所示。据此判断:

①该反应的ΔH 0(填“>”“<”)。
②在T2温度下,0~2 s内的平均反应速率v(N2)= 。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
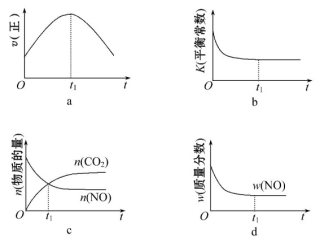
(2)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g)ΔH1
2CO(g)+O2(g)===2CO2(g)ΔH2
2H2(g)+O2(g)===2H2O(g)ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=___ 。
(3)某实验小组用50mL 0.50mol·L- 1 NaOH 溶液和30mL 0.50mol·L- 1硫酸溶液进行中和热的测定。实验数值结果比57.3 kJ/mol偏小,产生此实验偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
-
近年来,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO (g) +2CO (g)  2CO2 (g) +N2 (g)。在密闭容器中发生该反应时,c(CO2 )随温度(T)、催化剂的表面积(S)和时间((t)的变化曲线,如图1所示
2CO2 (g) +N2 (g)。在密闭容器中发生该反应时,c(CO2 )随温度(T)、催化剂的表面积(S)和时间((t)的变化曲线,如图1所示

据此判断:
①在T1温度下,0-2s内的平均反应速率v(N2)= _________mol/(L·s)
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率,若增大催化剂的表面积,则CO转化率_________(填“增大”“减少”或“不变”)。
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t、时刻达到平衡状态的是_________(填字母)
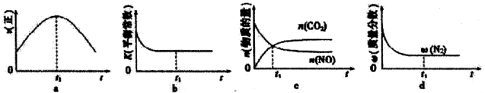
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) =N2(g)+CO2(g)+2H2O(g) △H=- 867.0kJ/mol
2NO2(g)  N2O4(g) △H=一56.9kJ/mol
N2O4(g) △H=一56.9kJ/mol
写出CH4催化还原N2O4 (g)生成N2和H2O(g)的热化学方程式_________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图2是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。
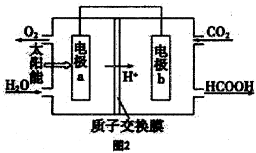
b电极上发生的电极反应式为_________。
-
2016年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
I.汽车尾气净化的主要原理为:2NO(g)+2CO(g)  2CO2(g)+N2(g),正反应为放热反应。
2CO2(g)+N2(g),正反应为放热反应。
(1)下列说法正确的是_______________。
A.装有尾气净化装置的汽车排出的气体中一定不再含有NO或CO
B.提高尾气净化效率的最佳途径是研制高效催化剂
C.升高温度可使该反应的正反应速率增大、逆反应速率减小
D.单位时间内消耗NO和CO2的物质的量相等时,反应达到平衡
(2)已知增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在线面实验设计表中,请在下表中的横线上填出合理数据:
| 实验编号 | t(℃) | NO初始浓度(10-3mol·L-1) | CO初始浓度(10-3mol·L-1) | 催化剂的比表面积(m2·g) |
| ① | 280 | 1.20 | 5.80 | 82 |
| ② | ______ | 1.20 | ______ | 124 |
| ③ | 350 | ______ | ______ | 82 |
实验①中,NO的物质的量浓度(c)随时间(t)的变化如下图所示。请在给出的坐标图中画出实验②、③中NO的物质的量浓度(c)随时间(t)的变化的曲线______,并标明各曲线的实验编号。
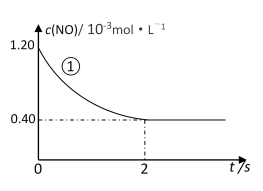
在280℃下,0~2 s内的平均反应速率v(N2) = ________________________。
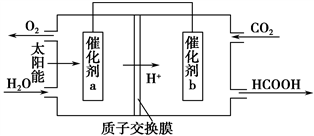
II.直接排放煤燃烧产生的烟气会引起严重的环境问题。
(3)煤燃烧产生的烟气含氮的氧化物,用CH4催化还原氮氧化物(NOx)可以转化成无毒害的空气组分,从而消除氮氧化物的污染。请写出CH4催化还原NO2的化学方程式:_______________________________________________________。
(4)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。右上图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂a表面发生_______反应(填“氧化”或“还原”),总反应的化学方程式为________________________。
-
2014年初雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)  2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。据此判断:
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。据此判断:
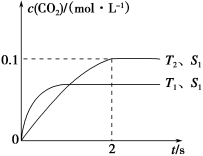
①该反应在 能自发进行(填“高温下” 、“低温下” 或“任何温度下”);
②在T2温度下,0~2 s内的平均反应速率v(N2)=___________。
(2)煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
在恒压下,将CH4(g)和NO2(g)置于密闭容器中,也可以发生化学反应:
CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2转化率的措施有
N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2转化率的措施有
A.增加原催化剂的表面积 B.降低温度
C. 减小投料比[n(NO2) / n(CH4)] D.增大压强
(3)在容积相同的两个密闭容器内 (装有等量的某种催化剂) 先各通入等量的CH4,然后再分别充入等量的NO和NO2。在不同温度下,同时分别发生上述的两个反应:并在t秒时测定其中NOx转化率,绘得图象如图所示:
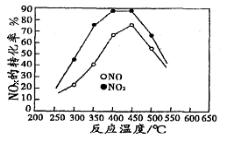
从图中可以得出的结论是
结论一:在250℃-450℃时,NOx转化率随温度升高而增大,450℃-600℃时NOx转化率随温度升高而减小
推测原因是
结论二:
-
2015年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2CO2(g)+N2(g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2(g)+N2(g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。

据此判断:
①该反应的平衡常数表达式为 。
②该反应的ΔH 0(选填“>”、“<”)。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H =-867kJ·mol-1
2NO2(g)  N2O4(g) △H =-56.9kJ·mol-1
N2O4(g) △H =-56.9kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式 。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过光电转化原理以廉价原料制备新产品的示意图。

写出上述光电转化过程的化学反应方程式 。催化剂a、b之间连接导线上电子流动方向是 (填a→b或b→a)。
-
雾霾天气多次肆虐我国中东部地区。其中汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和 时间(t)的变化曲线如图1所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和 时间(t)的变化曲线如图1所示。
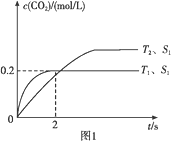
据此判断:
①该反应的ΔH____0(填“>”或“<”)。
②在T1温度下,0~2 s内的平均反应速率υ(N2)=_____。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若增大催化剂的表面积,则CO转化率____(填“增大”“减小”或“不变”)。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____(填字母)。
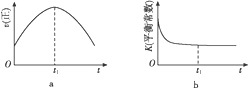
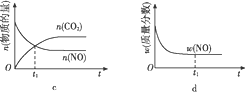
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)ΔH=-867.0 kJ/mol
2NO2(g) N2O4(g) ΔH=-56.9 kJ/mol
N2O4(g) ΔH=-56.9 kJ/mol
写出CH4催化还原N2O4(g)生成N2、CO2和H2O(g)的热化学方程式:_________________。
(3)工业上用CO2和H2反应合成二甲醚:2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g) △H3 = -130.8 kJ/mol
CH3OCH3(g)+3H2O(g) △H3 = -130.8 kJ/mol
①一定条件下,上述反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是______________ (填代号)。
a.逆反应速率先增大后减小
b. H2的转化率增大
c.反应物的体积百分含量减小
d.容器中  值变小
值变小
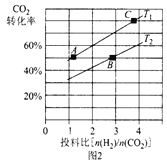
②在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的转化率如图2所示。KA、KB、Kc三者由大到小的关系是_____________________.
③上述合成二甲醚的过程中提高CO2的转化率可采取的措施有__________________、__________________(回答2点)。





















