-
氯气的实验室制法是MnO2和浓盐酸在加热条件下反应,若将MnO2换成KMnO4、KClO3等氧化剂氧化浓盐酸亦可快速制取氯气。根据上述反应原理,有人提出猜想:能否利用Na2O2的强氧化性氧化浓盐酸得到氯气呢?某课外小组在实验室进行了探索性实验,设计了如图所示装置:
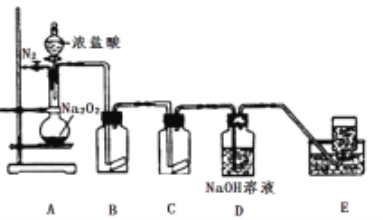
操作步骤及有关现象如下:
①装好装置,检查装置的气密性,加入药品。
②缓慢通入一定量的N2后,将装置E连接好(导管未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体.装置E中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)用化学方程式表示实验室制取Cl2的反应:____________________________________;若以含14.6g HCl的浓盐酸与足量MnO2充分反应,制得的Cl2在标准状况下总小于2.24L,原因可能是____________________________________________________。
(2)装置B中为湿润的KI-淀粉试纸,反应一段时间后试纸变蓝,能否仅通过该现象说明A装置中产生氯气?___________(填“能”或“不能”),请用离子方程式说明原因________;装置C中湿润的红色布条褪色,是因为产生了具有强氧化性的物质:_____。
(3)实验证明,Na2O2可以与HCl反应生成氯气,请写出反应的化学方程式:_____________。
(4)装置D的作用之一是吸收生成的氯气,请写出相应的离子方程式:_________________。
(5)利用Na2O2与浓盐酸反应制得的Cl2中通常含有的杂质气体有:___________(不包括水蒸气),较难分离,因此实验室很少用该方法制取氯气。
-
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、NaClO等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原理制取少量Cl2。现将一定质量的NaClO放入50mL 12.00mol•L-1的浓盐酸中,生成的Cl2在标准状况下的体积为3.36L。试计算(反应前后溶液的体积变化忽略不计):
(1)写出该反应的离子方程式 ;
(2)反应后溶液中HCl的物质的量浓度为 mol•L-1
(3)反应过程中,被氧化的HCl的物质的量为 mol。
-
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、NaClO等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原理制取少量Cl2。现将一定质量的NaClO放入50mL 12.00mol•L-1的浓盐酸中,生成的Cl2在标准状况下的体积为3.36L。试计算(反应前后溶液的体积变化忽略不计):
(1)写出该反应的离子方程式 ;
(2)反应后溶液中HCl的物质的量浓度为 mol•L-1
(3)反应过程中,被氧化的HCl的物质的量为 mol。
-
某化学兴趣小组在加热条件下利用二氧化锰与浓盐酸反应来制取并收集氯气。
(1)若要制取纯净干燥的氯气,应使气体依次通过装有_______和_____的洗气瓶。
(2)实验室中若无MnO2,可用固体KMnO4代替,发生下列反应:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的气体发生装置是(填序号)___________。
a.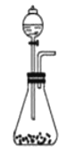 b.
b.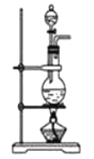 c.
c.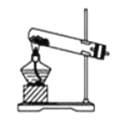
(3)某同学不慎将MnO2和KCl粉末混合了,分离该混合物的方法和步骤如下,请补充完整:先在盛有混合粉末的烧杯中加入适量的水溶解;然后____、洗涤、干燥沉淀得到MnO2;将所得液体________,即得到KCl固体。
-
实验室制取气体装置一般由发生装置、净化装置、收集装置以及尾气吸收装置组成。以Cl2的实验室制法为例(见下图):

(1)反应原理:用强氧化剂(如KMnO4、K2Cr2O7、KClO3、MnO2等)氧化浓盐酸。MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)制备装置类型:固体+液体 气体
气体
(3)净化方法:用___________________除去HCl,再用浓硫酸除去水蒸气。
(4)收集方法:________________法或排饱和食盐水法。
(5)尾气吸收:用强碱溶液(如NaOH溶液)吸收,不用Ca(OH)2溶液吸收的原因是_________________________________________________________________________。
(6)验满方法:将湿润的淀粉-KI试纸靠近盛Cl2的试剂瓶口,观察到__________________,则证明已集满;或将湿润的_________________靠近盛Cl2的试剂瓶口,观察到试纸先变红后褪色,则证明已集满。
-
利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组模拟上述过程,所设计的装置如图所示:
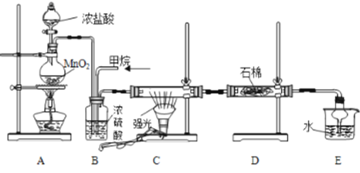
(1)A中制取Cl2时若将MnO2换成另一种固体即可不用加热并能快速制取氯气,写出该快速制氯气过程的离子方程式为______。
(2)B装置有三种功能:①控制气流速度;②___________;③___________。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是___________。
(4)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是___________。
(5)该装置还存在的明显缺陷是____________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是________。
-
已知实验室制氯气的化学方程式为:MnO2+4HCl (浓)=MnCl2+Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟二氧化锰反应制取氯气.若标准状况下制得Cl22.24L求:
(1)二氧化锰的质量;
(2)把(1)中反应后的溶液稀释到50mL,从中取出10.0mL,加入10.0mL 0.600mol/L的硝酸银溶液,恰好将氯离子完全沉淀.求(1)中反应后溶液稀释到50mL时氯离子的物质的量浓度是多少?
-
已知实验室制氯气的化学方程式为:MnO2 + 4HCl (浓) = MnCl2 + Cl2+2H2O,现用足量浓盐酸在加热条件下跟1.74g二氧化锰反应制取氯气。求:
(1)产生的氯气在标准状况下的体积。
(2)把(1)中反应后的溶液稀释到100 mL,从中取出20.0 mL,加入40.0 mL 0.600 mol / L的硝酸银溶液,恰好将氯离子完全沉淀。求(1)中反应后溶液稀释到100 mL时氯离子的物质的量浓度是多少?
-
实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。下图是实验室利用此反应制备氯气并进行一系列相关实验的装置(夹持设备已略)。
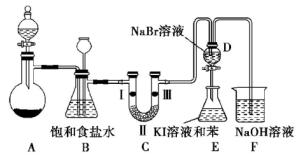
(1)上述反应中_________是氧化剂,_________是还原剂,若反应中氧化产物比还原产物多1mol,则转移的电子数目为__________。
(2)装置B的作用是_____________,实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象:_________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入________(选“a”“b”或“c”)。

(4)设计装置D、E的目的是为了比较Cl2、Br2、I2的氧化性强弱。已知Br2的水溶液因浓度不同而呈现橙色或红棕色,I2难溶于水而易溶苯,且I2的苯溶液为紫红色。当向D中缓缓通入足量Cl2时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2,请写出D中对应的离子方程式并用双线桥法表示出电子转移情况:________________。打开活塞,将D中的少量溶液加入E中,振荡E,观察到E中溶液分为两层,上层(苯层)为紫红色。该现象___________(填“能”或“不能”)说明Br2的氧化性大于I2。
(5)装置F的作用是除去污染性的物质(Cl2、Br2等),已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3,且c(Cl-)/c(ClO-)的值与温度高低有关。若烧杯中装有500mL0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为____________L(忽略Cl2溶于水)。
-
(1)实验室用二氧化锰跟浓盐酸共热反应制取氯气,化学方程式是 4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O,HCl 所起的作用有:_____________________。
Cl2↑+MnCl2+2H2O,HCl 所起的作用有:_____________________。
(2)KMnO4是常用的氧化剂。用高锰酸钾跟浓盐酸在室温下制氯气的化学方程式是:2 KMnO4 + 16 HCl == 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O ,用双线桥法表示该反应方程式的电子得失情况_____________。
(3)历史上曾用“地康法”制氯气。这一方法是用 CuCl2 作催化剂,在 450℃利用空气中的氧气跟氯化氢反应制氯气。这一反应的化学方程式为_____________________。
(4)若要制得 71g 氯气,则三种方法被氧化的 HCl 物质的量之比是_________,参与反应的 HCl 质量之比是_____________________。
(5)比较以上三个反应,氧化剂的氧化能力从强到弱的顺序为 KMnO4>MnO2>O2,你认为得到这个顺序的依据是:_____________________。

 b.
b. c.
c.



