A.
B.

C.

D.

高三化学选择题中等难度题




高三化学选择题中等难度题




高三化学选择题中等难度题查看答案及解析
向盛有少量NaCl溶液的试管中滴入少量AgNO3溶液,再加入氨水,有关实验现象的叙述不正确的是
A.先生成白色沉淀,加入足量氨水后沉淀消失
B.生成的沉淀为AgCl,它不溶于水,但溶于氨水,重新电离成Ag+和Cl-
C.生成的沉淀是AgCl,加入氨水后生成了可溶性的配合物[Ag(NH3)2]Cl
D.若向AgNO3溶液中直接滴加氨水,产生的现象也是先出现白色沉淀后沉淀消失
高三化学选择题中等难度题查看答案及解析
向盛有少量NaCl溶液的试管中滴入少量AgNO3溶液,再加入氨水,下列关于实验现象的叙述不正确的是( )
A.先生成白色沉淀,沉淀消失
B.生成的沉淀为AgCl,它不溶于水,但溶于氨水,重新电离成Ag+和Cl-
C.生成的沉淀是AgCl,加入氨水后生成了可溶性的配合物[Ag(NH3)2]Cl
D.若向AgNO3溶液中直接滴加氨水,产生的现象也是先出现白色沉淀后沉淀消失
高三化学单选题中等难度题查看答案及解析
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ +2NH3H2O
[Ag(NH3)2]
+ 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s)Ag+ (aq)
Cl- (aq)
B.实验可以证明NH3结合Ag+能力比Cl-强
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
高三化学选择题中等难度题查看答案及解析
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ + 2NH3· H2O Ag(NH3)2 + 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH3结合Ag+能力比Cl-强
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
高三化学选择题中等难度题查看答案及解析
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++ 2NH3·H2OAg(NH3)2++ 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl (s)Ag+(aq)+Cl-(aq)
B.实验可以证明NH3结合Ag+能力比Cl-强
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
高三化学单选题中等难度题查看答案及解析
14.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ + 2NH3· H2O Ag(NH3+)2 + 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH3结合Ag+能力比Cl-强
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
高三化学选择题中等难度题查看答案及解析
已知向含有Zn2+的溶液中滴加氨水,有白色沉淀Zn(OH)2生成,继续滴加氨水使其过量,沉淀又溶解,生成了[Zn(NH3)4]2+。此外,Zn(OH)2既可溶于盐酸,又可溶于过量的NaOH溶液生成[Zn(OH)4]2-。所以Zn(OH)2是一种两性氢氧化物。现有四组离子,每组有两种金属离子,请各选一种试剂,将它们两者分开,可供选择的试剂有
A.硫酸 B.盐酸
C.硝酸 D.氢氧化钠溶液
E.氨水
根据上述内容填写下表:
| 离子组 | 选用试剂(字母代号) | 沉淀物化学式 | 保留在溶液中的离子 |
| ①Zn2+和Al3+ | |||
| ②Zn2+和Mg2+ | |||
| ③Zn2+和Ba2+ | |||
| ④Mg2+和Al3+ |
高三化学填空题困难题查看答案及解析
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成,经查资料得知:
Ag++2NH3•H2OAg(NH3)2++2H2O下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s)Ag+(aq)+Cl-(aq)
B.实验表明实验室可用氨水洗涤银镜反应后的试管
C.实验可以证明NH3结合Ag+能力比Cl--强
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
高三化学选择题困难题查看答案及解析
下列离子方程式书写正确的是
A.AgCl沉淀在氨水中溶【解析】
AgCl+2NH3·H2O ==Ag(NH3)2++Cl—+2H2O
B.向Na2SO3、NaI的混合溶液中滴加少量氯水:2I—+C12==2 Cl—+I2
C.向水杨酸中加入适量Na2CO3溶液: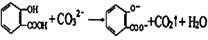
D.用铜片作阴、阳极电解硝酸银溶液:4Ag+2H2O
4Ag+O2↑+4H
高三化学选择题简单题查看答案及解析