-
1,2,3,4—四氢化萘的结构简式如下图, 分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+ 4Br2→ C10H8Br4+ 4HBr生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:


①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉。
②慢慢滴入液溴,不断搅拌,直到反应完全。
③取下反应容器,补充少量四氢化萘,直到溶液颜色消失。过滤,将滤液倒入分液漏斗,静置。
④ 分液,得到的“水层”即氢溴酸溶液。
回答下列问题:
(1) 如图所示的装置, 适合步骤①和②的操作的是________。
(2) 步骤②中如何判断“反应完全”_________________________________________。
(3) 步骤③中补充少量四氢化萘的目的是________。
(4) 步骤③中过滤后得到的固体物质是_____________________________。
(5) 已知在实验条件下,饱和氢溴酸溶液中氢溴酸的质量分数是66%,如果溴化反应进行完全,则步骤①中水和四氢化萘的质量比约是1:____________(保留小数点后1位)。
-
二氧化硫常温下为无色有刺激性气味的有毒气体,易液化,易溶于水。某同学设计如下实验方案,对二氧化硫的化学性质进行探究,装置如下图所示。请回答下列问题:
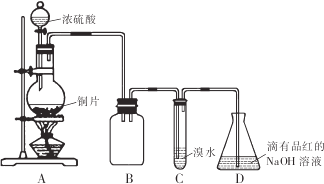
(1)反应结束时烧瓶中Cu由剩余,某同学认为H2SO4也有剩余,他设计了下列实验方案来测定剩余H2SO4的量。经冷却,定量稀释后进行下列实验,能达到的目的是 (填序号)
a.用酸碱中和滴定法测定
b.与足量Zn反应,测量生成H2的体积
c.用pH计测溶液PH值
d.与足量BaCl2溶液反应,称量生成沉淀的质量
(2)装置B的作用是 ,设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式 ,装置D中NaOH全部转化为NaHSO3的标志是____________
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能情况:
I.HSO3-与ClO-刚好反应完; Ⅱ.NaClO不足; Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请你完成下表:(已知酸性:H2SO3>H2CO3>HClO)
| 实验序号 | 实验操作 | 现象 | 反应的可能情况 |
| ① | 加入几小块CaCO3固体 | 有气泡产生 | |
| ② | 滴加少量淀粉KI溶液,振荡 | | Ⅲ |
| ③ | 滴加少量溴水,振荡 | | Ⅱ |
| ④ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液为紫色 | |
(4)设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小 。
-
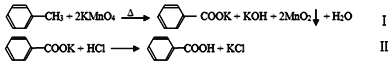
制备苯甲酸的反应原理及有关数据如下:
| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 溶解度 |
| 甲苯 | 92 | 无色液体 | -95℃ | 110℃ | 不溶于水 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122℃ | 248℃ | 微溶于水 |
| 高锰酸钾 | 158 | | | | 易溶于水 |
实验过程如下: ①将高锰酸钾、水和氢氧化钠溶液混合摇匀后,加入甲苯,采用电磁搅拌,加热(但温度不要太高),冷凝回流2h。如仍有高锰酸钾的紫色存在,则加数滴乙醇。 ②将混合液过滤后冷却。③滤液用盐酸酸化,析出白色晶体过滤,洗涤,干燥,得到苯甲酸的粗产品,最后测定其熔点。回答下列问题:
(1)①中反应易暴沸,本实验中采用______方法防止此现象;乙醇的作用是____________________。
(2)②中过滤出的沉淀是____________________。
(3)③中测定熔点时,发现到130℃ 时仍有少量不熔,推测此不熔物的成分是____________________。
(4)提纯苯甲酸粗产品的方法是____________________。
-
(14分)正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
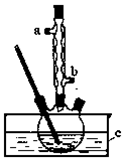
实验过程如下:在容积为100mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚。回答下列问题:
(1)合成粗产品时,液体试剂加入顺序是 。
(2)实验中冷凝水应从 口出去(填“a”或“b”)。
(3)为保证反应温度恒定在135℃,装置C中所盛液体必须具有的物理性质为 。
(4)加热时间过长或温度过高,反应混合液会变黑,写出用NaOH溶液吸收有毒尾气的离子方程式 。
(5)得到的正丁醚粗产品依次用8 mL50%的硫酸、10 mL水萃取洗涤。该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、 。该仪器使用前需要 。
(6)将分离出的有机层用无水氯化钙干燥,过滤后再进行 (填操作名称)精制得到正丁醚。
(7)本实验最终得到6.50g正丁醚,则正丁醚的产率是 。
-
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4 ℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去):

实验过程如下:在容积为100 mL的三颈烧瓶中加入5 mL浓硫酸、14.8 g正丁醇和几粒沸石,迅速升温至135 ℃,一段时间后,收集到粗产品,精制得到正丁醚。回答下列问题:
(1)制取正丁醚的化学方程式为____________。
(2)合成粗产品时,液体试剂加入顺序是____________。
(3)实验中冷凝水应从____________口进入(填“a”或“b”)。
(4)为保证反应温度恒定在135℃,装置C中所盛液体必须具有的物理性质为____________。
(5)得到的正丁醚粗产品依次用8 mL50%的硫酸、10 mL水萃取、洗涤、分液。该步骤中需要的玻璃仪器是烧杯、玻璃棒、____________。
(6)将分离出的有机层用无水氯化钙干燥,过滤后再进行____________(填操作名称)精制得到正丁醚。
-
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
实验过程如下:在容积为100mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚。回答下列问题:
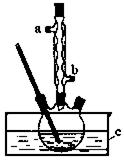
(1)合成粗产品时,液体试剂加入顺序是_______。
(2)实验中冷凝水应从_______口出去(填“a”或“b”).
(3)为保证反应温度恒定在135℃,装置C中所盛液体必须具有的物理性质为_______。
(4)加热时间过长或温度过高,反应混合液会变黑,写出可能发生的有机副反应的化学方程式:_______,用NaOH溶液吸收有毒尾气的离子方程式_______。
(5)得到的正丁醚粗产品依次用8mL 50%的硫酸、10mL水萃取洗涤。该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、_______,将分离出的有机层用无水氯化钙干燥,过滤后再进行_______(填操作名称)精制得到正丁醚。
(6)本实验最终得到6.50g正丁醚,则正丁醚的产率是_______。
-
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
实验过程如下:在容积为100mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚.回答下列问题:
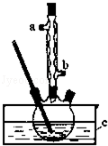
(1)合成粗产品时,液体试剂加入顺序是 .
(2)实验中冷凝水应从 口出去(填“a”或“b”).
(3)为保证反应温度恒定在135℃,装置C中所盛液体必须具有的物理性质为 .
(4)加热时间过长或温度过高,反应混合液会变黑,写出用NaOH溶液吸收有毒尾气的离子方程式 .
(5)得到的正丁醚粗产品依次用8mL 50%的硫酸、10mL水萃取洗涤.该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、 .该仪器使用前需要 .
(6)将分离出的有机层用无水氯化钙干燥,过滤后再进行 (填操作名称)精制得到正丁醚.
(7)本实验最终得到6.50g正丁醚,则正丁醚的产率是 .
-
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2CH3CH2CH2CH2OH 3CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。
3CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。
实验过程如下:在容积为l00mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚。回答下列问题:
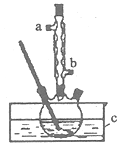
(1)合成粗产品时,液体试剂加入顺序是_________________。
(2)实验中冷凝水应从____口流出(填“a”或‘‘b”)。
(3)为保证反应温度恒定在135°C,装置C中所盛液体必须具有的物理性质为________。
(4)加热时间过长或温度过高,反应混合液会变黑,写出用浓NaOH溶液吸收有毒尾气的离子方程式________________。
(5)得到的正丁醚粗产品依次用8 mL50%的硫酸、10 mL水萃取洗涤。该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、________________________。
(6)本实验最终得到6.50g正丁醚,则正丁醚的产率是________________________。
-
二氯化二硫(S2Cl2),非平面结构,常温下是一种黄红色液体,有刺激性恶臭,熔点80℃,沸点135.6℃,对干二氯化二硫叙述正确的是
A.二氯化二硫的电子式为
B.分子中既有极性键又有非极性键
C.二氯化二硫属于非极性分子
D.分子中S-Cl键能小于S-S键的键能
-
乙酸乙酯是重要的有机物。某化学兴趣小组对乙酸乙酯的制取进行探究活动。
[查阅资料]乙酸乙酯:无色、有芬芳气味的液体,沸点77℃,熔点-83.6℃,密度0.901g/cm3,溶于乙醇、氯仿、乙醚和苯等,微溶于水,在饱和碳酸钠中溶液溶解度更小,比水轻。
[反应原理]
CH3COOH+CH3CH2OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
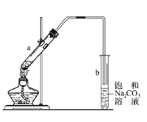
[实验探究]某化学兴趣小组设计如图装置进行实验。在大试管a内加入碎瓷片后,加入10mL乙醇,边振荡边加入5mL98%的浓H2SO4,冷却后再加入8mL冰醋酸,点燃酒精灯缓慢加热,将产生的蒸气经导管通入到试管b中的的饱和Na2CO3溶液的液面上,观察现象。
[问题讨论]
(1)试管a内加入碎瓷片的作用_______(填“防止暴沸”或“防止倒吸”);
(2)试管b中长导管没有伸入饱和Na2CO3溶液的原因是_______(填“防止暴沸”或“防止倒吸”);
(3)实验中饱和碳酸钠溶液的作用是_______________;
A.中和乙酸和乙醇
B.加速酯的生成,提高其产率
C.溶解乙醇,中和乙酸,降低乙酸乙酯的溶解,有利于分层析出。
(4)反应结束后试管b中的现象是_______;
A.溶液不分层
B.溶液分层,无色油状液体在上层
C.溶液分层,无色油状液体在下层
(5)若用9.2g乙醇与足量的冰醋酸反应,分离得到纯乙酸乙酯13.2g,反应的产率是________。








