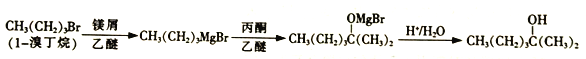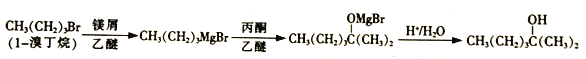-
2-甲基-2-己醇常用于合成洗涤剂、乳化剂等。实验室制备2-甲基-2-己醇的流程如下:
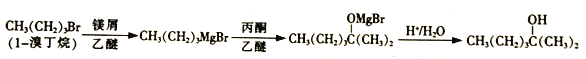
已知:RMgBr化学性质活泼,易与H2O、R'X 等发生反应生成RH、R-R'。
(1)仪器A的名称是___________。
(2)引发CH3(CH2)3Br 与镁屑反应可微热或加入米粒大小的碘单质,其中碘的作用可能是_____,若镁屑不足,则反应时生成的有机副产物为________ (填结构简式)。
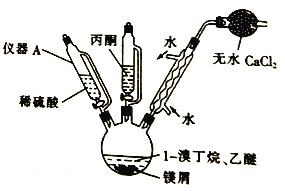
(3) 干燥管中无水氯化钙的作用为__________。
(4)加入丙酮及稀硫酸时均需用冰水冷却,这是因为_________。
(5)起始加入三颈烧瓶的1-溴丁烷的体积为5 mL,密度为1.28g/mL,最终所得产品的质量为2.71g,则2-甲基-2-己醇的产率为________。
-
2-甲基-2-己醇常用于合成洗涤剂、乳化剂等。实验室制备2-甲基-2-己醇的流程如下:
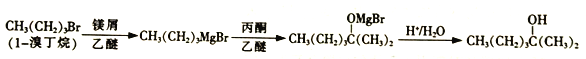
已知:RMgBr化学性质活泼,易与H2O、R'X 等发生反应生成RH、R-R'。
(1)仪器A的名称是___________。
(2)引发CH3(CH2)3Br 与镁屑反应可微热或加入米粒大小的碘单质,其中碘的作用可能是_____,若镁屑不足,则反应时生成的有机副产物为________ (填结构简式)。
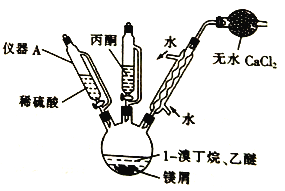
(3) 干燥管中无水氯化钙的作用为__________。
(4)加入丙酮及稀硫酸时均需用冰水冷却,这是因为_________。
(5)起始加入三颈烧瓶的1-溴丁烷的体积为5 mL,密度为1.28g/mL,最终所得产品的质量为2.71g,则2-甲基-2-己醇的产率为________。
-
CuCl常用于有机合成催化剂,并用于颜料、防腐等。工业上以黄铜矿 主要成分是
主要成分是 ,含有少量
,含有少量 为主要原料制备CuCl的主要流程如下:
为主要原料制备CuCl的主要流程如下:
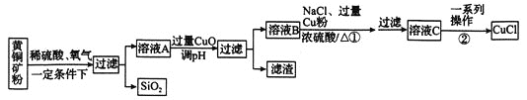
已知:CuCl难溶于水和乙醇,在空气中易被氧化,在水溶液中存在平衡: 白色
白色 无色溶液
无色溶液 。
。
回答下列问题:
 滤渣的主要成分是________
滤渣的主要成分是________ 填化学式
填化学式 。
。
 溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
 ①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
 ②中的一系列操作是________。
②中的一系列操作是________。
 已知:常温下
已知:常温下 ,
, 。若溶液A中
。若溶液A中 ,加入氧化铜
,加入氧化铜 忽略溶液体积变化
忽略溶液体积变化 ,使溶液中
,使溶液中 恰好沉淀完全,此时是否有
恰好沉淀完全,此时是否有 沉淀生成_______
沉淀生成_______ 列式计算
列式计算 。
。 已知:溶液中离子浓度
已知:溶液中离子浓度 时可认为沉淀完全
时可认为沉淀完全 。
。
 工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
-
氯化亚铜(CuCl)为白色粉末,微溶于水。常用作有机合成催化剂,并用于颜料、防腐等工业。实验室可采用亚硫酸钠还原氯化铜的方法制备氯化亚铜,主要流程如图所示:
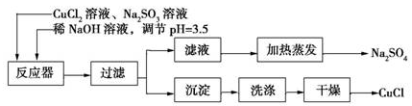
(1)上述方法制备氯化亚铜的化学方程式为_________________ 。
。
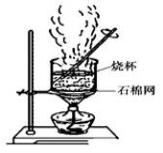
(2)下图是加热蒸发滤液,回收Na2SO4的装置。装置图中存在一处严重错误,该错误是_____________。
(3)洗涤产品氯化亚铜沉淀的试剂是___________,检验沉淀是否洗涤干净的方法是_______________。
(4)CuCl的盐酸溶液能吸收 一氧化碳而生成氯化羰基亚铜[Cu2Cl2(CO)2·2H2O]。下图是用CO(含有CO2杂质)还原CuO并验证其氧化产物的实验装置图。
一氧化碳而生成氯化羰基亚铜[Cu2Cl2(CO)2·2H2O]。下图是用CO(含有CO2杂质)还原CuO并验证其氧化产物的实验装置图。
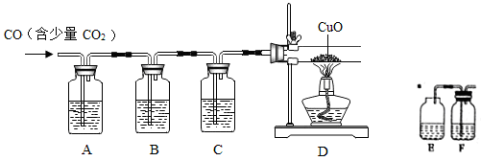
装置A中盛装的是饱和NaOH溶液,该装置的作用是_____________,装置B盛有澄清的石灰水,其中装置B的作用是___________,盛装CuCl的盐酸溶液的装置是____________(选填装置中提供的装置字母代号)。
-
氯化亚铜(CuCl)为白色粉末,微溶于水。常用作有机合成催化剂,并用于颜料、防腐等工业。实验室可采用亚硫酸钠还原氯化铜的方法制备氯化亚铜,主要流程如图所示:
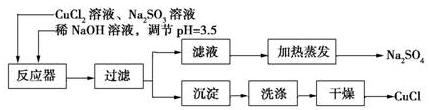
(1)上述方法制备氯化亚铜的化学方程式为_________________。
(2)下图是加热蒸发滤液,回收Na2SO4的装置。装置图中存在一处严重错误,该错误是_____________。
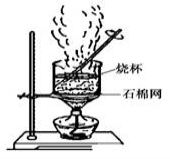
(3)洗涤产品氯化亚铜沉淀的试剂是____________,检验沉淀是否洗涤干净的方法是_______________。
(4)CuCl的盐酸溶液能吸收一氧化碳而生成氯化羰基亚铜[Cu2Cl2(CO)2·2H2O]。下图是用CO(含有CO2杂质)还原CuO并验证其氧化产物的实验装置图。

装置A中盛装的是饱和NaOH溶液,该装置的作用是______________,装置B盛有澄清的石灰水,其中装置B的作用是_____________,盛装CuCl的盐酸溶液的装置是__________(选填装置中提供的装置字母代号)。
-
(15分)草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如下:
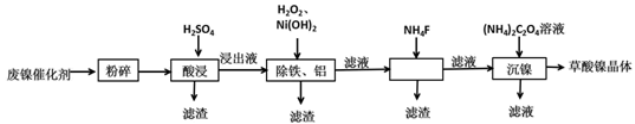
已知:①Ksp(CaF2)=1.46×10﹣10,Ksp(CaC2O4)=2.34×10﹣9。
②相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为0.1mol• L﹣1计算).
L﹣1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
(1)“粉碎”的目的是 。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为 (填字母).
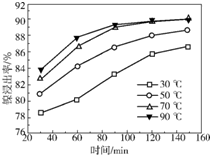
a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象是 ,将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是 。
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为 ,第2步中加入适量NH4F溶液的作用是 。
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式: 。
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得 kg草酸镍晶体。(Ni:59,C:12,H:1,O:16)
-
(14分)草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如下:
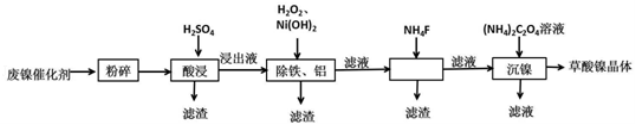
已知:①Ksp(CaF2)=1.46×10﹣10,Ksp(CaC2O4)=2.34×10﹣9.
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
②相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为1.0mol∙L﹣1计算).
(1)“粉碎”的目的是 .
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图.“酸浸”的适宜温度与时间分别为 (填字母).
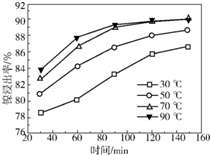
a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象是 .将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是 .
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为 .第2步中加入适量NH4F溶液的作用是 .
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式: .
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得 kg草酸镍晶体(Ni:59,C:12,H:1,O:16).
-
(16分)草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如下:
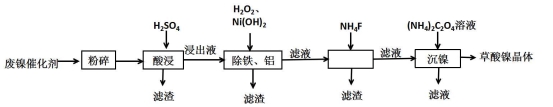
已知:①Ksp(CaF2)=1.46×10-10,Ksp(CaC2O4)=2.34×10-9。
②相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
(1)“粉碎”的目的是 。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为 (填字母)。
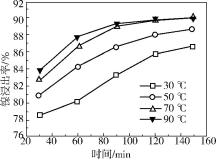
a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象是 。将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110 ℃下烘干,得草酸镍晶体。用75%乙醇溶液洗涤的目的是 。
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为 。第2步中加入适量NH4F溶液的作用是 。
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式: 。
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得 kg草酸镍晶体(Ni:59,C:12,H:1,O:16)。
-
MnO2是一种重要的化工原料,可用于合成工业的催化剂和氧化剂。采用软锰矿(主要成分为MnO2)可制备高纯MnO2,其流程如下:

下列叙述错误的是
A. “含Mn2+、A13+的溶液”中还含Fe3+
B. 加入“氨水”同时搅拌,搅拌的目的是提高反应速率
C. “滤渣”可完全溶解在NaOH溶液中
D. 电解含Mn2+的溶液,MnO2为阳极产物
-
三氯氧磷(POCl3) 俗名磷酰氯、氧氯化磷,是重要的基础化工原料,可用于制取染料、农药,有机合成的氯化剂、催化剂和阻燃剂等。某化学实验小组模拟PCl3直接氧化法制备POCl3,其实验装置设计如下:
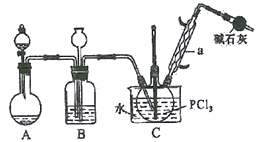
有关物质的部分性质如下表:
| 熔点/℃ | 沸点/℃ | 其他 |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
回答下列问题:
(1)仪器a的名称是__________,装置A中发生反应的化学方程式为__________________。
(2)B中所装试剂为__________,B装置的作用除观察O2的流速之外,还有_____________________。
(3)C装置控制反应在60℃~65℃进行,其控温的主要目的是__________。
(4) 实验制得的POCl3粗产品中常含有PCl3,可用__________方法提纯。
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液40.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖,以防止在滴加NH4SCN 时,将AgCl沉淀转化为AgSCN沉淀。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
已知: Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是__________ (填标号)。
a.FeCl2 b.甲基橙 c.淀粉 d.NH4Fe(SO4)2
②Cl元素的质量百分含量为__________ (列出算式)。
③在步骤Ⅲ中,若无加入硝基苯的操作,所测Cl-元素含量将会__________ (填“偏大”“偏小”或“不变”)。