-
按要求回答有关问题:
(1)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。则H2S的平衡转化率为______%,反应平衡常数K=________。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。则H2S的平衡转化率为______%,反应平衡常数K=________。
(2)已知25℃,NH3·H2O的Kb=1.8×10−5,H2SO3的Ka1=1.3×10−2,Ka2=6.2×10−8。若氨水的浓度为2.0 mol·L−1,溶液中的c(OH−)=_________________ mol·L−1。将SO2通入该氨水中,当c(OH−)降至1.0×10−7 mol·L−1时,溶液中的c( )/c(
)/c( )=___________________。
)=___________________。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为_______ mol·L−1,此时溶液中c(CrO42−)等于__________ mol·L−1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。
-
Ⅰ(1)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。则H2S的平衡转化率为______%,反应平衡常数K=________。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。则H2S的平衡转化率为______%,反应平衡常数K=________。
(2)已知25℃,NH3·H2O的Kb=1.8×10−5,H2SO3的Ka1=1.3×10−2,Ka2=6.2×10−8。若氨水的浓度为2.0 mol·L−1,溶液中的c(OH−)=_______mol·L−1,0.1 mol·L−1的(NH4)2SO3溶液显______(填“酸性”、“碱性”或“中性”)。
Ⅱ. 某学生用0.200mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是______ (填编号)。
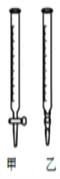
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______ 中(从图中选填“甲”或“乙”)。
(3)下列操作会引起实验结果偏大的是:______ 填编号
填编号 。
。
A. 在锥形瓶装液前,留有少量蒸馏水
B. 滴定前,滴定管尖嘴有气泡,滴定后无气泡
C. 滴定终点俯视读数
-
H2S与CO2在高温下发生反应:H2S(g)+CO2(g)  COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①向反应器中再分别充入下列气体,能使H2S转化率增大的是________(填标号)。
A. H2S B. CO2 C.COS D.N2
②在620 K重复实验,平衡后水的物质的量分数为0.03,该反应的ΔH________0(填“>”“<”或“=”)。
③H2S的平衡转化率α1=_____%,反应平衡常数K=______。(第③小题要写计算过程)
-
H2S与CO2在高温下发生反应:CO2 (g) + H2S (g)  COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
A. 升高温度,H2S浓度增加,表明该反应是放热反应
B. 通入CO2后,正反应速率先增大后减小
C. H2S的平衡转化率α = 4.5 %
D. 反应平衡常数K = 2.8×10-3
-
H2S与CO2在高温下发生反应:CO2 (g) + H2S (g)  COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
A. 升高温度,H2S浓度增加,表明该反应是放热反应
B. 通入CO2后,正反应速率先增大后减小
C. H2S的平衡转化率α = 4.5 %
D. 反应平衡常数K = 1/351
-
已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) ==COS(g)+H2O(g),在610K时,将0.1mol CO2加入与0.40molH2S充入2.5mL的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率a1=_______%,反应平衡常数K=___________。
②在620K重复试验,平衡后水的物质的量分数为003,H2S的转化率a2____a1,该反应的ΔH___0。(填“>”“<”或“=”)
-
按要求回答问题。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应: COS(g)+ H2O(g) H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) H2S(g)+CO(g) △H=+7kJ/mol
H2S(g)+CO(g) △H=+7kJ/mol
己知: 2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol
写出表示CO燃烧热的热化学方程式:_______________。
(2)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11;草酸H2C2O4,K1=5.9×10-2,K2=6.4×10-5; 0.1mol/LNa2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)。若将等分浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是___________。(选填编号)
A.c(H+)>c(HC2O4-)> (HCO3-)>c (CO32-)
B.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
D.c(H2CO3) >c(HCO3-)>c(HC2O4-)>c(CO32-)
(3)已知:①难溶电解质的溶度积常数:Ksp(CaF2)=1.5×10-10;②25℃时2.0×10-3mol/L氢氟酸水溶液中,调节溶液pH(忽略体长变化),得到c(HF)、c(F-) 与溶液pH 的变化关系,如图所示:
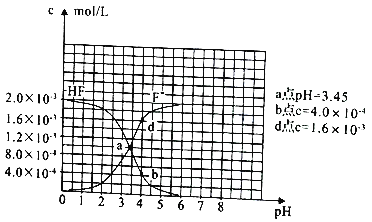
请根据信息回答下列问题:
①25℃时,HF电离平衡常数的数值Ka≈_______。
②4.0×10-3mol/LHF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。____________。
-
按要求回答问题。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应: COS(g)+ H2O(g) H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) H2S(g)+CO(g) △H=+7kJ/mol
H2S(g)+CO(g) △H=+7kJ/mol
己知: 2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol
写出表示CO燃烧热的热化学方程式:_______________。
(2)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11;草酸H2C2O4,K1=5.9×10-2,K2=6.4×10-5; 0.1mol/LNa2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)。若将等分浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是___________。(选填编号)
A.c(H+)>c(HC2O4-)> (HCO3-)>c (CO32-)
B.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
D.c(H2CO3) >c(HCO3-)>c(HC2O4-)>c(CO32-)
(3)已知:①难溶电解质的溶度积常数:Ksp(CaF2)=1.5×10-10;②25℃时2.0×10-3mol/L氢氟酸水溶液中,调节溶液pH(忽略体长变化),得到c(HF)、c(F-) 与溶液pH 的变化关系,如图所示:
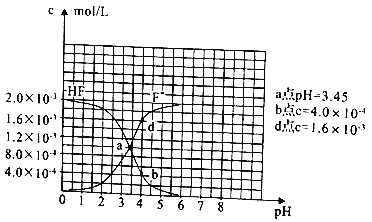
请根据信息回答下列问题:
①25℃时,HF电离平衡常数的数值Ka≈_______。
②4.0×10-3mol/LHF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。____________。
-
H2S与CO2高温下发生反应:H2S(g)+CO2(g)  COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)H2S的平衡转化率α1=________%,反应平衡常数K=___________________。
(2)在620K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率α2________α1,该反应的ΔH____0(填“>”“<”或“=”)。
(3)向反应器中再分别充入下列气体,能使H2S转化率增大的是______(填标号)。
A.H2S B.CO2 C.COS D.N2
-
已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)△H=﹣Q kJ•mol﹣1 (Q>0)。在温度为T1时,将0.10molCO2与0.40mol H2S充入2.5L 的空钢瓶中,经过4min反应达到平衡,平衡时H2O(g)的物质的量分数为 2%,则下列说法不正确的是( )
A.0~4 min内用H2S表示该反应的速率为0.001 mol•L﹣1•min﹣1
B.CO2的平衡转化率α=2.5%
C.上述条件下反应达到平衡时放出的热量为0.01Q kJ
D.其他条件不变,若该反应在温度为T2 条件下进行,达到平衡所需时间小于4 min,则 T1<T2
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。则H2S的平衡转化率为______%,反应平衡常数K=________。
)/c(
)=___________________。


