向10 mL 0.1 mol·L-1Na2CO3溶液中逐滴滴加V mL 0.1 mol·L-1HCl溶液,下列有关滴定过程中粒子浓度关系正确的是
A.当V=0时,c(OH-)=c(H+)+c()+c(H2CO3)
B.当V=5时,c(Na+)+c(H+)=2c()+c(
)+c(OH-)
C.当V=10时,c(Cl-)=c()+c(
)+c(H2CO3)
D.当V=15时,c(Na+)=c(Cl-)>c()>c(OH-)>c(H+)
高三化学选择题中等难度题
向10 mL 0.1 mol·L-1Na2CO3溶液中逐滴滴加V mL 0.1 mol·L-1HCl溶液,下列有关滴定过程中粒子浓度关系正确的是
A.当V=0时,c(OH-)=c(H+)+c()+c(H2CO3)
B.当V=5时,c(Na+)+c(H+)=2c()+c(
)+c(OH-)
C.当V=10时,c(Cl-)=c()+c(
)+c(H2CO3)
D.当V=15时,c(Na+)=c(Cl-)>c()>c(OH-)>c(H+)
高三化学选择题中等难度题
向10 mL 0.1 mol·L-1Na2CO3溶液中逐滴滴加V mL 0.1 mol·L-1HCl溶液,下列有关滴定过程中粒子浓度关系正确的是
A.当V=0时,c(OH-)=c(H+)+c()+c(H2CO3)
B.当V=5时,c(Na+)+c(H+)=2c()+c(
)+c(OH-)
C.当V=10时,c(Cl-)=c()+c(
)+c(H2CO3)
D.当V=15时,c(Na+)=c(Cl-)>c()>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析
(2013秋•金山区校级期中)向10mL 0.1mol/L Na2CO3溶液中逐滴滴加V mL 0.1mol/L HCl溶液,下列有关滴定过程中粒子浓度关系正确的是( )
A.当V=0时,[OH﹣]=[H+]+[HCO3﹣]+2[H2CO3]
B.当V=5时,[Na+]+[H+]=2[CO32﹣]+[HCO3﹣]+[OH﹣]
C.当V=10时,[Cl﹣]=[CO32﹣]+[HCO3﹣]+[H2CO3]
D.当V=15时,[Na+]=[Cl﹣]>[HCO3﹣]>[OH﹣]>[H+]
高三化学选择题中等难度题查看答案及解析
25℃时,用0.1mol·L-1HCl溶液滴定20.00mL 0.1mol·L-1BOH溶液所得的滴定曲线如图,下列说法正确的是
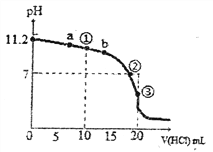
A. BOH为一元弱碱,滴定到点③时,该一元弱碱的电离平衡常数Kb约为10-5.6
B. 滴加盐酸的过程中,当溶液中c(BOH)=c(B+)时,可能出现在b点
C. 滴加盐酸的过程中水的电离程度逐渐增大,在②点时达到最大,后又逐渐减小
D. 点①所示溶液中:c(B+)+c(H+)>c(BOH)+c(OH-)
高三化学单选题困难题查看答案及解析
常温下,用0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
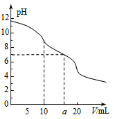
A.当V=0时:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
B.当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D.当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
高三化学选择题困难题查看答案及解析
常温下,用0.1 mol.L-1HCl溶液滴定10.0 mL浓度为0.1 mol.L-1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是 ( )
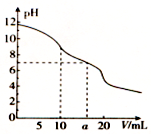
A.当V=0时:c( H+) +c( HCO3-)+c( H2 CO3) =c(OH-)
B.当V=5时:c(CO32-) +c(H)+c( H2CO3) =2c(Cl一)
C.当v=10时:c( Na+) >c( HCO3) > c(CO32-)>c( H2CO3)
D.当V=a时:c(Na+)=c(Cl一)>c(H+)=c(OH一)
高三化学选择题困难题查看答案及解析
常温下,用0.1 mol.L-1HCl溶液滴定10.0 mL浓度为0.1 mol.L-1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是 ( )
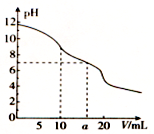
A.当V=0时:c( H+) +c( HCO3-)+c( H2 CO3) =c(OH-)
B.当V=5时:c(CO32-) +c(H)+c( H2CO3) =2c(Cl一)
C.当v=10时:c( Na+) >c( HCO3) > c(CO32-)>c( H2CO3)
D.当V=a时:c(Na+)=c(Cl一)>c(H+)=c(OH一)
高三化学选择题简单题查看答案及解析
常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如右图所示。下列说法正确的是
A.当V=0时:c(H+)+c(HCO 3-)+c(H2CO3)=c(OH-)
B.当V=5时:c(CO32—)+c(HCO 3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO 3-)>c(CO32—)>c(H2CO3)
D.当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
高三化学选择题中等难度题查看答案及解析
常温下,用 0.1 mol·L-1HCl溶液滴定10.0 mL浓度为0.1 mol·L-1 Na2CO3溶液,所得滴定曲线如如图所示。下列说法正确的是
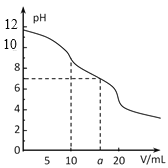
A.当V=0时:c(H+)+c(HCO 3-)+c(H2CO3)=c(OH-)
B.当V=5时:c(CO32—)+c(HCO 3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO 3-)>c(CO32—)>c(H2CO3)
D.当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
高三化学多选题中等难度题查看答案及解析
常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是
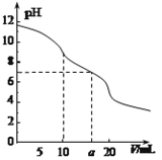
A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32—)+c(HCO3-)+c(H2CO3)=c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32—)>c(H2CO3)
D. 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
高三化学单选题困难题查看答案及解析
下列有关溶液中粒子浓度的关系式中一定不正确的是
A.在常温下,0.10mol•L﹣1Na2CO3溶液25mL 用0.10mol•L﹣1盐酸滴定.当滴定到消耗20mlHCl时所得溶液中离子浓度间的关系有:5c(Cl﹣)=4c(HCO3﹣)+4c(CO32﹣)+4c(H2CO3)
B.常温下,pH=12的氨水与pH=2的盐酸等体积混合溶液中:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
C.25℃时,0.1 mol•L﹣1pH=4.5的NaHSO3溶液中:c(HSO3﹣)>c(H2SO3)>c(SO32﹣)
D.常温下,等浓度的CH3COONa和CH3COOH混合溶液:c(CH3COO﹣)﹣c(CH3COOH)=2[c(H+)﹣c(OH﹣)]
高三化学选择题困难题查看答案及解析