-
[化学一选修3:物质结构与性质](15 分)
铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3等。
回答下列问题:
(1) UF4用Mg或Ca 还原可得金属铀。基态钙原子的核外电子排布式为__________________;熔点:MgO(2852℃)高于CaO(2614℃),原因是_______________________________;金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为_______________________________。
(2)已知:2UO2+5NH4HF2  2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是________(填选项字母)。
2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是________(填选项字母)。
a.氢键 b.配位键 c.共价键 d.离子键 e.金属键
(3)已知:3[(NH4)4[UO2(CO3)3]  3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑
3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑
①NH4+的空间构型为_____________________,与NH4+互为等电子体的分子或离子有_____(任写两种)。
②CO32-中碳原子的杂化轨道类型为___________________________。
③分解产物中属于非极性分子的是____________________(填选项字母)。
a.NH3 b. CO2 C.N2 d. H2O
(4)UO2的晶胞结构及晶胞参数如图所示:
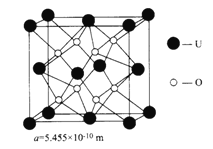
①晶胞中U 的配位数为__________________________。
②UO2晶体的密度为_____________g·cm-3(列出计算式即可。设NA表示阿伏加德罗常数的值)。
-
铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4【UO2(CO3)3】等。回答下列问题:
(1) UF4用Mg或Ca还原可得金属铀。金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为__________________;基态钙原子核外电子排布式为_________________;熔点:MgO(2852℃)高于CaO(2614℃),其原因是_____________________________。
(2)  。NH4HF2中所含作用力有____________(填字母)。
。NH4HF2中所含作用力有____________(填字母)。
a. 氢键 b. 配位键 c. 共价键 d. 离子键 e. 金属键
(3)已知: .
.
①NH4+ 的空间构型为__________________,与NH4+ 互为等电子体的分子或离子有________(写两种)
②CO32- 中碳原子杂化轨道类型为______________________。
③分解产物中属于非极性分子的是_____________________(填字母)。
a. NH3 b. CO2 c. N2 d. H2O
(4) UO2 的晶胞结构及晶胞参数如下图所示:
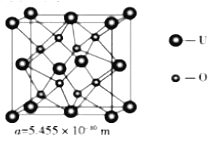
①晶胞中U的配位数为_________________。
②UO2 的密度为_________________g·cm-3(列出计算式即可,用NA表示阿伏伽德罗常数的值)。
-
铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3]等。
回答下列问题:
(1)UF4用Mg 或Ca还原可得金属铀。与钙同周期基态原子的未成对电子数为2 的元素共有___种;原子序数为镁元素的二倍的元素的基态原子价电子排布图为_______。
(2)已知:2UO2+5NH4HF2 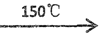 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑
HF2-的结构为[F-H…F]-
①NH4HF2中含有的化学键有__ (填选项字母)。
A.氢键 B.配位键 C.共价键 D.离子键 E.金属键
②与氧同周期,且第一电离能比氧大的元素有______种。
(3)已知:3(NH4)4[UO2(CO3)3] 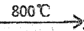 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
①写出与NH4+互为等电子体的一种分子和一种离子的化学式______、_______。
②物质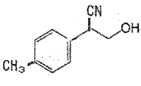 中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
③分解所得的气态化合物的分子键角由小到大的顺序为__ (填化学式)
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4 个碳原子位于立方体的面心,4 个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。
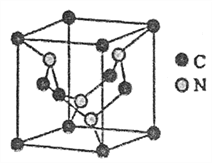
①晶胞中C 原子的配位数为______。该晶体硬度超过金刚石的原因是_________。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加德罗常数,则该晶胞的空间利用率为_______(用含d、r1、r2、NA的代数式表示,不必化简)。
-
铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3]等。
回答下列问题:
(1)UF4用Mg 或Ca还原可得金属铀。与钙同周期基态原子的未成对电子数为2 的元素共有___种;原子序数为镁元素的二倍的元素的基态原子价电子排布图为_______。
(2)已知:2UO2+5NH4HF2 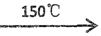 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑
HF2-的结构为[F-H…F]-
①NH4HF2中含有的化学键有__ (填选项字母)。
A.氢键 B.配位键 C.共价键 D.离子键 E.金属键
②与氧同周期,且第一电离能比氧大的元素有______种。
(3)已知:3(NH4)4[UO2(CO3)3] 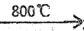 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
①写出与NH4+互为等电子体的一种分子和一种离子的化学式______、_______。
②物质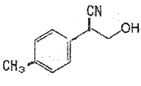 中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
③分解所得的气态化合物的分子键角由小到大的顺序为__ (填化学式)
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4 个碳原子位于立方体的面心,4 个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。
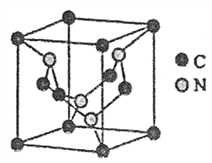
①晶胞中C 原子的配位数为______。该晶体硬度超过金刚石的原因是_________。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加德罗常数,则该晶胞的空间利用率为_______(用含d、r1、r2、NA的代数式表示,不必化简)。
-
铀是原子反应堆的原料,常见铀的化合物有UF4、UO2、及(NH4)4[UO2(CO3)3]等,回答下列问题:
(1)基态氟原子的价电子排布图为________________;用Mg或Ca还原UF4可得金属铀,其氧化产物MgF2的熔点高于CaF2,原因是_______________________________;
(2)已知:2UO2+5NH4HF2 2UF4·2NH4F+3NH3↑+4H2O↑
2UF4·2NH4F+3NH3↑+4H2O↑
①NH4HF2中存在的微粒间的作用力是__________(填选项字母)。
A.离子键 B.配位键 C.共价键 D.范德华力
②该反应中非金属元素的第一电离能由大到小的顺序是__________(填元素符号)。
(3)已知:3(NH4)4[UO2(CO3)3]  3UO2+10NH3↑+9CO2↑+ N2↑+ 9H2O↑
3UO2+10NH3↑+9CO2↑+ N2↑+ 9H2O↑
①分解产物中属于非极性分子的是_________(填选项字母)。
A.NH3 B.CO2 C.N2 D.H2O
②反应物中的CO32-的空间构型为_____________。分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则CO32-中的大
),则CO32-中的大 键应表示为______________。
键应表示为______________。
③HN3(氢叠氮酸)常用于引爆剂,其分子的结构式可表示为: 。则左边氮原子和中间氮原子的杂化方式分别为______________、_______________。
。则左边氮原子和中间氮原子的杂化方式分别为______________、_______________。
(4)UO2的晶胞结构如图所示:
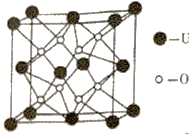
①晶胞中铀原子位于面心和顶点,氧原子填充在铀原子堆积形成的空隙中。则氧原子填充在铀原子形成的___________空隙中。(填“立方体”、“四面体”、“八面体”)
②若两个氧原子间的最短距离为a nm,则UO2晶体的密度为___________g·cm-3(列出计算式即可,设NA表示阿伏加德罗常数的值)。
-
中国的铀工业自20世纪50年代兴起,现已形成完整的和具有相当规模的科研和工业生产体系。铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4〔UO2(CO3)3〕等。回答下列问题:
(1)UF4用Mg或Ca还原可得金属铀。
①基态氟原子的价电子排布图为_____________;
②金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为_______;
③UF4用Mg或Ca还原时,其氧化产物是MgF2或CaF2,已知MgF2的熔点高于CaF2,其原因是_________________。
(2)已知:(NH4)4〔UO2(CO3)3〕 3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑
①(NH4)4〔UO2(CO3)3〕存在的微粒间作用力是_________;
a. 离子键 b. 共价键 c. 配位键 d. 金属键
②NH4+的空间构型为______,与NH4+等电子体的分子或离子有_____(写一种);
③CO32-中碳原子杂化轨道类型为_________;
(3)UO2的晶胞结构如图所示:
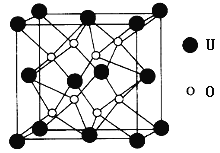
①晶胞中U原子位于面心和顶点,氧原子填充在U原子堆积形成的空隙中,在该空隙中氧原子堆积形成的立体的空间构型为___________(填“立方体”、“四面体”、“八面体”);
②若两个氧原子间的最短距离为a nm,则UO2晶体的密度为__________g·cm-3。(列出含a算式即可。用NA表示阿伏加德罗常数的值。)
-
【化学——选修3:物质结构与性质】(15分)
W、M、X、Y、Z是周期表前36号元素中的五种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)MX3-的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是___________________
_______________________________________________________________________。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
-
【化学—选修3:物质结构与性质】(15分)中学化学常见元素氮、磷、钾与氢、氧、卤素等能形成多种化合物。回答下列问题:
(1)氮、磷、钾三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(2)叠氮酸(HN3)是一种弱酸,可电离出H+和N3一。
①N3一的立体构型是 形:与N3一互为等电子体的一种分子是 (填分子式)。
②叠氮化物能与Co 3十形成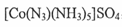 ,该配合物中心离子的配位数为 ;
,该配合物中心离子的配位数为 ;
基态钻原子的价层电子排布式为
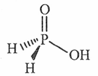
(3)磷能形成多种含氧酸,某资料认为次磷酸的结构如图。按此结构,P原子采用的杂化方式为 ,次磷酸分子中 键与
键与 键数目之比为 ,次磷酸属于 酸(填“强”或“弱,’),lmol次磷酸最多能与 mo1NaOH发生中和反应。
键数目之比为 ,次磷酸属于 酸(填“强”或“弱,’),lmol次磷酸最多能与 mo1NaOH发生中和反应。
(4)己知钾的一种化合物KIC12受热可分解,倾向于生成晶格能更大的物质。则下列化学反应更易发生的是

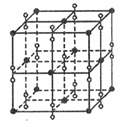
(5)钾在氧气中燃烧时得到多种氧化物,其中一种是面心立方结构,晶胞结构如下图所示。若该氧化物的密度是 ,则晶胞中最近的两个钾离子间的距离为 pm(只要求列算式,不必计算出数值,用NA表示阿伏加德罗常数的值)。
,则晶胞中最近的两个钾离子间的距离为 pm(只要求列算式,不必计算出数值,用NA表示阿伏加德罗常数的值)。
-
选考【化学——选修3:物质结构与性质】(15分)四种常见元素的性质或结构信息如F表所示,请问答下列问题。

(1)R的基态原子价层电子排布式为________,这四种元素的第一电离能由大到小的顺序为________________(写元素符号)。
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为_______,任意写出一种中心原子存在 两种杂化类型的物质的结构简式________,与A的常见单质互为等电子体的上述元素的氧化物是________。
两种杂化类型的物质的结构简式________,与A的常见单质互为等电子体的上述元素的氧化物是________。
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中 键之比为________,已知有下列两种数据:
键之比为________,已知有下列两种数据:

请解释键能大小与两种氧化物熔点、沸点高低差异过大的原因________。
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为________。

(5)A元素能形成组成为 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是________(填“极性”或“非极性”)分子,
②P的结构简式为________(AH3配体作为一个整体写)。
-
[化学——选修物质结构与性质](15分)
乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
(1)将乙炔通入 溶液生成
溶液生成 红棕色沉淀。
红棕色沉淀。 基态核外电子排布式为________。
基态核外电子排布式为________。
(2) Ca2+的原子结构示意图:________;已知 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为________ ;1mol
的电子式可表示为________ ;1mol  中含有的
中含有的 键数目为________。
键数目为________。
(3)乙炔与氢氰酸反应可得丙烯腈 。丙烯腈分子中碳原子轨道杂化类型是________;分子中处于同一直线上的原子数目最多为________。
。丙烯腈分子中碳原子轨道杂化类型是________;分子中处于同一直线上的原子数目最多为________。
(4) 晶体的晶胞结构与
晶体的晶胞结构与 晶体的相似(如下图所示),但
晶体的相似(如下图所示),但 晶体中含有的哑铃形
晶体中含有的哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个 周围距离最近的
周围距离最近的 数目为________ 。
数目为________ 。

2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是________(填选项字母)。
3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑

 。NH4HF2中所含作用力有____________(填字母)。
。NH4HF2中所含作用力有____________(填字母)。 .
.
 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑ 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑ 中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑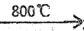 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑ 中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。
中与CO32- 的碳原子杂化类型相同和不同的碳原子的个数比为______。


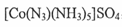 ,该配合物中心离子的配位数为
,该配合物中心离子的配位数为





 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。