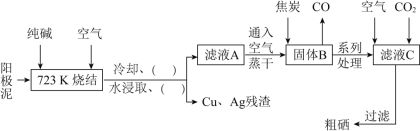-
中国的铀工业自20世纪50年代兴起,现已形成完整的和具有相当规模的科研和工业生产体系。铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4〔UO2(CO3)3〕等。回答下列问题:
(1)UF4用Mg或Ca还原可得金属铀。
①基态氟原子的价电子排布图为_____________;
②金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为_______;
③UF4用Mg或Ca还原时,其氧化产物是MgF2或CaF2,已知MgF2的熔点高于CaF2,其原因是_________________。
(2)已知:(NH4)4〔UO2(CO3)3〕 3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑
①(NH4)4〔UO2(CO3)3〕存在的微粒间作用力是_________;
a. 离子键 b. 共价键 c. 配位键 d. 金属键
②NH4+的空间构型为______,与NH4+等电子体的分子或离子有_____(写一种);
③CO32-中碳原子杂化轨道类型为_________;
(3)UO2的晶胞结构如图所示:
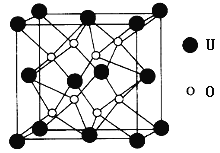
①晶胞中U原子位于面心和顶点,氧原子填充在U原子堆积形成的空隙中,在该空隙中氧原子堆积形成的立体的空间构型为___________(填“立方体”、“四面体”、“八面体”);
②若两个氧原子间的最短距离为a nm,则UO2晶体的密度为__________g·cm-3。(列出含a算式即可。用NA表示阿伏加德罗常数的值。)
-
硒(34Se)与氧同主族,硒元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥(主要成分是Se,含有CuSe、Ag2Se等杂质)为原料,提炼硒的流程如下:
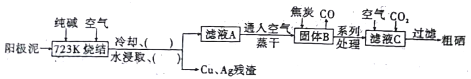
请回答下列问题:
(1)硒原子的次外层电子数_______,与硒同周期相邻元素是________(填元素名称)。
(2)已知A是Na2SeO3,可用于治疗克山病,则A的化学名称为______;C是Na2Se,则Na2Se的电子式为_______。
(3)上述流程图中的括号内“( )”,按操作先后顺序依次填写的内容是_____、_____。
(4)写出高温下用焦炭还原B的化学方程式___________________。
(5)溶液C中析出硒的离子方程式____________________。
(6)向Na2SeO3溶液中滴加稍过量的乙酸,其离子方程式为__________________。已知:Ka1(H2SeO3)=2.7×10-3、Ka2(H2SeO3)=2.5×10-8、Ka(CH3COOH)=1.8×10-5。
(7)粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:
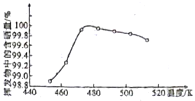
蒸馏操作中控制的最佳温度是________(填标号)。
A.455℃ B.462℃ C.475℃ D.515℃
-
硒 与氧同主族,硒元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥
与氧同主族,硒元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥 主要成分是Se,含有CuSe,
主要成分是Se,含有CuSe, 等杂质
等杂质 为原料,提炼硒的流程如下:
为原料,提炼硒的流程如下:
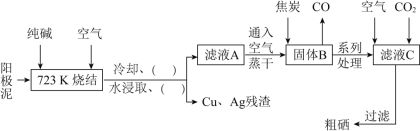
请回答下列问题:
 硒原子的次外层电子数为________,与硒同周期相邻元素是________
硒原子的次外层电子数为________,与硒同周期相邻元素是________ 填元素名称
填元素名称 。
。
 已知滤液A中主要成分是
已知滤液A中主要成分是 ,可用于治疗克山病,则
,可用于治疗克山病,则 的化学名称为________;滤液C中主要成分是
的化学名称为________;滤液C中主要成分是 ,则
,则 的电子式为________。
的电子式为________。
 上述流程图中的括号内“
上述流程图中的括号内“
 ”,按操作先后顺序依次填写的内容是________、________。
”,按操作先后顺序依次填写的内容是________、________。
 写出高温下用焦炭还原固体B的化学方程式________。
写出高温下用焦炭还原固体B的化学方程式________。
 滤液C中析出硒的离子方程式为________。
滤液C中析出硒的离子方程式为________。
 向
向 溶液中滴加稍过量的乙酸,其离子方程式为________。已知:
溶液中滴加稍过量的乙酸,其离子方程式为________。已知: 、
、 、
、 。
。
 粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:
粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:

蒸馏操作中控制的最佳温度是________ 填标号
填标号 。
。
A  B
B  C
C  D
D 
-
研究含碳化合物的结构与性质,对生产、科研等具有重要意义
(1)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。
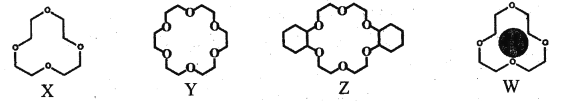
①Li+计与X的空腔大小相近,恰好能进入到X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。
a.基态锂离子核外能量最高的电子所处能层符号为___________;
b.W中Li+与孤对电子之间的作用属于___________(选填字母标号)
A.离子键 B.共价键 C.配位键 D.氢键 E.以上都不是
②冠醚Y能与K+形成稳定结构,但不能与Li+计形成稳定结构。理由是___________。
③烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶人冠醚Z,氧化效果明显提升。
i.水分子中氧的杂化轨道的空间构型是___________,H-O键键角___________(填“>”“<”或“=”)109°28′
ii.已知:冠醚Z与KMnO4可以发生右图所示的变化。加入冠醚Z后,烯烃的氧化效果明显提升的原因是___________。

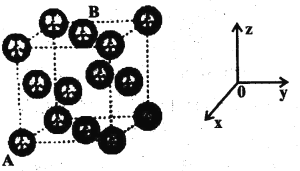
(2)甲烷是重要的清洁能源,其晶体结构如图所示,晶胞参数为anm。
①常温常压下不存在甲烷晶体。从微粒间相互作用的角度解释,其理由是___________;
②甲烷分子的配位数为___________;
③A分子中碳原子的坐标参数为(0,0,0),则B分子的碳原子的坐标参数为___________。
④甲烷晶体的密度为___________(g·cm-3)。
-
K3Fe(A2B4)3·3H2O(M)是制备负载型活性铁催化制的主要原料,也是一些有机反应催化剂,因而具有工业生产价值。A、B均为常见短周期非金属元素。某研究小组将纯净的化合物M在一定条件下加热分解,对所得气体产物有固体产物的组成进行探究。
(1)经实验分析,所得气体产物由甲、乙和水蒸气组成。甲、乙均只含A、B两种元素,甲能使澄清的石灰水交浑浊,乙常用于工业炼铁。
①写出甲的电子式:_________。
②写出工业炼铁的化学反应方程式:_______________。
(2)该研究小组查阅资料后推知,固体产物中不存在+3价铁,盐也只有K2AB3。小组同学对固体产物进行进行如图所示定量分析。

①操作I的具体操作为____________;“固体增重”说明固体产物中定含有的物质的化学式为_____________。
②写出与酸性KMnO4溶液反府的金属阳离子的离子结构示意图:_____________;用酸性KMnO4溶液去滴定该溶液时,终点颜色变化为______________。
③已知在酸州条件下KMnO4的还原产物为Mn2+,以上实验数据分析计算固体产物中各物质及它们之间的物质的量之比为_____________。
(3)写出复盐M加热分解的化学方程式:_______________。
-
[化学-选修3:物质结构与性质]
铁铜是人类最早大规模使用的金属,它们的化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)铁元素在周期表中的位置是 ,铜的基态原子核外电子排布式为 ,元素铁与铜的第二电离能分别为:ICu=1958 kJ·mol-1、IFe=1561 kJ·mol-1,ICu比IFe大得多的原因是 。
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为______________。
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:
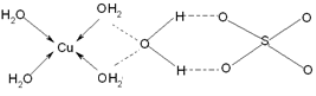
图中虚线表示_____________,SO42-的立体构型是__________,其中S原子的杂化轨道类型是___________;O原子的价电子排布图为__________________。
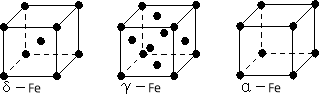
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为 。
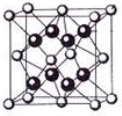
(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,该晶体中原子之间的作用力是_______________。氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如右图)相似,该晶体储氢后的化学式为 。
-
短周期主族元素W、X、Y、Z的原子序数依次增大。工业上以金红石(主要成分是TiO2)为原料制备金属钛的步骤:①在高温下,向金红石与W的单质的混合物中通入Z的气体单质,得到化合物甲和化学式为WX的常见可燃性有毒气体乙,乙燃烧火焰呈蓝色;②在稀有气体环境和加热条件下,用Y的金属单质与甲反应可得钛,下列说法不正确的是( )
A.非金属性:Z>X>W B.W与Z形成的化合物可用于工业上的重要有机溶剂
C.简单离子半径:Z>X>Y D.ZX2具有强氧化性,可用于饮用水消毒
-
短周期主族元素W、X、Y、Z的原子序数依次增大。工业上以金红石(主要成分是TiO2)为原料制备金属钛的步骤:①在高温下,向金红石与W的单质的混合物中通入Z的气体单质,得到化合物甲和化学式为WX的常见可燃性气体乙;②在稀有气体环境和加热条件下,用Y的金属单质与甲反应可得钛,下列说法不正确的是
A. 非金属性:Z>X>W
B. 简单离子半径:Z>X>Y
C. W与Z形成的化合物可用于工业上的重要有机溶剂
D. ZX2具有强氧化性,可用于饮用水消毒
-
短周期元素W、X、Y和Z的原子序数依次增大。其中W的原子半径最小,X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,且Y和Z可以形成化合物ZY2和ZY3。根据以上叙述,下列说法中正确的是
A.以上四种元素的原子半径大小为W<X<Y<Z
B.W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
-
短周期元素W、X、Y和Z的原子序数依次增大。其中W的原子半径最小,X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,且Y和Z可以形成化合物ZY2和ZY3。根据以上叙述,下列说法中正确的是
A.原子半径大小为W<X<Y<Z
B.W与X、Y、Z分别形成最简单化合物中最稳定的是Z
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑