-
(2015秋•桃源县校级月考)在热的稀H2SO4溶液中溶解了45.6g FeSO4,当加入100mL 1mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy气体逸出:□FeSO4+□KNO3+□H2SO4→K2SO4+□Fe2(SO4)3+□NxOy+□H2O据此推算出x、y的值分别为( )
A.1、2 B.1、1 C.2、1 D.2、3
高一化学选择题极难题查看答案及解析
-
(2015秋•桃源县校级月考)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,在所得的悬浊液中逐滴加入1mol•L﹣1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:
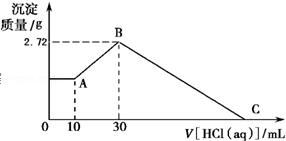
(1)从0开始到A点沉淀物的化学式为 ;B点沉淀物的化学式为 .
(2)原混合物中的MgCl2的物质的量为 ,AlCl3的物质的量为 ,NaOH的物质的量为 .
(3)HCl溶液在C点的体积数是 mL.
高一化学填空题极难题查看答案及解析
-
(2015秋•桃源县校级月考)取某铁的氧化物样品,用140mL 5mol/L盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中的Fe2+ 完全转化为 Fe3+,该样品中可能的化学式是( )
A.Fe3O4 B.Fe4O5 C.Fe5O6 D.Fe5O7
高一化学选择题困难题查看答案及解析
-
(2015秋•桃源县校级月考)配制100mL 0.1mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是( )
A.称量时,左盘高,右盘低 B.定容时,俯视读取刻度
C.容量瓶洗净后未干燥 D.定容时,液面超过了刻度线
高一化学选择题中等难度题查看答案及解析
-
(2015秋•桃源县校级月考)欲配制490mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3•10H2O晶体质量为 g.从配好的上述溶液中取出10mL溶液加水稀释至20mL,则此溶液中Na+的物质的量浓度为 mol/L.
高一化学填空题中等难度题查看答案及解析
-
(2015秋•桃源县校级月考)用NA表示阿伏加德罗常数,下列说法中正确的有( )
A.7.8gNa2O2与CO2反应,转移的电子数为0.2NA
B.1mol/L的CaCl2溶液中含Cl﹣的数目为2 NA
C.常温常压下,17g NH3含氢原子数目为3NA
D.1mol氢氧根离子中含有的电子数为9NA
高一化学选择题中等难度题查看答案及解析
-
在稀硫酸和稀硝酸的混合溶液中,加入铜粉。
(1)若将100mL 2mol/L HNO3和100mL 1mol/L H2SO4混合后,加入19.2g 铜粉,微热,充分反应。
①若忽略溶液体积变化,溶液中铜离子物质的量浓度为 mol/L
②生成气体折合成标准状况下体积 L;
③若使铜粉全部溶解,还需加入1mol/L H2SO4 mL
(2)若c(SO
)+c(NO
)=5.0 mol·L-1。取200 mL该混合酸,则能溶解铜的最大质量为 g
高一化学填空题困难题查看答案及解析
-
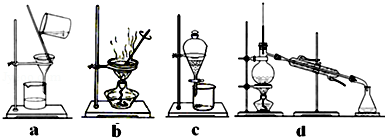
(2015秋•桃源县校级月考)下列实验操作中不正确的是( )
A.蒸发时,边加热边搅拌直至溶液完全蒸干
B.取液时,用规格为10mL的量筒量取6.2mL的液体
C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.蒸馏时,应使温度计水银球与蒸馏烧瓶的支管口齐平
高一化学选择题简单题查看答案及解析
-
(2015秋•桃源县校级月考)电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液.由该废液回收铜并得到净水剂(FeCl3•6H2O)的步骤如下:
I.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,不断通入氯气至完全反应;
IV. ,得到FeCl3•6H2O晶体.
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 .
(2)试剂A是 .
(3)步骤III反应过程中既有Fe2+又有Fe3+,如果要验证滤液中铁元素的存在形式,可另取反应过程中的两份滤液分别进行实验,实验方法、现象与结论如下表,请将其补充完整.可供选择的试剂:
a.酸性KMnO4 b.NaOH溶液 c.KSCN溶液 d.氯水
实验方法
实验现象
结论
步骤1:在滤液中加入 (填字母)
滤液中有Fe3+
步骤2:在滤液中加入 (填字母)
滤液中有Fe2+
(4)完成步骤IV需要用到的实验装置是 (填字母).
高一化学实验题极难题查看答案及解析
-
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量硫酸铁、硫酸亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeSO4溶液时需加入少量铁屑,其目的是__。
(2)甲组同学取2mLFeSO4溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeSO4溶液与氯水反应的离子方程式为___。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeSO4溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是__。
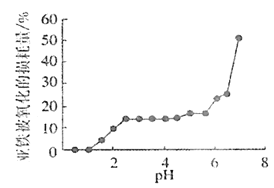
(4)丙组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为__。(写出一条即可)
(5)丁组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:
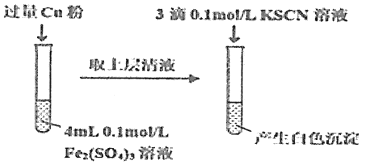
①Fe3+与Cu反应的离子方程式为__。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
ii.2Cu2++4I-=2CuI↓+I2。
填写实验方案:
实验方案
现象
步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。
无明显现象
步骤2:取4mL_mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。
产生白色沉淀
Cu2+与SCN-反应的离子方程式为__。
高一化学实验题中等难度题查看答案及解析