-
(2015秋•桃源县校级月考)欲配制490mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3•10H2O晶体质量为 g.从配好的上述溶液中取出10mL溶液加水稀释至20mL,则此溶液中Na+的物质的量浓度为 mol/L.
高一化学填空题中等难度题查看答案及解析
-
(2015秋•桃源县校级月考)配制100mL 0.1mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是( )
A.称量时,左盘高,右盘低 B.定容时,俯视读取刻度
C.容量瓶洗净后未干燥 D.定容时,液面超过了刻度线
高一化学选择题中等难度题查看答案及解析
-
实验室需要490mL 0.1mol•L-1 NaOH溶液,请回答下列问题:
(1)需称取 ___________g的烧碱固体,固体应放在 _______________中在托盘天平上称量.
(2)配制的玻璃仪器除烧杯和玻璃棒,还需要_______、______。
(3)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是 __________________________________(填序号)(操作可重复选)
(4)在容量瓶内确定溶液体积的过程中,完成后期加入少量水的做法是: _________________。
(5)下列各项中,可能导致实际浓度偏高的是 _________(填标号).
A.定容时,仰视容量瓶的刻度线
B.NaOH溶解时放出大量的热,未冷却立即配制溶液
C.溶解NaOH固体之后的烧杯未洗涤
D.向容量瓶中转移溶液时不慎洒出
(6)将取出10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为 __________。
高一化学实验题中等难度题查看答案及解析
-
用Na2CO3·10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。配制时涉及到如下操作:
①轻轻振荡容量瓶(振荡时不能将溶液溢出刻度线外),使溶液充分混合
②用天平称量纯净的Na2CO3·10H2O晶体 g
③待烧杯中的溶液冷却后沿玻璃棒小心地注入 (填容量瓶规格)容量瓶中
④将容量瓶用瓶塞盖好,反复上下颠倒、摇匀
⑤将配制好的溶液倒入干燥、洁净的试剂瓶中,贴好标签备用
⑥将称量好的固体放入烧杯中,加入适量的蒸馏水使固体完全溶解
⑦改用 加蒸馏水至溶液的凹液面正好与刻度线相切
⑧用蒸馏水洗涤烧杯内壁2~3次,将每次洗涤后的溶液也都注入容量瓶中
⑨向容量瓶中注入蒸馏水,直到容量瓶中的液面接近容量瓶刻度处1cm~2cm处
(1)请完成操作中的空余部分,
② ,③ ,⑦ 。
(2)在下列选项中选择正确的操作顺序 。
A.②⑥③④①⑦⑧⑨⑤ B.②⑥③⑧①⑨⑦④⑤
C.②③①④⑥⑦⑧⑨⑤ D.②③①⑥⑦⑧⑨④⑤
(3)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体准确称量后,失去了部分结晶水再溶解
②容量瓶未干燥用来配制溶液
③转移溶液后,未洗涤烧杯和玻璃棒
④定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
⑤定容时俯视刻度线
⑥溶解固体后,未等溶液冷却至室温立即转移到容量瓶定容
其中引起所配溶液浓度偏高的有______________(填序号,下同),偏低的有________________,无影响的有__________________。
(4)容量瓶所不具备的功能有________。(多项选择)
A.配制某浓度的稀硫酸 B.测量溶液的体积
C.用来溶解固体溶质 D.长期贮存溶液
高一化学实验题困难题查看答案及解析
-
某同学进行实验研究时,需要配制500mL 0.1mol•L﹣1 Na2CO3溶液.
(1)经过计算,使用托盘天平应该称量______g Na2CO3固体;
(2)配制溶液时,除了托盘天平、药匙、量筒、烧杯、玻璃棒外,还需要的仪器有______;
(3)配制溶液时,需经过称量、溶解、转移溶液、______、定容、摇匀等操作.下列图示对应的操作规范的一个是______;
A 称量

B 溶解
C 转移
D 转移
(4)误差(填偏高、偏低、无影响)
若配制溶液时,洗干净的容量瓶中残留有少量蒸馏水,则所配溶液的浓度______;若摇匀后发现液面低于刻度线,又加入少量蒸馏水与刻度线相平,则所配溶液的浓度______.
高一化学实验题中等难度题查看答案及解析
-
I、实验室需要490 mL 0.1 mol·L—1 Na2CO3溶液,现用Na2CO3·10H2O晶体配制,请回答下列问题:

(1) 应该用托盘天平称取Na2CO3·10H2O____________g。
(2) 如图Ⅰ表示10 mL量筒中液面的位置,A与C刻度间
相差1 mL,如果刻度A为8,量筒中液体的体积是____________mL。
(3) 实验中出现下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.定容前容量瓶底部有水珠____________;
B.定容时加水超过刻度线____________;
C.最终定容时俯视观察液面____________。
II、用9mol/L的硫酸稀释成0.9mol/L的稀硫酸100mL,回答下列问题:
(1)配制操作可分解成如下几步,以下正确的操作顺序是A、D、E、C、____________。
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C.用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线1~2 cm
(2) 如果实验室用98%的浓硫酸(密度约为1.8g·cm-3 ) 配制3.6 mol·L-1的稀硫酸250mL。计算用量简量取所需浓硫酸的体积为____________mL。
(3)由于错误操作, 使得到的浓度数据比正确的偏大的是____________(填写序号)。
A.浓硫酸加水后马上转移到容量瓶中
B.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
C.定容时,滴加蒸馏水,不小心液面略高于了刻度线,吸出少量水使液面凹面与刻度线相切
D.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
高一化学填空题中等难度题查看答案及解析
-
实验室配制500 mL 0.2 mol·L-1的Na2CO3溶液,下列说法错误的是( )
A. 称量时,若将Na2CO3固体置于托盘天平右盘,将导致所配溶液浓度偏小
B. 将Na2CO3固体置于烧杯中溶解,冷却后转移到容量瓶中
C. 定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线
D. 将配制好的Na2CO3溶液转移至带橡胶塞的试剂瓶中
高一化学单选题中等难度题查看答案及解析
-
(1)在________mL 0.2 mol/L NaOH溶液中含1 g溶质;配制480 mL 0.2 mol/L CuSO4溶液,需要用托盘天平称量CuSO4·5H2O _________g。( 已知:NaOH-40 CuSO4-160 )
(2)取100 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到29.02 g白色沉淀,用过量稀盐酸处理后沉淀量减少到9.32 g,并有气体放出。原混合溶液中Na2SO4的物质的量浓度为________mol·L-1;产生的气体在标准状况下的体积为________L。( 已知:BaCO3-197 BaSO4-233)
(3)在实验室将16.8g固体NaHCO3加热一段时间后,测得剩余固体的质量变为13.7g.则有______ g NaHCO3固体发生了分解反应。若继续对剩余固体加热,至不再产生气体后,冷却后的固体的质量是________ g。( 已知:NaHCO3-84 Na2CO3-106 )
(4)向1L AlCl3和FeCl3混合溶液中加入含6 mol NaOH的溶液时,产生的沉淀量可达最大值,继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到7mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为_______ mol/L。
高一化学计算题中等难度题查看答案及解析
-
用碳酸钠晶体(Na2CO3•10H2O),配制0.2mol/L的Na2CO3溶液480mL。
(1)所需主要仪器为:药匙、托盘天平、烧杯、玻璃棒、_________和胶头滴管。
(2)本实验所需称量碳酸钠晶体(Na2CO3•10H2O)_________g;
(3)根据下列操作对所配溶液的浓度产生的影响,完成下列要求。
①Na2CO3•10H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有_________,偏低的有__________,无影响的有_________。(填序号)
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
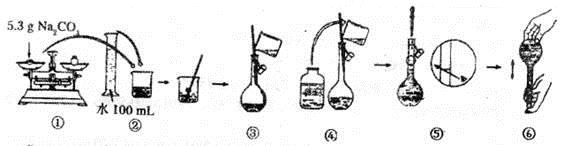
你认为该同学的操作步骤中错误(包含遗漏)之处有___________。
A.1处
B.2处
C.3处
D.4处
高一化学实验题简单题查看答案及解析
-
实验室需要配制240 mL 0.2 mol·L-1 的Na2CO3溶液,回答下列问题:
(1)需称量Na2CO3·10H2O的质量 g。
(2)配制时各步骤操作如下,其正确的操作顺序是(用字母表示,每个字母只能用一次) 。
A.用30 mL水洗涤烧杯和玻璃棒2~3次,将洗涤液均注入容量瓶,振荡
B.用称取所需质量的Na2CO3·10H2O 固体,放入烧杯中,再加入适量的蒸馏水,用玻璃棒慢慢搅动,使其完全溶解
C.将已冷却的溶液沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1﹣2 cm处
(3)下列操作会使所配溶液浓度偏高的是 。
A.所选用的溶质已经变质,部分已失去了结晶水
B.转移前,容量瓶中含有少量蒸馏水
C.将未冷却的溶液沿玻璃棒注入容量瓶中
D.定容时,仰视刻度线
E.称量时误操作为“左码右物”
F.定容后使溶液混匀静止,发现凹液面低于刻度线,立即滴蒸馏水至刻度线
(4)取所配制的碳酸钠溶液125 mL,向其加入125 mL 0.3 mol·L-1的硫酸溶液,待充分反应后,生成的气体在标准状况下所占的体积为(假设产生的气体全部逸出)________mL;设反应后溶液的体积为250 mL,则反应后溶液中Na+的物质的量浓度为____________。
高一化学实验题中等难度题查看答案及解析