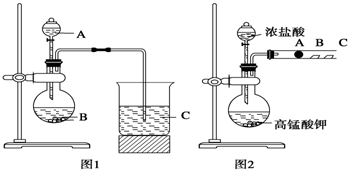
根据图1回答:(1)写出选用物质的名称:A______,B______
C______;
(2)烧瓶中反应的离子方程式为______;
烧杯中反应的离子方程式为______;
根据图2回答:(3)乙同学的实验原理是____________;
(4)B处的实验现象是______;
(5)B处的反应的离子方程式:______.
高三化学解答题中等难度题

高三化学解答题中等难度题

高三化学解答题中等难度题查看答案及解析
(12分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si元素非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
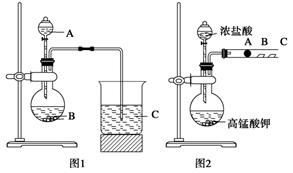
(1)甲同学设计实验的依据是_____________________________________________;
写出选用物质的名称:A____________,B__________,C____________;
反应的离子方程式为__________________________________________________________。
(2)乙同学的实验原理是__________________________________________;
写出B处的离子方程式: ___________________________________________________。
高三化学实验题简单题查看答案及解析

高三化学解答题中等难度题查看答案及解析
某研究性学习小组设计了一组实验来探究元素周期律。甲同学一次性完成N、C、Si的非金属性强弱的比较;乙同学完成了氧元素的非金属性比硫强的实验。
(1)从以下所给物质中选出甲同学设计的实验所用到物质:稀
溶液
稀盐酸
碳酸钙
溶液
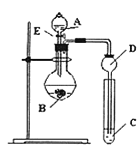
试剂A为______;试剂C为______填序号
(2)乙同学设计的实验所用到试剂A为______;装置C中反应的化学方程式为______。
高三化学实验题中等难度题查看答案及解析
在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、______、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
| 实验过程 | 预期现象 | 实际观察到的现象 |
| a取已切去表皮的一小块金属钠,放入盛有水的某容器中 | 立即剧烈反应 | 开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b向盛有适量水(内含2滴 | 有气泡产生,溶液变红色 | 没有相应现象,加热后仍无明显变化 |
| c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片 | 镁、铝与盐酸反应产生气泡剧烈程度不同 | 镁与盐酸反应产生气泡速率较快 |
①你认为a、b两步实验中出现异常现象的可能原因是:
a_______________________________________;
b___________________________________________。
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为____________________。
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是____________________。
高三化学实验题简单题查看答案及解析
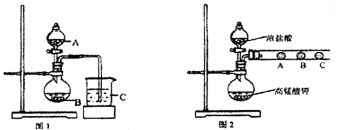
Ⅰ、某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
(1)甲同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其设计的依据是 ;但该装置存在缺陷,请指出 。
(2)乙同学设计了如图2装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。乙同学可能观察到的现象
A. ;B. ;C. 。
从环保角度考虑,该装置有明显不足,请指出提出改进建议 。
Ⅱ、另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:电解时,粗铜应与电源的 极相连。阴极上的电极反应式为 。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
| 序号 | 反应 | 平衡常数 |
| 1 | |
|
| 2 | |
|
请根据以上信息简要解释溶解阳极泥不用王水的原因 。
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程。

则滤液中
的浓度为
,
的浓度为
。
高三化学实验题极难题查看答案及解析
锡是第ⅣA族第五周期金属元素,四氯化锡(SnCl4)是重要的媒染剂,易与水反应,熔点为-33℃、沸点为114℃,某研究性学习小组设计如下装置(部分夹持装置及加热仪器省略,MnO2过量)制备SnCl4。
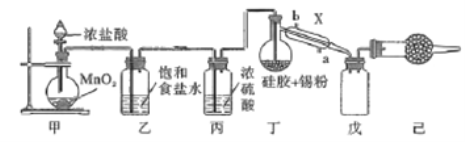
(1)仪器X的名称是_____,加热装置丁前要先排出装置内的空气,排出空气的目的是______,排出空气的方法是_______
(2)锡粉被吸附在硅胶上,其优点是______,甲中反应的离子方程式_______
(3)装置己中的试剂是________,实验过程中,乙装置内可观察到的明显现象是__________
(4)设计一种实验方案,证明在MnO2过量的情况,盐酸仍无法反应完______________。
高三化学实验题中等难度题查看答案及解析
某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。甲同学取钠、镁、锡各1 mol分别投入到足量的盐酸中,预测实验结果。
(1)甲同学设计实验的目的是______。
(2)与盐酸反应最剧烈的是______。
(3)利用如图所示装置可以验证非金属性的变化规律。
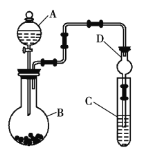
①仪器A的名称为______,干燥管D的作用是______。
②实验室中现有药品:溶液、
、浓盐酸、
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为______、______、______,装置C中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______。
③若要证明非金属性:,则A中加______,B中加
,C中加______,观察到C中的现象为______。
高三化学实验题中等难度题查看答案及解析
某研究性学习小组设计两套实验方案制备氨气并探究其还原性(部分夹持装置已省略)。
甲方案:如图所示。
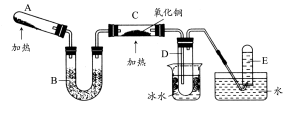
乙方案:如图所示。
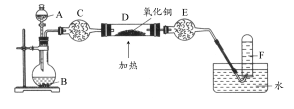
根据方案回答下列问题:
(一)甲方案
(1)B装置盛装碱石灰,A装置中药品可以是 。
a.氯化铵固体和烧碱 b.碳酸氢铵固体
c.氯化铵固体 d.硫酸铵和熟石灰
(2)实验完毕后,设计简单实验检验D试管收集到的物质(简述操作过程、现象和结论) 。
(3)写出C中发生反应的化学方程式 。
(二)乙方案
(4)A为浓氨水,B为生石灰,简述实验原理: 。E装置里盛装的药品是 。
(5)能证明氨气具有还原性的实验现象 。(任写两条)
(6)铜有+2价、+1价、0价,根据氧化还原反应原理,D玻璃管里还原产物除铜外,还可能有 ,假设有铜以外的还原产物生成,写出D中发生反应的化学方程式: 。
高三化学填空题中等难度题查看答案及解析
某研究性学习小组设计两套实验方案制备氨气并探究其还原性(部分夹持装置已省略)。
甲方案:如图所示。

乙方案:如图所示。
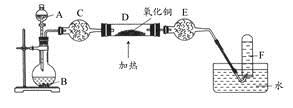
根据方案回答下列问题:
(一)甲方案
(1)B装置盛装碱石灰,A装置中药品可以是 。
a.氯化铵固体和烧碱 b.碳酸氢铵固体
c.氯化铵固体 d.硫酸铵和熟石灰
(2)实验完毕后,设计简单实验检验D试管收集到的物质(简述操作过程、现象和结论) 。
(3)写出C中发生反应的化学方程式 。
(二)乙方案
(4)A为浓氨水,B为生石灰,简述实验原理: 。E装置里盛装的药品是 。
(5)能证明氨气具有还原性的实验现象 。(任写两条)
(6)铜有+2价、+1价、0价,根据氧化还原反应原理,D玻璃管里还原产物除铜外,还可能有 ,假设有铜以外的还原产物生成,写出D中发生反应的化学方程式: 。
高三化学实验题困难题查看答案及解析