-
(11分)(1)现有A、B、C、D、E五种原子序数递增的主族元素,A的原子核中没有中子;B、D元素处于同一周期,D的原子半径较小,B、D的质子数之和为27,质子数之差为5;C的单质跟盐酸反应,生成C3+和氢气;E和D能形成E2D型离子化合物,且E、D两元素的简单离子具有相同电子层结构。
① 写出元素符号:A________,D________,E________。
② B、C的最高价氧化物对应水化物相互反应的离子方程式为:
________。
③ 写出A2D的电离方程式:________,________。
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质。N P AS ;O S Se 分别是VA族、VIA族连续三元素。
①根据元素周期律,预测:酸性强弱 H3AsO4 ________H3PO4。(用“>”或“<”表示)
② 元素S的最高正价和最低负价的代数和为____________,在一定条件下,S与H2反应有一定限度,请判断:在相同条件下Se与H2反应的限度比S与H2反应限度________。(选填“更大”、“更小”或“相同”)
③将SO2气体通入溴水恰好完全反应后,溶液中存在的离子浓度由大到小的顺序是_________________。
高二化学填空题困难题查看答案及解析
-
A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)B元素的原子结构示意图是 ________ ;C元素原子的电子排布图是 ;D元素原子的价电子排布式是 ;
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示) ;(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式 ;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因 。
高二化学填空题极难题查看答案及解析
-
A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)B元素的原子结构示意图是___,D元素原子的价电子排布式是___,C元素原子核外电子的轨道表示式是___。
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是___(用化学式表示)。
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式___,用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因___。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)B元素的原子结构示意图是 ;C元素原子的轨道表示式是 ;D元素原子的价电子排布式是 ;
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示) ;
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学
式 ;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因 。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E是短周期的五种主族元素.A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构.根据上述信息回答下列问题:
(1)B元素的原子结构示意图是 ;C元素原子的轨道表示式是 ;D元素原子的价电子排布式是 ;
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示) ;
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式 ;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因 .
高二化学推断题困难题查看答案及解析
-
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期,B元素含有3个能级,且每个能级所含的电子数相同;DD的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
(1)用元素符号表示B、C、D三种元素的第一电离能由低到高的顺序________________;
(2)F离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点,向F的硫酸盐溶液中通入过量C与A形成的气体N,反应现象为________________,反应的离子方程式为__________、______;
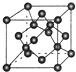
(2)B单质的一种同素异形体的晶胞如图所示,若晶体的密度为ρg/cm3,阿伏加德罗常数的值为NA,则晶体中最近的两个原子之间的距离为________________;
高二化学推断题困难题查看答案及解析
-
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为______________,G的原子结构示意图是___________。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为____________________,所含化学键类型为_____________________________________。向甲中滴加足量水时发生反应的化学方程式是________________________________。
(3)E、F、G形成的简单离子,半径由大到小顺序是____________。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,负极的电极反应式为_______________________________
高二化学简答题中等难度题查看答案及解析
-
(11分)现有A、B、C、D、E、F、G七种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可发生非氧化还原反应
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
在地壳中的含量位居第三
F
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
G
该元素的一种氧化物M可用作油漆颜料,与E的单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)画出元素C的基态原子核外电子排布图: ;G元素位于周期表的 区;
B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)FD2中F原子的杂化类型为 ;分子空间构型为 ;FD2易溶于水的原因可能是: (填入序号)。①FD2与水极性相同 ②FD2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:
高二化学填空题困难题查看答案及解析
-
(11分)现有A、B、C、D、E、F六种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可发生非氧化还原反应
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
F
该元素的一种氧化物M可用作油漆颜料,与某单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)画出元素C的基态价电子排布图: ;F元素位于周期表的__ 区;B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)ED2中F原子的杂化类型为 ; ED2易溶于水的原因可能是: (填入序号)。
①ED2与水极性相同
②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为: 。
高二化学填空题困难题查看答案及解析
-
现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可生成盐
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
F
该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
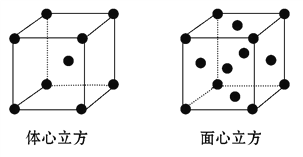
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。
高二化学综合题中等难度题查看答案及解析