-
I.已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是__________________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入__________________。
A.硫酸钾 B.硫酸锰 C.氯化钾 D.水
II. 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
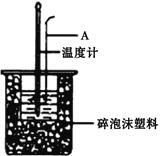
(1)仪器A的名称是__________________,烧杯间填满碎泡沫塑料的作用是__________________。
(2)加入NaOH溶液的正确操作是__________________ (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g·℃)。为了计算中和热,某学生实验记录数据如下:
实验序号
起始温度t1℃
终止温度t2℃
盐酸
氢氧化钠
混合溶液
1
20.0
20.1
23.2
2
20.2
20.4
23.4
3
20.5
20.6
23.6
依据该学生的实验数据计算,该实验测得的中和热△H=__________________(结果保留一位小数)。
(4)实验中若改用50 mL 0.50 mol/L的盐酸与40 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量__________________(填“相等”“不相等”),若实验操作均正确,则所求中和热__________________(填“相等”“不相等”)。
高二化学实验题中等难度题查看答案及解析
-
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化学小组根据上述反应原理进行下列实验:
Ⅰ.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会________(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为________。
(4)计算H2C2O4溶液的物质的量浓度为________mol·L-1。
Ⅱ.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号
体积V/mL
0.1mol·L-1KMnO4溶液
0.1mol·L-1H2C2 O4溶液
0.1mol·L-1H2SO4溶液
H2O
①
2.0
5.0
6.0
7.0
②
2.0
8.0
6.0
V1
③
2.0
V2
6.0
2.0
请回答:
(5)表中V1=________,V2=________。
(6)实验中需要测量的数据是________。
(7)实验中________(填“能”或“不能”)用0.2mol·L-1盐酸代替0.1mol·L-1H2SO4溶液,理由是________。
高二化学实验题困难题查看答案及解析
-
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化学小组根据上述反应原理进行下列实验:
Ⅰ.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会________(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为________。
(4)计算H2C2O4溶液的物质的量浓度为________mol·L-1。
Ⅱ.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号
体积V/mL
0.1mol·L-1KMnO4溶液
0.1mol·L-1H2C2 O4溶液
0.1mol·L-1H2SO4溶液
H2O
①
2.0
5.0
6.0
7.0
②
2.0
8.0
6.0
V1
③
2.0
V2
6.0
2.0
请回答:
(5)表中V1=________,V2=________。
(6)实验中需要测量的数据是________。
(7)实验中________(填“能”或“不能”)用0.2mol·L-1盐酸代替0.1mol·L-1H2SO4溶液,理由是________。
高二化学实验题困难题查看答案及解析
-
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化学小组根据上述反应原理进行下列实验:
Ⅰ.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会________(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为________。
(4)计算H2C2O4溶液的物质的量浓度为________mol·L-1。
Ⅱ.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号
体积V/mL
0.1mol·L-1KMnO4溶液
0.1mol·L-1H2C2 O4溶液
0.1mol·L-1H2SO4溶液
H2O
①
2.0
5.0
6.0
7.0
②
2.0
8.0
6.0
V1
③
2.0
V2
6.0
2.0
请回答:
(5)表中V1=________,V2=________。
(6)实验中需要测量的数据是________。
(7)实验中________(填“能”或“不能”)用0.2mol·L-1盐酸代替0.1mol·L-1H2SO4溶液,理由是________。
高二化学实验题困难题查看答案及解析
-
17.⑴(9分)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10 ,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①请写出方框内物质的化学式: 。
②针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是 的影响。
③若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是 。
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰
高二化学填空题中等难度题查看答案及解析
-
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组根据上述反应原理进行下列实验:
I.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol/L KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在_____(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会_____(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为_____。
(4)计算H2C2O4溶液的物质的量浓度为_____mol/L。
II.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号
体积V/mL
0.1mol•L﹣1KMnO4溶液
0.11mol•L﹣1H2C2O4溶液
0.11mol•L﹣1H2SO4溶液
H2O
①
2.0
5.0
6.0
7.0
②
2.0
8.0
6.0
V1
③
2.0
V2
6.0
2.0
请回答:
(5)表中v1=_____,V2=_____。
(6)实验中需要测量的数据是_____。
(7)实验中_____(填“能”或“不能”)用0.2mol/L盐酸代替0.1mol/LH2SO4溶液,理由是_____。
高二化学实验题中等难度题查看答案及解析
-
已知草酸晶体(H2C2O4·X H2O)可溶于水,并可与酸性高锰酸钾溶液完全反 应:2KMnO4+5H2C2O4+ 3H2SO4==K2SO4+2MnSO4+10CO2↑+8H2O。 现用氧化还原滴定法测定草酸晶体的结晶水分子数 X,步骤如下:
①用分析天平称取草酸晶体 1.260 g,将其配制成 100.00 mL 待测草酸溶液
②用移液管移取 25.00 mL 待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为 0.1000 mol/L 的 KMnO4 标准溶液进行滴定,三次结果如下:
第一次滴定
第二次滴定
第三次滴定
待测溶液体积(mL)
25.00
25.00
25.00
标准溶液体积(mL)
9.99
10.01
10.00
已知 H2C2O4 的相对分子质量为 90,请回答下列问题:
(1)滴定时,KMnO4 标准溶液应该装在_____(填“酸式”或“碱式”)滴定管中。
(2)在整个实验过程中,不需要的仪器或用品是_____(填序号)。
①100 mL 容量瓶②烧杯③滴定管夹④漏斗⑤玻璃棒⑥托盘天平
(3)到达滴定终点的标志是_________。
(4)根据上述数据计算 X=__________。
(5)误差分析(填偏高、偏低或无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则 X 值_____;
②若 KMnO4 标准溶液浓度偏低,则 X 值_____;
高二化学实验题中等难度题查看答案及解析
-
已知草酸晶体(H2C2O4·xH2O)可溶于水,并可与酸性高锰酸钾溶液完全反应:
2KMnO4+5H2C2O4+3H2SO4==K2SO4+2MnSO4+8H2O+10CO
2↑
现用氧化还原滴定法测定草酸晶体的结晶水分子数X,步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100.00mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000 mol·L-1的KMnO4标准溶液进行滴定,三次结果如下:
第一次滴定
第二次滴定
第三次滴定
待测溶液体积(mL)
25.00
25.00
25.00
标准溶液体积(mL)
9.99
10.01
10.00
已知H2C2O4的相对分子质量
为90,请回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在 (填“酸式”或“碱式”)滴定管中。
(2)在整个实验过程中,不需要的仪器或用品是 (填
序号)。
①100mL容量瓶 ②烧杯 ③滴定管夹 ④漏斗 ⑤玻璃棒 ⑥托盘天平
(3)到达滴定终点的标志是 。
(4)根据上述数据计算x= 。
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则x值 ;
②若滴定管水洗后直接加入KMnO4标准溶液,则X值 。
高二化学实验题困难题查看答案及解析
-
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理] 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
[实验内容及记录]
实验
编号
室温下,试管中所加试剂及其用量/mL
室温下溶液颜色褪至无色所需时间/min
0.6 mol/L
H2C2O4溶液
H2O
0.2 mol/L
KMnO4溶液
3 mol/L
稀硫酸
1
3.0
2.0
3.0
2.0
4.0
2
3.0
3.0
2.0
2.0
5.2
3
3.0
4.0
1.0
2.0
6.4
请回答:
(1)根据上表中的实验数据,可以得到的结论是___________________________。
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=_____________________________。
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设。并继续进行实验探究。
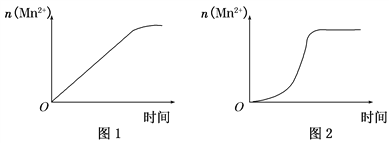
①该小组同学提出的假设是____________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验
编号
室温下,试管中所加试剂及其用量/mL
再向试管中加入少量固体
室温下溶液颜色褪至无色所需时间/min
0.6 mol/L
H2C2O4溶液
H2O
0.2 mol/L KMnO4溶液
3 mol/L稀硫酸
4
3.0
2.0
3.0
2.0
________
t
③若该小组同学提出的假设成立,应观察到的现象是_________________________。
高二化学实验题中等难度题查看答案及解析
-
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(原理)2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(实验内容及记录)
实验编号
室温下,试管中所加试剂及其用量/mL
室温下溶液颜色褪至无色所需时间/min
0.6mol·L-1 H2C2O4溶液
H2O
0.2mol·L-1 KMnO4溶液
3mol·L-1稀硫酸
1
3.0
2.0
3.0
2.0
4.0
2
3.0
3.0
2.0
2.0
5.2
3
3.0
4.0
1.0
2.0
6. 4
请回答:
(1)根据上表中的实验数据,可以得到的结论是____________________;
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)= __________;
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
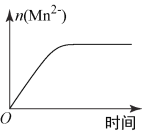
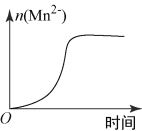
图1
图2
①该小组同学提出的假设是__________________________________________;
②请你帮助该小组同学完成实验方案,并填完表中空白。
实验编号
室温下,试管中所加试剂及其用量/mL
室温下溶液颜色褪至无色所需时间/min
0.6mol·L-1 H2C2O4溶液
H2O
0.2mol·L-1 KMnO4溶液
3mol·L-1稀硫酸
向试管中加入少量固体
4
3.0
2.0
3.0
2.0
_____________
t
③若该小组同学提出的假设成立,应观察到的现象是______________________。
高二化学实验题中等难度题查看答案及解析