-
现实验室需要450mL 0.5mol/L的NaOH溶液和500mL 0.5mol/L的H2SO4溶液,试回答下列问题:
(1)选择仪器:配制NaOH溶液时所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、__________、__________等。
(2)在配制NaOH溶液时:
①计算:根据计算用托盘天平称取NaOH固体的质量为___________g。
②称量:称量过程中NaOH固体应放于小烧杯中并放在天平的_________(填“左盘”或“右盘”)
③溶解。该步实验中需要使用玻璃棒,作用是_______________________。
④转移、洗涤。a.若NaOH溶解后立即转移入容量瓶,则浓度会_________;(填“偏大”“偏小”或“无影响”,下同)
b.若转移完溶液后未洗涤玻璃棒和烧杯,则浓度会_________;
c.若容量瓶中原来有少量蒸馏水,则浓度会__________。
⑤定容、摇匀。将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下_________处,改用胶头滴管滴加蒸馏水至液面与刻度线相切。盖好瓶塞,反复上下颠倒,摇匀。
(3)在配制H2SO4溶液时:某同学欲用98%的浓硫酸(密度ρ=1.84g/cm3)配制500mL0.5mol/L的稀H2SO4溶液。请回答:
①用量筒量取所需浓硫酸的体积为_______mL。
②如果实验室有10mL、20mL、50mL量筒,应选用_______mL量筒量取。
③将量取的浓硫酸沿内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌,目的是_______________________。
④用量筒量取浓硫酸时,仰视读数,则最终配得稀硫酸的浓度会_________。(填“偏大”“偏小”或“无影响”)
高一化学实验题中等难度题查看答案及解析
-
现实验室需要450 mL 0.5 mol/L的NaOH溶液和500 mL 0.2 mol/L的H2SO4溶液。
请回答下列问题:
Ⅰ.配制NaOH溶液
1.根据计算,用托盘天平称取NaOH固体的质量应为_____g。
A.0.9 B.9.0 C.10 D.10.0
Ⅱ.配制稀H2SO4
某同学欲用质量分数为98%的浓硫酸(密度ρ=1.84 g/cm3)配制所需的稀H2SO4。可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④量筒;⑤500 mL容量瓶;⑥圆底烧瓶
2.以上仪器中不需要的是
A.① B.② C.③ D.⑥
3.用量筒量取所需浓硫酸的体积应为_______mL。
A.5.4 B.5.5 C.18.4 D.27.2
4.如果实验室有10 mL、20 mL、50 mL的量筒,应选用_______mL量筒量取。
A.10 B.20 C.50 D.以上都可以
5.下列操作会使所配制的溶液浓度偏高的是
A.容量瓶中原来有少量蒸馏水未作处理
B.定容时仰视容量瓶刻度线
C.用量筒量取浓硫酸时仰视读数
D.定容时,不慎加水超过刻度线,又用滴管将多出部分吸出
高一化学实验题中等难度题查看答案及解析
-
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称).
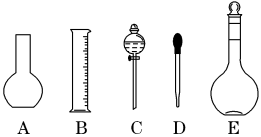
(2)根据计算用托盘天平称取NaOH的质量为 g.
(3)配制时,其正确的操作顺序是 。(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为: mL(计算结果保留一位小数).如果实验室有15 mL、20 mL、50 mL量筒,应选用 mL的量筒最好。
高一化学实验题中等难度题查看答案及解析
-
实验室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是______(填仪器名称).
(2)根据计算用托盘天平称取NaOH的质量为______ g.
(3)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为______ mL(计算结果保留一位小数).如果实验室有15mL、20mL、50mL量筒,应选用______ mL的量筒最好.配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______.
(4)取用任意体积的所配0.5mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是(填字母)
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液中SO42-的数目 D.溶液的密度
(5)将所配制的稀H2SO4进行测定,发现浓度大于0.5mol/L.请你分析下列哪些操作会引起所配浓度偏大(填写字母)______
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容;
D.往容量瓶转移时,有少量液体溅出
E.用量筒量取浓硫酸时,仰视量筒的刻度
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.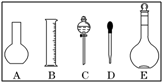
高一化学解答题中等难度题查看答案及解析
-
(16分)实验室需要0.1 mol·L-1NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
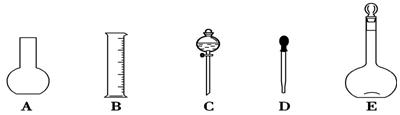
(2)下列是通过使用质量分数为98%(密度为1.84 g·cm-3)的浓硫酸来配制500 mL 0.5 mol·L-1硫酸溶液的操作步骤,其正确的操作顺序是 (填序号)。
A.把容量瓶活塞塞上,反复摇匀后,装贴标签以保存
B.加入蒸馏水进容量瓶中进行定容,待水面离刻度线只有1~2厘米时,采用胶头滴管滴加蒸馏水使其凹液面正好与刻度线相切
C.在烧杯中注入适量的蒸馏水,用量筒准确量取98%的浓硫酸13.3ml慢慢注入烧杯中,并不停地搅拌使之稀释均匀
D.通过计算需要量取98%(密度为1.84 g·cm-3)的浓硫酸13.3ml
E.待烧杯中稀释的硫酸溶液冷却至室温后,通过玻璃棒引流转移至500ml的容量瓶中
F.把玻璃棒和烧杯分别都洗涤2~3次,洗涤液也转移至容量瓶
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1 (填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol·L-1;溶解NaOH后在未降至室温时,立即将NaOH溶液转移至容量瓶定容,则所得溶液浓度_______ 0.1 mol·L-1。
(4)在容量瓶的使用方法中,下列操作不正确的是 (填写标号).
A.使用容量瓶前检查它是否漏水.
B.容量瓶用蒸馏水洗净后,不需要进行烘干就可以直接使用.
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线.
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线.
高一化学实验题简单题查看答案及解析
-
实验室需要0.2 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:

(l)如图所示的仪器中配制溶液一定不需要的是 ___(填字母序号),配制上述溶液还需用到的玻璃仪器是____填仪器名称)。
(2)在配制NaOH溶液时:
①根据计算,用托盘天平称取NaOH固体____g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则配置的溶液浓度_____填“偏高”、“偏低”或“无影响”)。
(3)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为____mL(计算结果保留一位小数);
②如果实验室有15 mL、20 mL、50 mL量筒,应选用 ___mL量筒最好。
高一化学实验题中等难度题查看答案及解析
-
某化学实验室需要0.2 mol·L-1的NaOH溶液450 mL和0.5 mol·L-1的硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是__(填序号),配制上述溶液还需用到的玻璃仪器是__________(填仪器名称)。

(2)容量瓶是配制溶液的主要仪器,容量瓶上标有以下六项中的 ____(填写序号)。
①温度 ②浓度 ③容量 ④压强 ⑤酸式或碱式 ⑥刻度线
(3)配制时,其正确的操作顺序是____(用字母表示,每个字母只能用一次)。
A.用30 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算好的氢氧化钠固体于烧杯中,再加入少量水(约50 mL),用玻璃棒慢慢搅动,使其充分溶解,冷却到室温
C.将容量瓶盖紧,摇匀
D.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(4)根据计算可知,该实验需称取NaOH固体的质量为_______________g。
(5)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________________。
(6)将所配制的稀H2SO4进行测定,发现实际浓度小于0.5 mol·L-1。请你分析下列哪些操作会引起所配浓度偏小_________________(填字母)。
A.用量筒量取浓硫酸时,仰视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视容量瓶刻度线
E.烧杯未进行洗涤
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
高一化学填空题中等难度题查看答案及解析
-
实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____(填序号),配制上述溶液还需用到的玻璃仪器是_____(填仪器名称)。
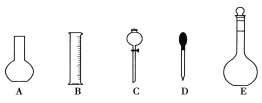
(2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度_____0. 1 mol·L-1(填“大于”、“等于”或“小于”,下同)。
(4)由计算知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是:________________。
高一化学实验题中等难度题查看答案及解析
-
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
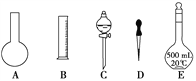
①如图所示的仪器中,配制溶液肯定不需要的是(填序号) _________________________,配制上述溶液还需用到的玻璃仪器有________________________________(填仪器名称)。
②配制0.1 mol/L NaOH溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次)___________。
A.将容量瓶盖紧,振荡,摇匀
B.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
C.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
D.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
E.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
③配制0.1 mol/L NaOH溶液时,在实验中其他操作均正确,若定容时仰视容量瓶刻度线,则所配溶液浓度_____________________0.1 mol/L(填“大于”、“等于”或“小于”)。
④配制0.5 mol/L硫酸溶液500 mL时,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_________________________mL(计算结果保留一位小数)。
高一化学实验题中等难度题查看答案及解析
-
实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
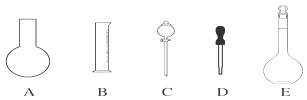
(1)如图所示的仪器中配制溶液肯定不需要的是___________(填序号),配制上述溶液还需用到的玻璃仪器是_____ (填仪器名称)。
(2)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为________g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度_____(填“>”、“<”或“=”)0.1 mol/L;
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度________(填“>”、“<”或“=”)0.1 mol·L-1。
(3)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________(计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL量筒,应选用________mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是__________________。
高一化学实验题中等难度题查看答案及解析