-
氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高.
(1)若电解质溶液为KOH溶液,其正极反应为 ,负极反应为 ﹣ ;
(2)若电解质溶液为硫酸,其正极反应为 ,负极反应为 ;若反应过程中转移了2mol电子,可产生水的质量为 g.
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3mol•L﹣1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体.此时氢氧燃料电池外电路中转移电子数为 ,消耗H2的质量为 g.
高二化学填空题困难题查看答案及解析
-
燃料电池是将乙醇通入负极,O2通入正极而发生电池反应的,其能量转换率高.
(1)若电解质溶液为KOH,其正极反应为 ,负极反应为 ;
(2)若电解质溶液为硫酸,其正极反应为 ,负极反应为 ;
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3mol•L﹣1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体.此时燃料电池中消耗H2的质量是 ,O2的质量是 .
高二化学填空题困难题查看答案及解析
-
氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高.
(1)若电解质溶液为KOH溶液,其正极反应为______,负极反应为______;
(2)若电解质溶液为硫酸,其正极反应为______,负极反应为______;若反应过程中转移了2mol电子,可产生水的质量为______ g.
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3mol•L-1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体.此时氢氧燃料电池外电路中转移电子数为______,消耗H2的质量为______g.高二化学解答题中等难度题查看答案及解析
-
(11分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH溶液,其正极反应为________,负极反应为________;
(2)若电解质溶液为硫酸,其正极反应为________,负极反应为________;
若反应过程中转移了2mol电子,可产生水的质量为________ g。
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)
=0.3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体。此时氢氧燃料电池外电路中转移电子数为________,消耗H2的质量为________。
高二化学填空题简单题查看答案及解析
-
氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,其正极反应为____________,负极反应为_____________。
(2)若电解质溶液为硫酸,其正极反应为_________,负极反应为_______;若在常温下转移2mol电子,可产生水质量为_________g。
高二化学填空题中等难度题查看答案及解析
-
科学家预言,燃料电池将是21世纪获得电能的重要途径。
(1)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
①若电解质溶液为KOH,其负极反应为______________________________,电池总反应为 _______________________________。
②若电解质溶液为硫酸,其正极反应为_____________________________,负极反应为________________________________;
(2)近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:
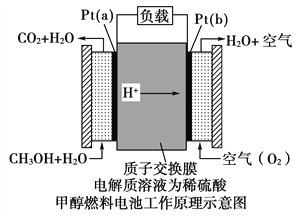
请回答下列问题:
① Pt(a)电极是 _____ 极,电极反应式为_______________________________;
② Pt(b)电极发生________反应(填“氧化”或“还原”)。
③该电池的总反应方程式为_____________________________________________。
④如果该电池工作时电路中通过3 mol电子,则消耗掉的CH3OH有________mol。
高二化学填空题中等难度题查看答案及解析
-
(12分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,其正极反应为____________________________,
负极反应为__________________________________________;
(2)若电解质溶液为硫酸,其正极反应为______________________,负极反应为_________________;若在常温下转移2mol电子,可产生水质量为_________g。
(3)还有一个很大的优点是________。
高二化学填空题简单题查看答案及解析
-
(10分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,其正极反应为____________________________,
负极反应为__________________________________________;
(2)若电解质溶液为硫酸,其正极反应为______________________,负极反应为_________________;若在常温下转移2mol电子,可产生水质量为_________g。
(3)若用氢氧燃料电池做电源电解由NaCl和CuSO4组成的混合溶液,其中
c(Na+)=3c(Cu2+)=0.3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体。计算(写出计算过程)
此时氢氧燃料电池中消耗H2和O2的质量各是多少?(保留2位小数)
高二化学计算题简单题查看答案及解析
-
(12分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,其正极反应为____________________________,
负极反应为__________________________________________。
(2)若电解质溶液为硫酸,其正极反应为______________________,
负极反应为___ ______________。
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体。计算:
①电解池阳极生成氯气的物质的量是 mol。
②氢氧燃料电池中转移的电子数目是 个
消耗H2的质量是 g。(写出计算过程)(保留2位小数)
高二化学填空题中等难度题查看答案及解析
-
(每空2分,共10分)
氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH溶液,其
正极反应为____________________________________________,
负极反应为__________________________________________;
(2)若电解质溶液为H2SO4,其正极反应为________________,负极反应为____________________;若反应过程中转移了2mol电子,可产生水的质量为_________________g。
高二化学填空题简单题查看答案及解析