-
(14分)某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们进行了下列探究:
【猜想】(1)甲同学认为可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液,而不能用澄清石灰水鉴别。
(2)乙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别。
依据是。
(3)丙同学认为可用盐酸鉴别Na2CO3和NaHCO3固体。
【实验探究】
(1)甲同学:① 将CaCl2溶液加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现盛有Na2CO3的试管产生了白色沉淀;②将澄清石灰水加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现两支试管中也都产生了白色沉淀。
此实验结果与猜想相同。
(2)乙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图1):
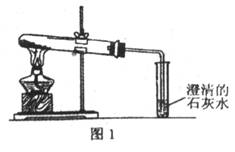
①加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO3时,乙同学观察到实验现象与①不同,证实了自己的猜想是合理的。
(3)丙同学在两支分别盛有少量Na2CO3、NaHCO3固体的试管中,各加入2 mL
2 mol/L的盐酸,观察到两支试管中均产生了大量气体,实验结果与猜想不一致,即得出不能用盐酸鉴别Na2CO3和NaHCO3。
【问题讨论】
(1)甲同学的两个实验中,大家对CaCl2与Na2CO3溶液的反应比较熟悉,该反应的离子方程式为________;
(2)乙同学在加热Na2CO3固体时,开始产生少量气泡的原因是________;在加热NaHCO3固体时,乙同学观察到的实验现象是________。
(3)丁同学认为丙同学的结论不对。丁同学认为对实验方案做一些改进,可用于鉴别碳酸钠与碳酸氢钠。他的改进方法是:称取各2.1 g 两种固体,放入两个容积一样的气球中,在两只锥形瓶中各加入约25 mL 2 mol/L 的盐酸,分别将气球套在锥形瓶瓶口上,同时将气球中的固体同时倒入锥形瓶中,气球的膨胀比较________(填快或慢)的或最后气球比较________(填大或小)的是碳酸氢钠。
【拓展应用】
(1)要除去Na2CO3溶液中混有的少量NaHCO3,可加入适量的________溶液。
(2)要测定Na2CO3与NaHCO3固体混合物中Na2CO3的质量分数,可采用的方案有多种,请简述其中一种方案(写出简要步骤及要测定的数据,不要求写出如何用数据求出结果):
________
________。
-
某化学实验小组拟用50mLNaOH溶液吸收CO2气体(用大理石和稀盐酸反应来制取CO2),以制备纯净的Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,他们设计了如下实验过程:
a.取25 mL NaOH溶液,向其中通入过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸此溶液1~2 min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应。
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式:____________________________________、_____________________________________
(2)煮沸溶液的目的是 。
此方案第一步的实验装置如右图所示:
(3)加入反应物前,如何检查整个装置的气密性_________________________________。
(4)装置B中盛放的试剂是____________,作用是__________________________________。
(5)在实验室制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
①CH2=CH2 ②H2S ③CH4 ④CH≡CH ⑤H2
(6)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
| 尾 气 吸 收 装 置 | 
| 
|
| 处理气体 | | |
(7)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g / mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_________________。
-
有关碳酸氢钠和碳酸钠的性质,以下叙述错误的是( )
A.等质量的Na2CO3、NaHCO3与足量的盐酸反应,在相同条件下Na2CO3产生CO2的体积大
B.等物质的量的Na2CO3和NaHCO3与同浓度的足量盐酸反应,Na2CO3所消耗盐酸的体积是NaHCO3的两倍
C.将石灰水加入Na2CO3和NaHCO3溶液中,都产生白色沉淀
D.同物质的量浓度的两种溶液,碳酸钠溶液的pH大于碳酸氢钠溶液
-
某学习小组设计有关Na2CO3和NaHCO3的探究实验,其中设计方案明显错误的是
A.可用加热的方法除去Na2CO3固体中混有NaHCO3
B.可向NaHCO3溶液中通入过量的CO2气体除去其中混有的Na2CO3
C.可用澄清石灰水鉴别NaHCO3和Na2CO3两种溶液
D.分别向Na2CO3溶液、NaHCO3溶液中滴加过量的稀盐酸,均有气泡产生
-
(12分)(1)某化学小组的同学在学习了NaHCO3和Na2CO3的有关知识后,进行如下实验:在两支试管中分别加入3mL4 mol·L-1稀盐酸,将两个各装有0.3g NaHCO3或 Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:
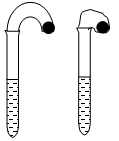
① 试管中(填产生沉淀或气体及反应速率等相关现象)____________________。
② 盛______________的试管中气球变得更大,大小气球体积之比约为(填简单整数比)____________;
③ 甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3
的试管温度有升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。类似如中和热,甲同学写出了下列热化学方程式:
HCO3-(aq)+H+(aq)=H2O(l)+CO2(g); △H>0
CO32-(aq)+2H+(aq)=H2O(l)+CO2(g); △H<0
甲下结论的方法是否正确____________(填“正确”或“不正确”)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 35mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 3.2g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL 稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL 稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1 mL+10ml水 | 20℃ | 24.2℃ |
| ⑤ | 35mL 稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL 稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
请你帮助填写相关内容:
①该研究报告的题目是《_____________________________________》;
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为_________和__________;通过上述实验可得出五条结论(用“吸热”或“放热”填写):
a:NaHCO3的溶解是_______过程;
b:Na2CO3的溶解是_______过程;
c:NaHCO3的饱和溶液和盐酸的反应是____________反应;
d:Na2CO3的饱和溶液和盐酸的反应是____________反应;
e:NaHCO3固体与稀盐酸反应的反应热是______(填a、b、c、d中的字母)的热效应之和。
-
下列关于Na2CO3和NaHCO3的性质的比较中,不正确的是
A.热稳定性:Na2CO3>NaHCO3
B.常温时的溶解度:NaHCO3<Na2CO3
C.与相同浓度稀盐酸反应的剧烈程度:Na2CO3>NaHCO3
D.等质量的固体与足量盐酸反应放出CO2的质量NaHCO3>Na2CO3
-
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的实验,他们提出下列实验方案。
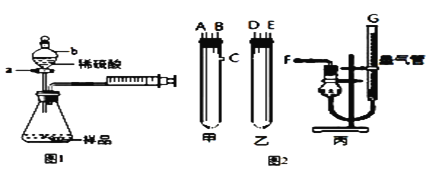
(1)甲同学用图1装置,把m g的混合物样品与足量稀硫酸反应后,测定产生的CO2气体的体积,检查该装置的气密性时,某同学将注射器活塞拉出一定距离,___,说明该装置的气密性好;当锥形瓶内不再产生气泡时立即读数,测定结果 ___(填 “偏大”、“偏小”、“无影响”)。
(2)乙同学用图2装置,Na2CO3、NaCl的固体混合物样品和稀硫酸应分别置于甲和乙中,导管连接方式如下:A连接____,B连接____,C连接_____(填写各接口的字母编号)。
-
下列有关NaHCO3与Na2CO3的说法中,正确的是
A、分别与相同物质的量浓度的盐酸反应,产生CO2的速率:Na2CO3<NaHCO3
B、分别加热两种样品,没有残留物质的是NaHCO3
C、分别配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3
D、二者在一定条件下不能相互转化
-
有关Na2CO3 和NaHCO3的下列叙述中错误的是( )
A、相同质量的NaHCO3和Na2CO3与足量盐酸反应,Na2CO3产生的CO2少
B、将石灰水加入NaHCO3溶液中不产生沉淀,加入Na2CO3 溶液中产生白色沉淀
C、向Na2CO3饱和溶液中通入足量CO2气体会出现浑浊
D、Na2CO3中含少量NaHCO3,可用加热的方法除去
-
下列关于Na2CO3、NaHCO3说法正确的是
A. 受热时Na2CO3较NaHCO3更不稳定,更易分解产生CO2
B. 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多
C. 常温下相同物质的量浓度的Na2CO3、NaHCO3溶液,前者碱性更强
D. 向Na2CO3、NaHCO3溶液中分别滴加澄清石灰水,前者产生白色沉淀,后者无沉淀



