-
(1)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是 (填化学式)。

(2)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(3)氧化亚铜为半导体材料,在其立方晶胞内部有四个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______ 个铜原子。
(4)很多金属盐都可以发生焰色反应,其原因是
(5) 已知HF与F-通过氢键结合成HF2-.判断HF2-和HF2-微粒间能否形成氢键,并说明理由.
-
如图中曲线表示原子序数在前20号元素的原子序数(按递增顺序连接排列)和单质沸点的关系。其中A点表示的元素是( )

A. Cl B. Si C. F D. S
-
元素的性质随着原子序数的递增出现周期性变化的根本原因是
A.原子半径的周期性变化 B.化合价呈周期性变化
C.单质熔沸点呈周期性变化 D.元素原子核外电子排布呈周期性的变化
-
(4分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)元素b的基态原子电子排布式为 。
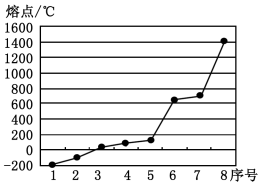
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
-
下图是部分短周期元素的常见化合价与原子序数的关系:

(1)元素A在周期表中的位置为________________________。
(2)用电子式表示D2G的形式过程:_________________________________________________,其所含化学键类型为__________。
(3)C2-、D+、G2-半径由大到小的顺序是________(填离子符号)。
(4)C、G的简单氢化物中,沸点较低的是________(填化学式),原因是________________。两种气态氢化物的稳定性C________G(填“>”或“<”)。
(5)C与D形成的具有强氧化性、可以做供氧剂的化合物的电子式为_________________。
-
周期表中同族元素单质及其化合物在许多性质上都存在着递变规律,随着原子序数的递增,下列有关说法正确的是
A.IA族,单质的熔点逐渐降低 B.ⅥA族,对气态氢化物还原性逐渐增强
C.VA族氢化物的沸点逐渐升高 D.ⅣA族最高氧化物对应水化物的酸性逐渐增强
-
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如下图转化关系,回答下列问题:

(1)若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的非极性气态分子,Y原子的电子排布图为_________,乙的电子式为________;
(2)若X为非金属,甲是由两种短周期元素的原子构成的A2B型极性分子,且是常见的溶剂,甲的电子式___,乙的化学式为_____;
(3)若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为:___。
-
(每空2分,共12分)有X、Y、Z三种单质和甲、乙、丙三种常见的化合物,它们有如下图及叙述所示的关系:

(1)X、Y、Z都是短周期元素的单质,X元素原子的最外层电子数是其次外层电子数的2倍;Y元素有两种常见单质,二者质量相等时其物质的量之比为3 :2;Z元素原子的次外层电子数是其最外层电子数的4倍。则:
①写出化合物甲的电子式___________________;
②写出Z与甲反应的化学方程式_______________________________________________;
(2)X、Y、Z都是非金属单质,X是原子晶体,Y、Z都是分子晶体,X、Y都能与强碱溶液反应;乙的水溶液是工业三酸之一,也是实验室常用试剂。则:
①写出X与NaOH溶液反应的离子方程式________________________________________;
②在①所得溶液中加入乙的溶液,观察到的现象___________________________________
___________________________________________;
(3).X、Z是常见金属,Z与甲的反应只有在高温下才能进行,甲是一种具有磁性的化合物,乙在工业上常用于制取Z单质。则:
①写出乙与NaOH溶液反应的化学方程式______________________________;
②将等物质的量的X和Z分别与足量的稀硫酸反应,当两种金属完全溶解后,得到气体的质量之比是____________________________。
-
有a、b、c、d四种原子序数依次增大的常见短周期元素,a、c结合构成化合物x;b、c结合构成化合物y;c、d结合构成化合物z。元素组成的单质(仍用a、b、c、d表示)和组成的化合物之间的反应关系如下(未配平):
①x+z→c↑+n ②y+z→c↑+m ③n+y→m+x ④d+x→n+a↑
(1)上述反应中,有充分理由说明该反应一定属于氧化还原反应的是
(填反应编号)。
(2)组成化合物n的元素为 (填字母),判断理由为 。
(3)根据题意写出:z的电子式为 ,y的结构式为 。
(4)根据题意写出:反应①的化学方程式 。
-
(9分)下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物。
I.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)

(1)若E为氧化物,则A与水反应的化学方程式为________,①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为________
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为________
(2)若E为单质气体,D为白色沉淀,A的化学式可能是________




