-
【化学——物质结构与性质】
氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是________。前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________________________
(3)N2F2分子中N原子的杂化方式是___________________,l mol N2F2含有______mol 键。
键。
(4)NF3的键角______NH3的键角(填“<”“>”或“=”),原因是__________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。l mol NH4BF4_________mol配位键。
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑

①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质。写出两种与N3-互为等电子体的分子或离子____________。
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为_____,Na2O晶体的密度为_____g·cm-3(只要求列算式,不必计算出结果)
-
氯、氧、碳、铁是与人类生产生活息息相关的化学元素.
(1)基态铁原子的价电子排布式为________.
(2)COCl2俗称光气,分子中C原子采取________杂化成键,根据原子轨道重叠方式的不同来看.碳原子与每个氧原子之间形成共价键的类型和数目为________,C、0、Cl三种元素的电负性由大到小的顺序为________(用元素符号表示).
(3)甲烷和四氯化碳具有相似的空间结构.但常温下甲烷是气体,四氯化碳是液体,其原因是________.
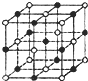
(4)Fexy的晶胞结构如图所示(黑色球代表铁原子,白色球代表氧原子),与一个铁原子距离最近且相等的氧原子构成的几何形状为________.每个氧原子周围与之距离最近的氧原子个数为________.
-
氮及其化合物与人类生产、生活息息相关.回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是__________,前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________。
(3)N2F2分子中N原子的杂化方式是__________,l mol N2F2含有__________molσ键.
(4)NF3的键角__________NH3的键角(填“<”“>”或“=”),原因是__________.
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4__________mol配位键.
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑
①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子__________.
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为__________,Na2O晶体的密度为__________g•cm-3(只要求列算式,不必计算出结果)。

-
【化学选修3:物质结构与性质】Ⅰ.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是__________,N2F2分子中N原子的杂化方式是_____________,1mol N2F2含有___________个σ键.
(2)高温陶瓷材料Si3N4晶体中键角N-Si-N___Si-N-Si(填“>”“<”或“=”),原因是__________;
II.金属元素在现代工业中也占据极其重要的地位,钛也被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大,是宇航、航海、化工设备等的理想材料。
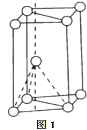
(4)基态钛原子核外共有________种运动状态不相同的电子.金属钛晶胞如下图1所示,为_______堆积(填堆积方式).

(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2.化合物乙的沸点明显高于化合物甲,主要原因是_____________;化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为_____________;
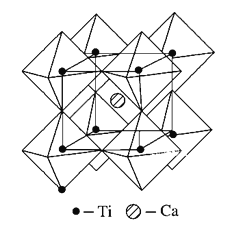
(6)钙钛矿晶体的结构如图3所示.假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被________个氧离子包围。
-
【化学—选修3:物质结构与性质】
I.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是________,N2F2分子中N原子的杂化方式是____________,1mol N2F2含有______个σ键。
(2)高温陶瓷材料Si3N4晶体中键角N—Si—N________Si—N—Si(填“>”“<”或“=”),原因是_________。
II.金属元素在现代工业中也占据极其重要的地位,钛被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大特点,是理想化工设备材料。
(3)基态钛原子核外共有________种运动状态不相同的电子。金属钛晶胞如下图1所示,为_______
堆积(填堆积方式)。
4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是_______。化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为__________。
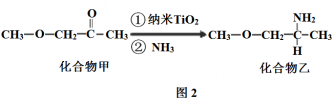

(5)钙钛矿晶体的结构如图3所示。假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被__________个氧离子包围。
-
碳、氧、氯、铁是与人类生产、生活息息相关的化学元素.
(1)基态铁原子的核外电子排布式为______.
(2)C、O、Cl三种元素的电负性由大到小的顺序为______(用元素符号表示).COCl2俗称光气,分子中C原子采取______杂化成键,根据原子轨道重叠方式的不同来看,碳原子与每个氧原子之间形成共价键的类型和数目为______.
(3)甲烷和四氯化碳具有相似的空间结构,但常温下甲烷是气体,四氯化碳是液体,其原因是______.
(4)FexOy的晶胞结构如图所示(白色球代表铁原子,黑色球代表氧原子),与一个铁原子距离最近且相等的氧原子构成的几何形状为______,每个氧原子周围与之距离最近的氧原子个数为______.

-
氮及其化合物与人类生产、生活息息相关。 回答下列问题:
(1)前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为____________________________________________________________。
(2)N2F2分子中氮原子的杂化方式是_____________,1molN2F2含有_____________mol σ键。
(3)NH3的键角 _____________H2O的键角(填“<”“ >”或“=”),原因是_____________。
(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1molNH4BF4含有_____________mol配位键。
(5)安全气囊的设计原理为6NaN3+Fe2O3 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。
①等电子体的原理是原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,其具有许多相近的性质。写出两种与N3-互为等电子体的分子或离子_____________;
②Na2O的晶胞结构如下图所示,晶胞边长为566pm,晶胞中氧离子的配位数为_____________,Na2O晶体的密度为_____________g·cm-3(只要求列算式,不必计算出结果)。

-
自然界存在的元素中,金属元素种类更多,非金属元素丰度更大。
Ⅰ.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子的价电子排布图是_____________,N2F2分子中N原子的杂化方式是_______,1 mol N2F2含有________个σ键。
(2)高温陶瓷材料Si3N4晶体中键角N-Si-N____(填“>”、“<”或“=”)Si-N-Si,原因_________。
Ⅱ.金属元素在现代工业中也占据极其重要的地位。其中钛也被称为“未来的钢铁”,具有质轻、抗腐蚀、硬度大,是宇航、航海、化工设备等的理想材料,是一种重要的战略资源,越来越受到各国的重视。
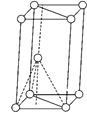
(3)基态钛原子核外共有________种运动状态不相同的电子。金属钛晶胞如下图所示,为________(填堆积方式)堆积。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图。化合物乙的沸点明显高于化合物甲,主要原因是__________。化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为__________________。

(5)钙钛矿晶体的结构如图所示。假设把氧离子看作硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,钙离子位于立方晶胞的体心,一个钙离子被________个氧离子包围。钙钛矿晶体的化学式为________。若氧离子半径为a pm,则钙钛矿晶体中两个钛离子间最短距离为_______pm。
-
I.元素周期表中80%左右的非金属元素在现代技术包括能源、功能材料等领城占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是_____,N2F2分子中N原子的杂化方式是_______,1mol N2F2含有____个δ键。
(2)高温陶瓷材料Si3N4晶体中N-Si-N的键角大于Si-N-Si的键角,原因是_______。
II.金属元素铁、铜及其化合物在日常生产、生活有着广泛的应用。
(1)铁在元素周期表中的位置_________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_____(填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子吸之和为18,则x=________。
(3)N2是CO的一种等电子体,两者相比较沸点较高的为_______(填化学式)。
(4)铜晶体中铜原子的堆积方式如下图甲所示。
①基态铜原子的核外电子排布式为___________。
② 每个铜原子周围距离最近的铜原子数目为___________。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如下图乙所示(黑点代表铜原子)。己知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为_________pm。(只写计算式)。

-
氮及其化合物与人类生产、生活息息相关。
(1)在现代化学中,常利用________上的特征谱线来鉴定元素,称为光谱分析。
(2)基态N原子的价电子占据的能量最高的能级是________,价电子在该能级上的排布遵循的原则是_____________。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。l mol NH4BF4含有______mol配位键。
(4)化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。N4比P4的沸点________,原因为_______________________。

(5)尿素(H2NCONH2)也是一种常用的化肥,其分子中原子的杂化轨道类型有________,σ键和π键数目之比为__________。
(6)Cu3N具有良好的电学和光学性能,其晶胞结构如图。Cu+半径为a pm,N3-半径为b pm,Cu+和N3-都是紧密接触的刚性小球,则N3-的配位数为________,Cu3N 的密度为________ g·cm-3。(阿伏加德罗常数用NA表示)













