-
(本题共11分)氮族元素按原子序数增大,依次为:氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)。请回答:
28.常温常压下,向100mL 1.6mol/L稀氨水中逐滴滴入10mL 4.0mol/L稀硫酸,得到的溶液能使酚酞显红色。请比较所得溶液中NH4+、 NH3﹒H2O、SO42— 三种微粒的物质的量浓度大小关系: 。
29.含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢在热玻璃管中完全分解成氢气和1.50 mg单质砷。则在整个过程中,转移的电子总数为 。
30.铋酸钠(NaBiO3)溶液呈无色。向硫酸锰溶液中依次滴加下列溶液,对应的现象如表所示:
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
请比较实验中所有的氧化剂和氧化产物的氧化性强弱关系(反应过程中的涉及的气体均不参与比较): 。
31.五氟化锑(SbF5)是无色黏稠液体,是很强的具有特殊酸性的酸,而且是超强酸氟锑酸HSbF6(目前酸性最强的酸,比纯硫酸强2×1019倍)的组分之一。SbF5可用于制备一般化学方法很难制备的氧化性极强的F2,其过程如下(均未配平):
①KMnO4 + KF + H2O2 + HF → K2MnF6 +O2 + H2O
②SbCl5 + HF → SbF5 + HCl
③K2MnF6 + SbF5 → KSbF6 + MnF3 + F2↑
反应①中氧化剂和被氧化的元素的物质的量之比为 ____;反应③中SbF5表现的性质为 ______性。
32.能在一定程度上抵消、减轻外加强酸或强碱对溶液酸度的影响,从而保持溶液的pH值相对稳定。这种溶液称为缓冲溶液。例如:人体血液中HCO3—和H2CO3等微粒形成的平衡体系,使得血液pH能稳定在7.4±0.05。某同学取19ml 0.2mol/L的NaH2PO4溶液,81ml 0.2mol/L的Na2HPO4溶液混合,配制0.2mol/L PH=7.4的磷酸缓冲溶液。已知该缓冲溶液利用的平衡体系是:H2PO4— H++HPO42—,请根据该平衡体系分析其缓冲原理: 。
H++HPO42—,请根据该平衡体系分析其缓冲原理: 。
-
(本题共14分)碱金属元素按原子序数增大,依次为:锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr,放射性元素)。请回答:
52.常温常压下,将一定量锂单质投入到一定量重水中,锂完全反应,产生1.6g气体,过滤得到6.75g沉淀和100mL澄清溶液。则得到的澄清溶液中溶质的物质的量浓度为 。
53.钠钾合金许多特殊反应中有着非常重要的应用。取59.80g钠钾合金和一定量四氯化碳在一定条件下恰好完全反应,制造出5.40g纳米级金刚石粉末。则该钠钾合金中钠元素和钾元素的质量比为 。
54.某同学在实验室模拟制备纯碱。0.600 mol NH3和35.100g食盐混合,得到氨盐水总质量为105.300 g。向该溶液通入CO2至反应完全,过滤,得到滤液88.200g,则NaHCO3的产率为______________。(保留三位小数)
55.一定条件下,85.5g铷与氧气和臭氧的混合气体22.4L(已折算为标况,且该混合气体对相同状况下氢气的相对密度为20.8)恰好完全反应,得到两种离子化合物A和B的固体混合物。A和B中,阴阳离子个数比均为1:1且均存在两种微粒间作用力,A的含氧量为0.3596。则化合物A的化学式为 。
将上述固体混合物加热,A可分解生成B和氧气。加热一段时间后,固体混合物中两种阴离子的物质的量相等,则分解产生的氧气在标况下的体积为 。
-
(本题共12分)目前,碳族元素按原子序数增大,依次为:碳(C)、硅(Si)、锗(Ge)、锡(Sn)、铅(Pb)。请回答:
23.锗原子的最外层电子排布式: ,锡原子的最外层电子云有 种伸展方向; 单质锗具有__________(填字母)。
a.只有金属性
b.只有非金属性
c.既有金属性,又有非金属性
24.某同学根据反应:SiO2 + 2C Si + 2CO↑,得出结论:碳的非金属性强于硅的反应。请对此给予评价并说明理由: 。
Si + 2CO↑,得出结论:碳的非金属性强于硅的反应。请对此给予评价并说明理由: 。
25.常温下,在400mL稀氢氟酸中,投入一颗石英玻璃,2.5min后,溶液质量减少了11.22g。此时SiF4为气体,则这段时间内用HF表示该反应的平均化学反应速率为 。
高温下,在容积固定的密闭容器中,用足量焦炭与一定量二氧化碳发生可逆的吸热反应生成了CO。回答26-27题:
26.下列选项中,一定符合反应达到化学平衡时情况的选项是 。
a.压缩体积达到新平衡时,CO的浓度增大的倍数比CO2的浓度增大的倍数更大
b.速率关系:2v(CO2)= v(CO)
c.转移电子数随温度升高而增多
d.气体密度随着焦炭的增加而增大
27.达到化学平衡之后,保持其他条件不变,移走少量CO,达到新的平衡时,下列选项中,增大的是 (填选项编号)。
A.CO2和CO浓度比 b.混合气体的密度
c.转化率 d.CO的体积分数
-
(共14分)已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子。R+核外有28个电子。请回答下列问题(用所对应的元素符号表示)。
(1)R在基态时价层电子排布式为 。
(2)写出R单质与A2G2及M最高价氧化物对应水合物反应的离子方程式 。
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NGX、G3、等二次污染物。测定大气中PM2.5的浓度方法之一是β一射线吸收法,β一射线放射源可用85Kr,已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则m/n=__(填数字)。

(4)1 mol晶体L中含有σ键的数目为________。
(5)G与M可形成MG3与MG2,MG3分子的空间构型是___,
MG2中M原子的杂化方式___。
(6)在(EA4)2R(MG4)2中存在的化学键除极性键外,还有________(填字母)。
a.离子键 b.氢键 c.配位键 d.金属键
-
已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子。R+核外有28个电子。请回答下列问题:(答题时,A、D、E、G、L、M、R用所对应的元素符号表示)
(1)E、G、M的第一电离能由大到小的顺序为 ________ 。
(2)下图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价。基态R2+的核外电子排布式为________ ;Q的化合价为 ________ 价。

(3)1 mol晶体L中含有δ键的数目为 ________ 。
(4)G与M可形成MG3与MG2,MG3分子的空间构型是________ ,MG2中M原子的杂化方式是________。
(5)在(EA4)2R(MG4)2中存在的化学键除极性键外,还有________ (填字母)。
a.离子键 b. 氢键 c.配位键 d.金属键
-
(12分)【选做题】本题包括A、B两小题,请选定其中一小题作答。若多做,则按A小题评分。
A.【物质结构与性质】
我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数与A的相同 |
请回答下列问题(用A、B、C、D、E所对应的元素符号作答):
(1)B、C、D第一电离能由小到大为______________。
(2)E的二价离子的电子排布式为______________。
(3)A2B2D4常用作除锈剂,该分子中B的杂化方式为____________;1 mol A2B2D4分子中含有σ键数目为____________。
(4)与化合物BD互为等电子体的阴离子化学式为__________(任写一种)。
(5)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是__________________。
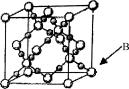
(6)BD2在高温高压下所形成晶体的晶胞如图所示。一个该晶胞中含________个D原子。
-
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
(1)X、Y、Z的电负性从大到小的顺序为______(用元素符号表示),元素Y的第一电离能大于Z的原因是______.
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.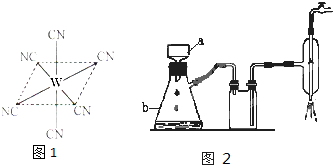
①W元素基态原子价电子排布式为______.
②已知CN-与______分子互为等电子体,1molCN-中π键数目为______.
③上述沉淀溶解过程的化学方程式为______.
B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是______;
②加热蒸发、浓缩溶液时,应加热到______时,停止加热.
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a______;b______.
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是______.
③用少量无水乙醇洗涤晶体的目的是______.
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量______(填“有”、“无”)影响,原因是______.
-
【选做题】(12分)本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
X、Y、Z、M为前四周期中除氢以外原子序数依次增大的四种元素,X基态原子未成对电子数在所处周期中最多;Y元素原子核外共有3个能级,且最高能级电子数是前两个能级电子数之和;Z的单质常温下为淡黄色固体,ZY3分子呈平面正三角形;M原子外围电子排布式为3dn4sn。
请回答下列问题:
(1)X、Y、Z三种元素原子第一电离能由大到小的顺序是 。(用元素符号表示)
(2)某X氢化物分子结构式为:H-X=X-H,该分子中X原子的杂化方式是 ;Y元素简单氢化物的沸点高于Z的氢化物,主要原因是 。
(3)根据等电子原理,写出X2Y分子的电子式: 。
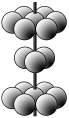
(4)M晶体的原子堆积方式为六方堆积(如图所示),则晶体中M原子配位数是 。某M配合物化学式是[M(H2O)5Cl]Cl2·H2O,1 mol该配合物中含配位键的数目是 。
-
氮族元素中有N、P、As三种非金属元素,请回答下列相关问题。
(1)基态砷原子的价电子排布式为_________________,同周期元素原子中与其含有相同数目未成对电子的是___________________(填元素符号)。
(2)雄黄(As4S4)是很多人熟悉的一种物质,其分子结构如图所示,分子中所有原子最外层均达到8电子结构。分子中含有的σ键的数目是__________________,●表示的原子是______________,该原子的杂化形式是____________________。

(3)硝酸的沸点较低,从氢键的角度推断其可能的原因是_______________________。硝酸根的空间构型是_____________________。
(4)白磷(P4)晶体中分子堆积方式属于分子密堆积,每个分子周围紧邻的分子有_________个。若白磷晶体晶胞的棱长为ypm,阿伏伽德罗常数的数值用NA表示,则白磷晶体的密度为____________g·cm-3。
-
氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价电子轨道表示式为___________;第二周期的元素中,第一电离能介于B和N之间的元素有___________种。
(2)雌黄的分子式为As2S3,其分子结构如图所示: As原子的杂化类型为___________。
As原子的杂化类型为___________。
(3)①向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。SO42-的空间构型为___________;[Cu(NH3)4]SO4·H2O固体中含有的化学键有___________(填标号)。
A.离子键 B.共价键 C.氢键 D.金属键 E.配位键
若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是进行___________实验。
②已知NF3与NH3分子的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是___________。
(4)大π键可用 表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为 。N2O分子中的大π键表示为_________________。
。N2O分子中的大π键表示为_________________。
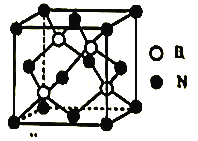
(5)立方氮化硼晶胞如图,其密度为ρg/cm3,氮化硼的摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,硼原子的半径为r cm,则硼原子的空间占有率为____________________(用含有ρ、M、NA、r的代数式表示)。
H++HPO42—,请根据该平衡体系分析其缓冲原理: 。






