-
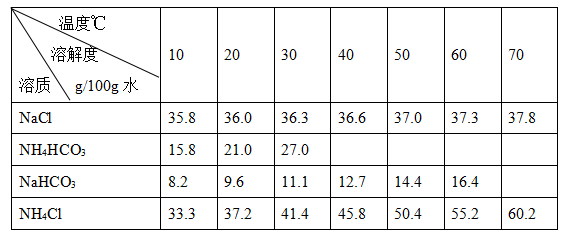
碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。各物质在不同温度下的溶解度见表。
实验步骤
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7。
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,a 、b ;③得到NaHCO3晶体。
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱。
完成下列填空:
(1)“化盐与精制”可除去的粗盐中的杂质离子是 。
(2)“转化”的离子方程式是 。
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是 ;为什么温度控制在30~35℃之间? 。
(4)a、b处的操作分别是 、 。
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1mL。此时发生的反应为:
CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是 。
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL。滴定终点时溶液颜色的变化是 ;根据实验数据,如何判断样品含NaHCO3 。
-
碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。各物质在不同温度下的溶解度见表。
|   温度℃ 温度℃
溶解度 溶质 g/100g水 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | | | | |
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
实验步骤
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7。
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置, a 、 b ;③得到NaHCO3晶体。
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱。
完成下列填空:
(1)“化盐与精制”可除去的粗盐中的杂质离子是________。
(2)“转化”的离子方程式是________。
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是________;为什么温度控制在30~35℃之间?________。
(4)a、b处的操作分别是、________。
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1 mL。此时发生的反应为:CO32- + H+ →HCO3-
①样品中碳酸钠质量百分含量的表达式是________。
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL。滴定终点时溶液颜色的变化是________;根据实验数据,如何判断样品含有NaHCO3________。
-
碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。
(1)饱和食盐水所用的原料粗盐主要来自于海洋,从海水中得到粗盐我们通常用的方法是_______。
(2)所得的粗盐(含Ca2+、Mg2+、SO42-)需要提纯,需要加入足量NaOH、BaCl2、Na2CO3溶液将杂质离子除去,随后过滤并加入盐酸调pH至7。其中先用BaCl2,再用Na2CO3的原因是______。
(3)饱和食盐水除用于制纯碱,也是氯碱工业的原料。氯碱工业中电解饱和食盐水的方程式为_______。
(4)测试纯碱产品中NaHCO3含量的方法是:用_______(定量仪器)称取纯碱样品1.144g,用蒸馏水溶解,加入0.500mol/L的HCl溶液100mL,再加1-2滴酚酞,继续用0.500mol/L标准氢氧化钠溶液滴定。当滴定至溶液由_____色变_____色,半分钟不变色为滴定终点。
(5)若上述过程中共消耗氢氧化钠58.00mL,纯碱样品中NaHCO3质量分数为_____。(保留3位小数)
(6)如果装氢氧化钠的滴定管滴定结束读数时有漏液情况,会导致测定结果______(选填“偏大”、“偏 小”、“不受影响”)。
-
某课外活动小组模拟工业制备纯碱,方案如下:
(一)实验原理:向饱和食盐水中通入足量氨气和过量二氧化碳,析出溶解度较小的碳酸氢钠。(1)写出相关离子方程式 。
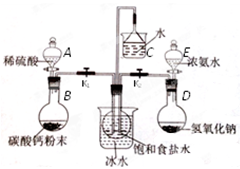
(二)实验装置:所需实验药品和装置如下图所示:
(三)实验步骤:
(2)组装好装置,然后应该进行的操作是 。
(3)中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中;D中加入足量氢氧化钠固体,E中加入足量浓氨水;B中加入足量碳酸钙粉末,A中 加入足量稀硫酸于(可分多次加入)。仪器A的名称是 ,选择用稀硫酸而不用稀盐酸的好处是 。
加入足量稀硫酸于(可分多次加入)。仪器A的名称是 ,选择用稀硫酸而不用稀盐酸的好处是 。
(4)先打开 (填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶。大约20分钟左右时,观察到饱和食盐水上方有 现象时,再打开 (填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,大约5分钟即有浑浊出现,约15分钟出现大量白色固体。
(四)纯碱制备:
(5)上述实验结束后,欲得到纯碱,将固体过滤、洗涤后,还需进行的操作是 (不加任何其它试剂,装置任选),反应的化学方程式为 ;若将上述操作产生的气体全部通过浓硫酸,再通过足量的过氧化钠,过氧化钠增重0.28g,则制得的纯碱质量为 g。
-
某课外活动小组模拟工业制备纯碱,方案如下:
(一)实验原理:NaCl+H2O+NH3+CO2═NaHCO3↓+NH4Cl
向饱和食盐水中通入足量氨气至饱和,然后通入二氧化碳,析出溶解度较小的碳酸氢钠.
(二)实验装置:所需实验药品和装置如图所示:

(三)实验步骤
(1)搭好装置,然后应该进行的操作是__________。
(2)中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中;D中加入足量氢氧化钠固体,E中加入足量浓氨水;B中加入足量碳酸钙粉末,A中加入足量稀硫酸于(可分多次加入).仪器A的名称是__________,选择用稀硫酸而不用稀盐酸的好处是__________。
(3)先打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,烧瓶中产生气体的原理是__________,大约20分钟左右时,观察到饱和食盐水上方有__________大量的白雾
现象时,再打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,大约5分钟即有浑浊出现,约15分钟出现大量白色固体.
(四)纯碱制备:
(4)上述实验结束后,欲得到纯碱,将固体过滤、洗涤后,还需进行的操作是__________(不加任何其它试剂,装置任选),反应的化学方程式为__________;若将上述操作产生的气体全部通过浓硫酸,再通过足量的过氧化钠,过氧化钠增重0.28g,则制得的纯碱质量为__________g。
-
(1)侯德榜制碱法生产流程为:

①沉淀池中反应的化学方程式: ;
②检验产品碳酸钠中是否含有氯化钠的操作方法为: 。
③上述流程中物质X的分子式为 。
(2)实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30—35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。
四种盐在不同温度下的溶解度表 (g/100g水)
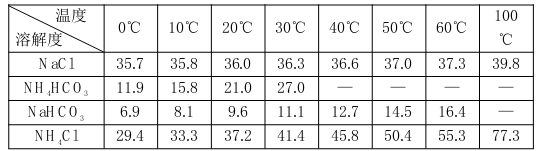
④反应控制在30—35℃,是因为高于35℃ NH4HCO3会分解,低于30℃则反应速率降低,为控制此温度范围,通常采取的加热方法为___________________;
⑤加料完毕,保温30分钟,目的 ;
⑥静置后只析出NaHCO3晶体的原因 ;
⑦过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使 (填化学式)循环使用,回收得到NH4Cl晶体。
-
(10分)在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3 + CO2 + NaCl + H2O == NH4Cl + NaHCO3↓,依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
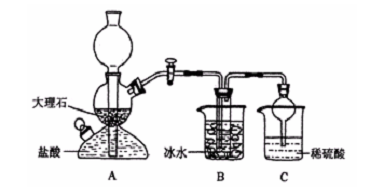
(1)A装置中所发生反应的离子方程式为: 。
C装置中稀硫酸的作用为: 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
-
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
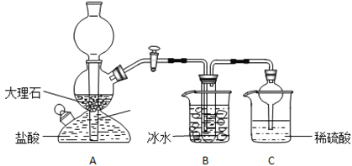
(1)A装置中所发生反应的离子方程式为:_________________。C装置中稀硫酸的作用为:________________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为________________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 ______装置____之间(填写字母)连接一个盛有_________ 的洗气装置,其作用是___________。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结论:______________。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为__________。
-
工业上常用氨碱法制取纯碱,是将氨和二氧化碳先后通入饱和食盐水而析出小苏打,再经过滤,焙烧而得纯碱。但不能用氨碱法制取碳酸钾,原因可能是 ( )
A.KHCO3溶解度较大 B.KHCO3溶解度较小
C.K2CO3溶解度较小 D.K2CO3溶解度较大
-
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献,他以饱和食盐水、 、
、 为原料先制得
为原料先制得 ,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示
,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示 图中夹持、固定用的仪器未画出
图中夹持、固定用的仪器未画出 。
。
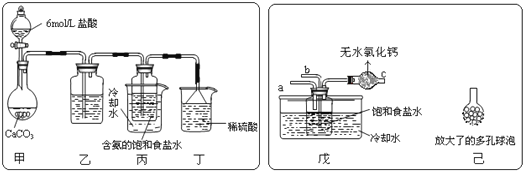
 乙装置中的试剂是___________。丁装置中稀硫酸的作用是_________________。
乙装置中的试剂是___________。丁装置中稀硫酸的作用是_________________。
 另一位同学用图中戊装置
另一位同学用图中戊装置 其他装置未画出
其他装置未画出 进行实验。实验时,须先从______管通入_____气体。
进行实验。实验时,须先从______管通入_____气体。
 有同学建议在戊装置的b管下端连接己装置,理由是________________。
有同学建议在戊装置的b管下端连接己装置,理由是________________。
 下表中所列出的是相关物质在不同温度下的溶解度数据
下表中所列出的是相关物质在不同温度下的溶解度数据 水
水 :
:
参照表中数据,请分析丙、戊装置中使用冷却水或者冰水的原因:____________。
 该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度
该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质 ,将晶体充分干燥后,称量质量为
,将晶体充分干燥后,称量质量为 。再将晶体加热到质量不再变化时,称量所得粉末质量为
。再将晶体加热到质量不再变化时,称量所得粉末质量为 。然后进行下图所示实验:
。然后进行下图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是______ 填字母
填字母 。
。
a.在加入氯化钙溶液后,振荡、静置,向上层清液中继续加入少量氯化钙溶液
b.在加入氯化钙溶液后,振荡、静置,向上层清液中再加入少量碳酸钠溶液
c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②所得晶体中碳酸氢钠的纯度为_______________。








