-
(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃10kPa下,10g甲醇燃烧生成CO2和液态水时放热226.8kJ。请写出表示甲醇燃烧的热化学方程式:
________
(2) 某些化学反应可用下式表示:A + B C + D + H2O
请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式。
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),
写出该反应的化学方程式:。
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用
或(任写两种试剂的名称)就可以鉴别C、D两种气体。
高三化学填空题中等难度题查看答案及解析
-
近年来,广州市的大部分公交车及部分出租车已采用LPG(液化石油气)作为汽车的燃料,其主要目的在于( )
A.防止石油短缺
B.降低成本
C.减少对大气的污染
D.加大发动机的动力高三化学选择题中等难度题查看答案及解析
-
从石油中提取的矿物燃料燃烧后,产生的气体对环境会造成污染.为减少汽车尾气对大气的污染,我国成功制造出新燃料作能源的“绿色汽车”,这种新燃料是( )
A.90号汽油
B.甲醇
C.92号汽油
D.0号汽油高三化学选择题中等难度题查看答案及解析
-
从石油中提取的矿物燃料燃烧后,产生的气体对环境会造成污染。为减少汽车尾气对大气的污染,我国成功地制造出以新燃料作能源的“绿色汽车”,这种新燃料是( )
A.90号汽油
B.甲醇
C.92号汽油
D.0号柴油
高三化学单选题简单题查看答案及解析
-
化学与生活密切相关,下列说法正确的是( )
①乙醇汽油是在汽油中加入适量乙醇作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染。
②聚乙烯塑料的老化是由于发生了加成反应。
③煤经过气化和液化等物理变化可以转化为清洁燃料。
④合成纤维、人造纤维及碳纤维都属于有机高分子材料。
⑤利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程。
⑥“地沟油”禁止食用,但可以用来制肥皂。
A.①②③ B.①④⑤ C.①⑤⑥ D.③④⑥
高三化学选择题简单题查看答案及解析
-
CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法。
I、甲醇可以补充和部分替代石油燃料,缓解能源紧张。利用CO可以合成甲醇。
(1) 已知:CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H2=-285.8kJ·mol-1
CH3OH(g)+3/2 O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
则CO(g)+2H2(g)=CH3OH(g) △H=____________kJ·mol-1
(2)一定条件下,在容积为2L的密闭容器中充入1mol CO与2 mol H2合成甲醇 平衡转化率与温度、压强的关系如右图所示。
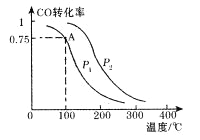
①在2 min时测得容器内甲醇的浓度为0.25 mol·L-1,则0-2 min内CO的平均反应速率为____mol·L-1·min-1,H2的转化率为____。
②由图判断P1_______P2(填“>” 、“<” 或“=” ),理由是____________________________________
③该甲醇合成反应在A点的平衡常数K=____
④下列措施中能够同时满足增大反应速率和提高CO转化率的是____。(填写相 应字母)
A、使用高效催化剂 b、降低反应温度 c、增大体系压强
D、不断将CH3OH从反应混合物中分离出来
Ⅱ、某学习小组以SO2为原料,采用电化学方法制取硫酸。
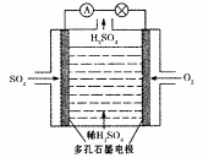
(3)原电池法:
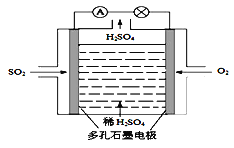
该小组设计的原电池原理如右图所示。
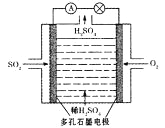
该电池中右侧为________极,写出该电池负极的电极反应式 ____。
(4)电解法:
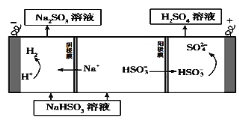
该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如右图所示。
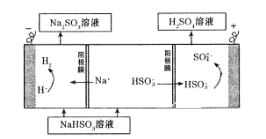
写出开始电解时阳极的电极反应式____________________
高三化学综合题困难题查看答案及解析
-
CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法.
Ⅰ.甲醇可以补充和部分替代石油燃料,缓解能源紧张,利用CO可以合成甲醇.
(1)已知:CO(g)+1/2O2(g)═CO2(g)ΔH1=-283.0kJ·mol-1
H2(g)+1/2O2(g)═H2O(l)ΔH2=-285.8kJ·mol-1
CH3OH(g)+3/2O2(g)═CO2(g)+2H2O(l)ΔH3=-764.6 kJ·mol-1
请写出CO与H2合成甲醇蒸汽的热化学方程式____________________
(2)一定条件下,在溶剂为VL的密闭容器中充入a molCO与2a molH2合成甲醇,平衡转化率与温度、压强的关系如图所示.
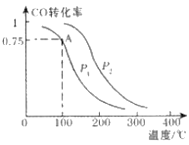
①该反应在A点的平衡常数K=_________________(用a和V表示)
②下列能说明反应达到平衡状态的是_____
A.v(CO)=v(H2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D. c(CO)=c(H2)
③写出能增大v(CO)又能提高CO转化率的一项措施_____________________________
Ⅱ.某学习小组以SO2为原料,采用电化学方法制取硫酸。
(3)原电池原理:该小组设计的原理示意图如左下图,写出该电池负极的电极反应式______。
(4)电解原理:该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如图,写出开始电解时阳极的电极反应式________________。
(5)已知25℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为________________________________(已知25℃时,H2SO3的电离平衡常数Ka1=1×10-2,Ka2=1×10-7)
高三化学填空题困难题查看答案及解析
-
CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法.
Ⅰ.甲醇可以补充和部分替代石油燃料,缓解能源紧张,利用CO可以合成甲醇.
(1)已知:CO(g)+1/2O2(g)═CO2(g)ΔH1=-283.0kJ·mol-1
H2(g)+1/2O2(g)═H2O(l)ΔH2=-285.8kJ·mol-1
CH3OH(g)+3/2O2(g)═CO2(g)+2H2O(l)ΔH3=-764.6 kJ·mol-1
请写出CO与H2合成甲醇蒸汽的热化学方程式____________________
(2)一定条件下,在溶剂为VL的密闭容器中充入a molCO与2a molH2合成甲醇,平衡转化率与温度、压强的关系如图所示.
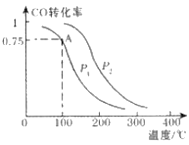
①该反应在A点的平衡常数K=_________________(用a和V表示)
②下列能说明反应达到平衡状态的是_____
A.v(CO)=v(H2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D. c(CO)=c(H2)
③写出能增大v(CO)又能提高CO转化率的一项措施_____________________________
Ⅱ.某学习小组以SO2为原料,采用电化学方法制取硫酸。
(3)原电池原理:该小组设计的原理示意图如左下图,写出该电池负极的电极反应式______。
(4)电解原理:该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如图,写出开始电解时阳极的电极反应式________________。
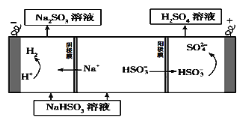
(5)已知25℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为________________________________(已知25℃时,H2SO3的电离平衡常数Ka1=1×10-2,Ka2=1×10-7)
高三化学填空题困难题查看答案及解析
-
近年来,北京公共汽车大部分采用天然气作为汽车的燃料,其主要目的是
A.防止石油短缺 B.降低成本
C.减少对大气的污染 D.加大发动机的动力
高三化学选择题简单题查看答案及解析
-
(14分)CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法。
I、甲醇可以补充和部分替代石油燃料,缓解能源紧张。利用CO可以合成甲醇。
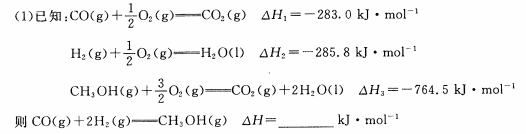
(2)一定条件下,在容积为VL的密闭容器中充入α mol CO与2a mol H2合成甲醇平衡转化率与温度、压强的关系如图所示。
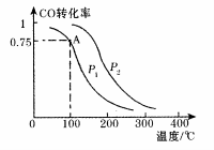
①P1__P2(填“>”、“<”或“=”),理由是
②该甲醇合成反应在A点的平衡常数K= (用a和V表示)
③该反应达到平衡时,反应物转化率的关系是:CO H2(填“>” 、“<” 或“=” )
④下列措施中能够同时满足增大反应速率和提高CO转化率的是 。(填写相应字母)
A、使用高效催化剂
B、降低反应温度
C、增大体系压强
D、不断将CH30H从反应混合物中分离出来
E、增加等物质的量的CO和H2
Ⅱ、某学习小组以SO2为原料,采用电化学方法制取硫酸。
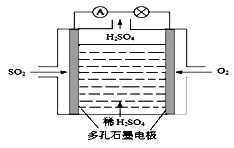
(3)原电池法:该小组设计的原电池原理如图所示。写出该电池负极的电极反应式 。
(4)电解法:该小组用Na2SO3溶液充分吸收S02得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如下图所示。
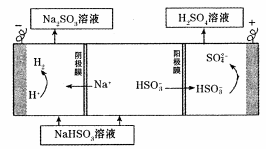
写出开始电解时阳极的电极反应式 。
高三化学填空题极难题查看答案及解析