下表是元素周期表的一部分,回答下列有关问题:
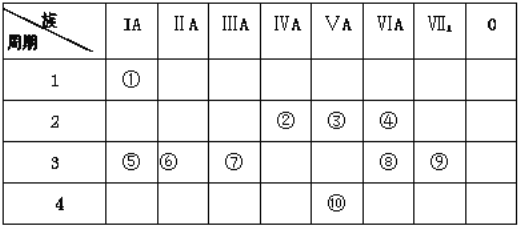
(1)从⑤到⑨元素中非金属性较强的元素是_________(用元素符号表示),这些元素的最高价氧化物对应的水化物中碱性最强的是 _________ (填化学式)。
(2)写出元素④具有强氧化性的氢化物的电子式:_______________。
(3)写出一种由①、③、④三种元素形成的常见离子化合物:________________。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________。
高二化学综合题中等难度题
下表是元素周期表的一部分,回答下列有关问题:

(1)从⑤到⑨元素中非金属性较强的元素是_________(用元素符号表示),这些元素的最高价氧化物对应的水化物中碱性最强的是 _________ (填化学式)。
(2)写出元素④具有强氧化性的氢化物的电子式:_______________。
(3)写出一种由①、③、④三种元素形成的常见离子化合物:________________。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________。
高二化学综合题中等难度题
下表是元素周期表的一部分,回答下列有关问题:

(1)从⑤到⑨元素中非金属性较强的元素是_________(用元素符号表示),这些元素的最高价氧化物对应的水化物中碱性最强的是 _________ (填化学式)。
(2)写出元素④具有强氧化性的氢化物的电子式:_______________。
(3)写出一种由①、③、④三种元素形成的常见离子化合物:________________。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________。
高二化学综合题中等难度题查看答案及解析
下列为元素周期表的一部分、表中阿拉伯数字(1、2……)是元素周期表中行或列的序号,请参照元素A~I在表中的位置,回答下列问题。
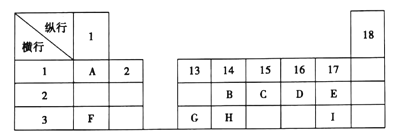
(1)B、C、H三元素中非金属性最强的是__________(写出元素符号)。
(2)表中某元素能形成两性氧化物,写出该氧化物的化学式___________。
(3)D与F构成原子个数比为1:1和1:2的两种离子化合物Z和M,写出Z与H2O反应的化学方程式_____________________________________。
高二化学填空题简单题查看答案及解析
一种价电子排布为2s22p5的元素,下列有关它的描述正确的有
A. 原子序数为8
B. 在同周期元素中非金属性最强
C. 在同周期元素中,其原子半径最大
D. 在同周期元素中,元素的第一电离能最大
高二化学单选题简单题查看答案及解析
一种价电子排布为2s22p5的元素,下列有关它的描述正确的有
A.原子序数为8
B.在同周期元素中非金属性最强
C.在同周期元素中,其原子半径最大
D.在同周期元素中,元素的第一电离能最大
高二化学单选题简单题查看答案及解析
如图是元素周期表的一部分,表中所列字母分别代表一种元素
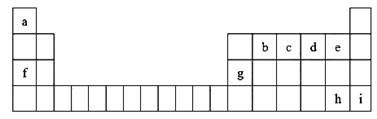
回答下列问题:
(1)h元素的名称是_________,九种元素中金属性最强的是_________(填元素符号)。
(2)f的最高价氧化物对应的水化物的化学式___________(填化学式)。
(3)b、c、d、e的原子半径依次___________(填增大或减小)。
(4)e、h元素的氢化物中,热稳定性大的是_________(填氢化物的化学式)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________。
高二化学填空题简单题查看答案及解析
A、B两元素的最外层都只有一个电子,A的原子序数等于B的原子序数的11倍,A离子的电子层结构与周期表中非金属性最强的元素的阴离子的电子层结构相同;元素C与B易形成化合物B2C,该化合物常温下呈液态,则:
(1)A的原子结构示意图为____,在固态时属于___晶体。
(2)C的单质属于___晶体。B与C形成化合物B2C的化学式为___,电子式为____;它是由___键形成的___分子,在固态时属于___晶体。
高二化学推断题简单题查看答案及解析
如图为元素周期表中短周期的一部分,下列说法正确的是
A.电负性:Y>Z>M
B.离子半径:M->Z2->Y-
C.Z和M的最高价含氧酸中非羟基氧原子数分别为2和3
D.Z元素基态原子的轨道表示式为:
高二化学单选题中等难度题查看答案及解析
下表是元素周期表的一部分,回答有关问题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | i | |
| 4 |
| k | l |
(1) 画出下列元素的轨道表示式:
a:________d:________
(2)写出下列元素原子的电子排布式:
k:________l:________
(3) 在这些元素中,第一电离能最小的元素是_____,电负性最大的元素是_____,最不活泼的元素是______;(填元素符号或化学式,下同)
(4) 在这些元素的最高价氧化物对应的水化物中,酸性最强的是_____,碱性最强的是_____,呈两性的氢氧化物是_____
(5) 在g与h元素中,非金属性较强的是_____,用一个化学方程式验证该结论:________
(6)元素d和e的电离能如下:
| 电离能kJ/mol | I1 | I2 | I3 | I4 |
| d | 738 | 1450 | 7730 | 10550 |
| e | 577 | 1817 | 2745 | 11578 |
请解释元素d的I1比元素e的I1大的原因
高二化学填空题简单题查看答案及解析
下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。其中J为0族元素。
| X | Y | Z | |
| R | |||
| W | |||
| J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)R原子的电子排布图为__________。
(2)在化合物YZ2中Y的化合价为__________;Y2-与Na+的半径大小为__________。
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是__________;X与Y的第一电离能:X__________Y(填“<”、“>”或“=”),其理由是__________________________________________________________。
【答案】 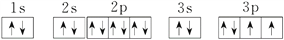 +2 O2->Na+ F>O>N > N原子的p轨道为半充满,能量低较稳定,难失电子
+2 O2->Na+ F>O>N > N原子的p轨道为半充满,能量低较稳定,难失电子
【解析】试题分析:X、Y、Z、R、W、J是前五周期的元素,其中J为0族元素,所以X、Y、Z、R、W、J分别是N、O、F、S、Br、Xe;
解析:(1)R是S元素,原子的电子排布图为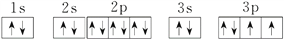 。
。
(2)化合物YZ2是OF2,F元素的化合价是-1,所以O元素的化合价为+2;O2-与Na+都有2个电子层,钠的质子数大于氧,所以半径大小为O2->Na+ 。
(3)同周期元素从左到右电负性增大,所以在N、O、F三种元素中,电负性由大到小的顺序是F>O>N;N原子2p能级半充满,能量低较稳定,第一电离能大于相邻的氧元素,N与O的第一电离能:N>O。
【题型】综合题
【结束】
22
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)I的最高化合价为__________,K的元素名称为__________。
(2)写出基态时Q元素原子的电子排布式__________,J元素原子的外围电子排布式________________。
(3)下列对比正确的是__________。
a.原子半径H>G>B>A
b.第一电离能E>D>C>B
c.电负性A>H>G>Q
d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是__________。
a.L位于元素周期表第五周期ⅠA族,属于s区元素
b.O位于元素周期表第七周期Ⅷ族,属于ds区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
高二化学综合题中等难度题查看答案及解析
(9分)下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
| X | Y | Z | |
| R | |||
| W | |||
| J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1) 在化合物YZ2中Y的化合价为________;Y2-与Na+的半径大小为_______________;
(2) R原子的电子轨道排布图为___________________________________;
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是______________________;X与Y的第一电离能:X___Y(填“<”、“>”或“=”),其理由是__________________________________。
(4)有一种酸HX3的酸性与醋酸相近,HX3溶液与NaOH溶液反应的离子方程式为:___________________________________。
高二化学填空题简单题查看答案及解析