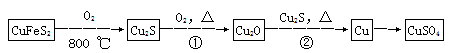-
(12分)【物质结构与性质】翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅。
(1)Na、Al、Si、O四种元素电负性由大到小的顺序为 。
(2)Cr3+的基态核外电子排布式为 。
(3)Cr可形成配合物K[Cr(C2O4)2(H2O)2],与H2O互为等电子体的一种分子是 (填化学式),水分子中氧原子的杂化方式为 ,1 mol H2C2O4分子中含有的σ键的数目为 。
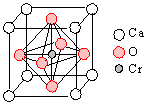
(4)Cr和Ca可以形成一种具有特殊导电性的复合氧化物,晶胞如图所示。该复合氧化物的化学式可表示为 。
-
翡翠的主要成分为 NaAlSi2O6,还含有其他多种金属阳离子。
(1)NaAlSi2O6所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:______________________。
(2)Al的电子排布式为______________________。
(3)配合物K[Cr(C2O4)2(H2O)]中的配体是:___________,H2O的中心原子的杂化轨道类型是:___________,与H2O互为等电子体的离子是:___________(任写一种)
(4)Ca、O、Gr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+,O2-采用面心立方最密堆积方式。
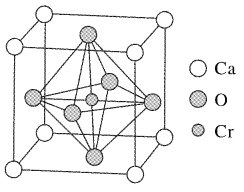
①该晶体的化学式为:_______________。
②已知钙离子、氧离子半径分别为100pm、140pm,该晶胞的参数(边长)为________pm。
-
[化学——选修5物质结构与性质]
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为 ,该元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4, B原子的杂化方式为 。
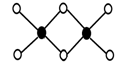
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“不是”)平面型分子。
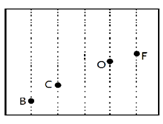
(4)依据第二周期元素第一电离能的变化规律,参照图中B、C、O、F元素的位置,用小黑点表示N元素的相对位置。
(5)Al单质为面心立方晶体,其晶体参数a=0.405nm,列式表示Al单质的密度: g·cm-3。
-
氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
A.使新鲜的红玫瑰花褪色(HCl) B.新制氯水呈浅黄绿色(Cl2)
C.加入小苏打固体,有气泡产生(H+) D.滴加AgNO3溶液生成白色沉淀(Cl-)
-
下列说法中,正确的是 ( )
A.由分子构成的物质中一定含有共价键
B.离子化合物中一定含有金属元素
C.正四面体结构的分子中的键角一定是109°28′
D.不同的原子的化学性质可能相同
-
(6分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,A为日常生活中常见的金属单质, G为黄绿色气体,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
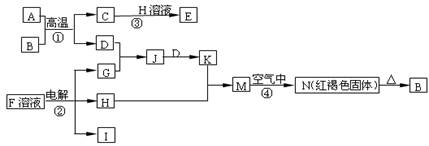
请回答下列问题:
(1)H的化学式为_______________。(2)反应②在工业上通常称之为__________工业。
(3)写出反应③的离子方程式。
(4)写出反应②的化学方程式________。
-
如图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去.反应①常被应用于野外焊接钢轨,A为日常生活中常见的金属单质,G为黄绿色气体,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液.
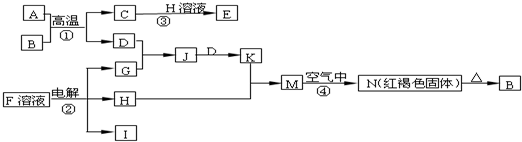
请回答下列问题:
(1)H的化学式为________.
(2)反应②在工业上通常称之为________工业.
(3)写出反应③的离子方程式________.
(4)写出反应②的化学方程式________.
-
【化学——选修3:物质结构与性质】目前半导体生产展开了一场“铜芯片”革命—在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
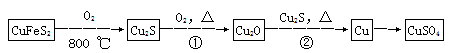
(1)基态铜原子的外围电子排布式为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是___,其立体结构是____。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深
沉淀溶解,得到深
蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式______;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
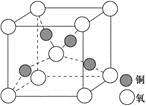
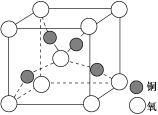
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。((用含d和NA的式子表示)。
-
【化学——选修3:物质结构与性质】目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
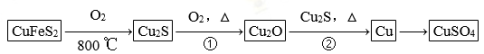
(1)基态铜原子的外围电子排布式为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、② 中均生成有相同的气体分子,该分子的中心原子杂化类型是____,其立体结构是______。
中均生成有相同的气体分子,该分子的中心原子杂化类型是____,其立体结构是______。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ___;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ___;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
(4) 铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。 (用含d和NA的式子表示)。
-
结构决定性质,性质决定用途;已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,Z的单质在常温下均为无色气体,W原子的最外层电子排布是nSn npn+2,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出W元素的元素符号和该原子基态的电子排布式:__ _____
(2)写出Z元素的原子结构示意图和该原子基态的电子排布图:_ _____
(3)X单质和Z单质在一定条件下反应生成化合物E,则E的电子式是:________。E可以进行喷泉实验的主要原因是:________。
(4)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子反应方程式为___________ __________________ ________
(5)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序)为(写名称)________,该化合物的浓溶液与足量NaOH热浓溶液反应的离子方程式为:____________ __ __