-
 某温度时,在一容积为1L的密闭容器中,加入 0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,5min时达到平衡,反应中NH3的物质的量浓度的变化情况如右图所示:
某温度时,在一容积为1L的密闭容器中,加入 0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,5min时达到平衡,反应中NH3的物质的量浓度的变化情况如右图所示:
请回答下列问题:
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(N2)= ________。
(2)该反应的化学平衡常数表达式为 。
(3)反应达到平衡后,第5min末保持其他条件不变,若改变反应温度,则NH3的物质的量浓度不可能为 ________(填序号)
a.0.82mol•L-1 b.0.25mol•L-1 c.0.20mol•L-1 d.0.08mol•L)
(4)反应达到平衡后,第5min末保持其他条件不变,若只把容器的体积缩小一半,平衡 ________ 移动(填“向右”、“向左”或“不”),化学平衡常数________(填“增大”、“减少”或“不变”)。(5) 其它条件不变,在第5min末将容器的体积缩小
一半,若第8min达到新的平衡(此时NH3的物
质的量约为0.25mol),请在上图中画出第5min
末到此平衡时NH3物质的量浓度的变化曲线。
-
在一定温度下容积恒定的密闭容器中,充入2mol A、1mol B和4mol M,发生如下反应: ,达到平衡后C的体积分数为
,达到平衡后C的体积分数为 若在相同条件下,x分别为2或3时,均按起始物质的量为
若在相同条件下,x分别为2或3时,均按起始物质的量为 A、
A、 B、
B、 C、2mol M充入容器中,分别达到平衡状态,两平衡状态中C的体积分数为
C、2mol M充入容器中,分别达到平衡状态,两平衡状态中C的体积分数为
A.两者都小于 B.两者都大于
B.两者都大于
C.两者都等于 D.无法确定
D.无法确定
-
.一定温度下,将4mol PCl3和2mol Cl2充入容积不变的密闭容器中,在一定条件下反应:
 ,各物质均为气态。达平衡后,PCl5为0.8mol。若此时再移走2molPCl3和lmolCl2,相同温度下达到平衡,PCl5的物质的量为 ( )
,各物质均为气态。达平衡后,PCl5为0.8mol。若此时再移走2molPCl3和lmolCl2,相同温度下达到平衡,PCl5的物质的量为 ( )
A.0.8mol B.0.4mol C. 0.4mol<x<0.8mol D.<0.4mol
-
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)⇌xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B、3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是( )
A.若平衡时,甲、乙两容器中A的物质的量不相等,则x=4
B.平衡时,甲、乙两容器中A、B的物质的量之比相等
C.平衡时甲中A的体积分数为40%
D.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5
-
将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)⇌2C(g);△H<0 4s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6mol•L-1,下列说法中正确的是( )
A.反应过程中,当A、B、C的物质的量浓度之比为 2:1:2时,反应即达到平衡状态
B.4 s 内用物质B表示的反应速率为0.075 mol•L-1•S-1
C.达平衡后若增大压强,A的转化率降低
D.达平衡后若升高温度,C的浓度将减小
-
温度容积相同的3个密闭容器中,按不同方式投入反应物并保持恒温恒容,测得反应达到平衡时的有关数据如下 已知:
已知: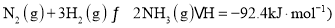
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol  、 、 | 2mol  | 4mol  |
|  的浓度 的浓度
| 
| 
| 
|
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | 
| 
| 
|
| 反应物转化率 | 
| 
| 
|
下列说法正确的是
A. B.
B. C.2
C.2 D.
D.
-
在容积可变的密闭容器中充入2mol苯蒸气和4mol氢气,恒温T1和恒压P1条件下进行如下反应: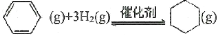 △H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )
△H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )
A.苯蒸气的体积分数不再变化时,说明该反应己达平衡状态
B.反应体系中气体总浓度保持不变,说明该反应己达平衡状态
C.在原平衡基础上,再向容器中充入3mol苯蒸气,平衡逆向移动
D.在原平衡基础上,升高温度,苯的转化率增大
-
将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)⇌2C(g),若经2s后测得C的浓度为0.6mol•L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol•L-1•s-1
②用物质B表示的反应的平均速率为0.6mol•L-1•s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol•L-1
其中正确的是( )
A.①③
B.①④
C.②③
D.③④
-
将E和F加入固定容积的密闭容器中,在一定条件下发生反应:
E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
(1)915℃、2.0MPa时E的转化率为________。
(2)该反应的△S________0(填“>”、“<”或“=”,下同),b________f。
(3)平衡常数K(1000℃)________ K(810℃) ,理由是________。
(4)对于上述反应,下列说法正确的是________(填序号)。
①混合气体的密度不再变化,反应达到平衡
②该反应的正反应为放热反应
③增大F的量,单位体积活化分子数增大,化学反应速率加快
④恒温恒容条件下通入惰性气体,平衡不移动
⑤恒温恒压条件下通入惰性气体,化学反应速率加快
-
某温度时,在一容积为1L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)⇌2NH3(g)△H<0,5min时达到平衡,反应中NH3的物质的量浓度的变化情况如图所示:请回答下列问题:(1)根据上图,计算从反应开始到平衡时,平均反应速率v(N2)=______.
(2)该反应的化学平衡常数表达式为______.
(3)反应达到平衡后,第5min末保持其他条件不变,若改变反应温度,则NH3的物质的量浓度不可能为______(填序号)
a.0.82mol•L-1 b.0.25mol•L-1 c.0.20mol•L-1 d.0.08mol•L-1
(4)反应达到平衡后,第5min末保持其他条件不变,若只把容器的体积缩小一半,平衡______移动(填“向右”、“向左”或“不”),化学平衡常数______(填“增大”、“减少”或“不变”).
(5)其它条件不变,在第5min末将容器的体积缩小一半,若第8min达到新的平衡(此时NH3的物质的量约为0.25mol),请在上图中画出第5min末到此平衡时NH3物质的量浓度的变化曲线.
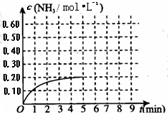
某温度时,在一容积为1L的密闭容器中,加入 0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,5min时达到平衡,反应中NH3的物质的量浓度的变化情况如右图所示:
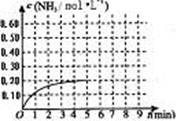
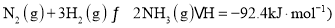
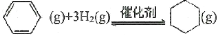 △H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )
△H1= -208.8kJ· mol-1,达平衡时容器的体积为2L,苯的转化率为50%。下列有关说法正确的是( )