C和H2在生产、生活、科技中是重要的燃料。
①2C(s)+O2(g) ===2CO(g) ΔH1=—220 kJ/mol
②
下列推断正确的是
A. C(s)的燃烧热110kJ/mol
B. 2H2(g)+O2(g)===2H2O(g)ΔH1=+480kJ/mol
C. C(s)+H2O(g)===CO(g)+H2(g)ΔH1=+130kJ/mol
D. 欲分解2molH2O(l),至少需要提供4×462kJ的热量
高三化学选择题中等难度题
C和H2在生产、生活、科技中是重要的燃料。
①2C(s)+O2(g) ===2CO(g) ΔH1=—220 kJ/mol
②
下列推断正确的是
A. C(s)的燃烧热110kJ/mol
B. 2H2(g)+O2(g)===2H2O(g)ΔH1=+480kJ/mol
C. C(s)+H2O(g)===CO(g)+H2(g)ΔH1=+130kJ/mol
D. 欲分解2molH2O(l),至少需要提供4×462kJ的热量
高三化学选择题中等难度题
C和H2在生产、生活、科技中是重要的燃料。
①2C(s)+O2(g) ===2CO(g) ΔH1=—220 kJ/mol
②
下列推断正确的是
A.C(s)的燃烧热110kJ/mol
B.2H2(g)+O2(g)===2H2O(g)ΔH1=+480kJ/mol
C.C(s)+H2O(g)===CO(g)+H2(g)ΔH1=+130kJ/mol
D.欲分解2molH2O(l),至少需要提供4×462kJ的热量
高三化学单选题中等难度题查看答案及解析
C和H2在生产、生活、科技中是重要的燃料。
①2C(s)+O2(g) ===2CO(g) ΔH1=—220 kJ/mol
②
下列推断正确的是
A. C(s)的燃烧热110kJ/mol
B. 2H2(g)+O2(g)===2H2O(g)ΔH1=+480kJ/mol
C. C(s)+H2O(g)===CO(g)+H2(g)ΔH1=+130kJ/mol
D. 欲分解2molH2O(l),至少需要提供4×462kJ的热量
高三化学选择题中等难度题查看答案及解析
碘及其化合物在生产、生活和科技等方面都有着重要的应用。回答下列问题:
(1)已知:①2I2(s)+5O2(g)=2I2O5(s) ΔH=—1966 kJ•mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=—1200 kJ•mol-1 。
则5CO(g)+I2O5(s)=5CO2(g)+I2(s)的△H= __________________________。
(2)碘不易溶于水,但易溶于碘化钾溶液并生成多碘离子,反应如下:
① I2(s)+I-(aq)I3-(aq) △H<0; ② I2 (s)+2I-(aq)
I42-(aq)。
温度降低时,反应①的平衡常数将______________(填“增大”“减小”或“不变”);反应②的平衡常数的表达式为K=__________________________。
(3)碘与钨在一定温度下,可发生如下可逆反应:W(s)+I2(g)WI2(g)。现准确称取0.508g碘和0.736g金属钨放置于50.0mL的密闭容器中,并加热使其反应。如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。

① 该反应△H____________0(填“>”或“<”)。
② 反应从开始到t1(t1= 3 min)时间内 I2 的平均反应速率v(I2)=_________。
③ 在450℃时,该反应的平衡常数K的值为__________________。
④ 能够说明上述反应已经达到平衡状态的有________________ (填选项字母)。
A.I2与WI2的浓度相等 B. 容器内各气体的浓度不再改变
C. 容器内混合气体的密度不再改变 D.容器内气体压强不发生变化
高三化学综合题困难题查看答案及解析
碘及其化合物在生产、生活和科技等方面都有着重要的应用。回答下列问题:
(1)已知:①2I2(s)+5O2(g)=2I2O5(s) ΔH=—1966 kJ•mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=—1200 kJ•mol-1 。
则5CO(g)+I2O5(s)=5CO2(g)+I2(s)的△H= __________________________。
(2)碘不易溶于水,但易溶于碘化钾溶液并生成多碘离子,反应如下:
① I2(s)+I-(aq)I3-(aq) △H<0; ② I2 (s)+2I-(aq)
I42-(aq)。
温度降低时,反应①的平衡常数将______________(填“增大”“减小”或“不变”);反应②的平衡常数的表达式为K=__________________________。
(3)碘与钨在一定温度下,可发生如下可逆反应:W(s)+I2(g)WI2(g)。现准确称取0.508g碘和0.736g金属钨放置于50.0mL的密闭容器中,并加热使其反应。如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
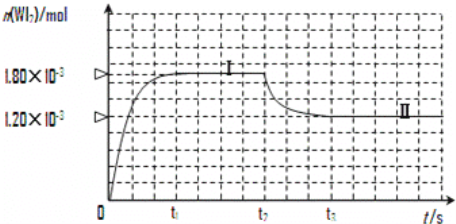
① 该反应△H____________0(填“>”或“<”)。
② 反应从开始到t1(t1= 3 min)时间内 I2 的平均反应速率v(I2)=_________。
③ 在450℃时,该反应的平衡常数K的值为__________________。
④ 能够说明上述反应已经达到平衡状态的有________________ (填选项字母)。
A.I2与WI2的浓度相等 B. 容器内各气体的浓度不再改变
C. 容器内混合气体的密度不再改变 D.容器内气体压强不发生变化
高三化学综合题困难题查看答案及解析
碘及其化合物在生产、生活和科技等方面都有着重要的应用。回答下列问题:
(1)已知:①2I2(s)+5O2(g)=2I2O5(s) ΔH=—1966 kJ•mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=—1200 kJ•mol-1 。
则5CO(g)+I2O5(s)=5CO2(g)+I2(s)的△H= __________________________。
(2)碘不易溶于水,但易溶于碘化钾溶液并生成多碘离子,反应如下:
① I2(s)+I-(aq)I3-(aq) △H<0; ② I2 (s)+2I-(aq)
I42-(aq)。
温度降低时,反应①的平衡常数将______________(填“增大”“减小”或“不变”);反应②的平衡常数的表达式为K=__________________________。
(3)碘与钨在一定温度下,可发生如下可逆反应:W(s)+I2(g)WI2(g)。现准确称取0.508g碘和0.736g金属钨放置于50.0mL的密闭容器中,并加热使其反应。如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
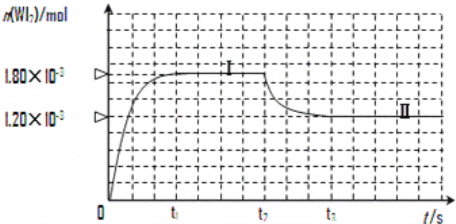
① 该反应△H____________0(填“>”或“<”)。
② 反应从开始到t1(t1= 3 min)时间内 I2 的平均反应速率v(I2)=_________。
③ 在450℃时,该反应的平衡常数K的值为__________________。
④ 能够说明上述反应已经达到平衡状态的有________________ (填选项字母)。
A.I2与WI2的浓度相等 B. 容器内各气体的浓度不再改变
C. 容器内混合气体的密度不再改变 D.容器内气体压强不发生变化
高三化学综合题困难题查看答案及解析
(14分)碳及其化合物在工农业生产生活中有着重要作用。请按要求回答下列问题:
(1)已知:C(s)+O2(g) = CO2(g) △H = -393 kJ•mol-1;
2CO(g)+O2(g) = 2CO2(g) △H = -566 kJ•mol-1;
2H2(g)+O2(g) = 2H2O(g) △H = -484 kJ•mol-1
将水蒸气喷到灼热的炭上可实现炭的气化(制得CO、H2),该反应的热化学方程式为______________________________________________________________________。
(2)将一定量CO(g)和H2O(g)分别通入容积为2 L的恒容密闭容器中,一定条件下发生反应为CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组实验数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
①该反应的正反应为 (填“吸热”或“放热”)反应。
②实验1中,0~4 min时段内,以v(H2)表示的反应速率为 。若在此温度下H2O(g)、CO(g)起始量分别为2 mol、4 mol,则此反应的平衡常数为___________。
③实验2达到平衡时CO的转化率为 。
④实验3与实验2相比,改变的条件是 ;
请在下图坐标中画出“实验2”与“实验3”中c(CO2)随时间变化的曲线,并作标注实验编号。

(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池的负极反应式为____________________________________。
(4)一定条件下,下图装置可实现有机物的电化学储氢(忽略其它有机物),则阴极的电极反应式为
______________________________________。

高三化学填空题极难题查看答案及解析
TiO2和TiCl4均为重要的化工原料,已知:
Ⅰ.TiCl4(g)+O2(g)TiO2(s)+2Cl2(g) ΔH=-175.4kJ/mol
Ⅱ.2C(s)+O2(g)2CO(g) ΔH=-220.9kJ/mol
请回答下列问题:
(1)TiCl4(g)+2CO(g)TiO2(s)+2C(s)+2Cl2(g)的ΔH=___kJ/mol。
(2)t℃时,向10L恒容密闭容器中充入1molTiCl4和2molO2,发生反应I,4min达到平衡时测得TiO2的物质的量为0.2mol。
①反应0~4min末的平均速率v(Cl2)=_,该温度下K=_(用分数表示),O2的平衡转化率=__。
②下列措施,既能加快正反应速率,又能增大O2的平衡转化率的是_。
A.缩小容器的体积
B.加入催化剂
C.分离出部分TiO2
D.增加O2的浓度
E.减低温度
F.以上方法均不可以
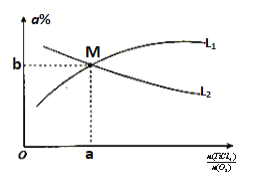
③t℃时,向10L恒容密闭容器中充入3molTiCl4和一定量的O2,发生反应I,两种气体的平衡转化率(a%)与起始的物质的量之比(TiCl4/O2)的关系如图1所示:能表示O2的平衡转化率的曲线为___(填“L1”或“L2”),M点的坐标为___(用整数或分数表示)。
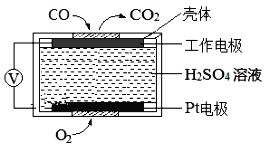
(3)CO是有毒气体,测定空气中CO含量常用的方法之一是电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为___;为减少对环境造成的影响,用CO和H2可以制备甲醇(CH3OH),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中溶质的主要成分是___(写化学式)。
高三化学综合题困难题查看答案及解析
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.
已知:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
A. CO的燃烧热为566.0 kJ•mol﹣1
B. 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低
C. 完全燃烧20g甲醇,生成二氧化碳和液态水时放出的热量为908.3 kJ
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H =﹣1453.28 kJ•mol﹣1
高三化学单选题中等难度题查看答案及解析
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。
已知:CH3OH(l)+O2(g)= CO(g)+2H2O(g)= -443.64 kJ·mol-1
2CO(g)+ O2(g)= 2CO2(g)= -566.0kJ·mol-1
下列说法或热化学方程式正确的是
A.CO的燃烧热为566.0 kJ·mol-1
B.2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低
C.完全燃烧20g甲醇,生成二氧化碳和液态水时放出的热量为908.3 kJ
D.2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g)=-1453.28 kJ·mol-1
高三化学选择题中等难度题查看答案及解析
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。
已知:CH3OH(l)+O2(g)= CO(g)+2H2O(g) =-443.64 kJ·mol-1
2CO(g)+ O2(g)= 2CO2(g) = -566.0kJ·mol-1
下列说法或热化学方程式正确的是
A.CO的燃烧热为566.0 kJ·mol-1
B.2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低
C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3 kJ
D.2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) =-1453.28 kJ·mol-1
高三化学选择题中等难度题查看答案及解析