-
空气质量高低直接影响着人类的生产和生活。《空气质量日报》中空气污染指数的项目有SO2、 CO、NOx、O3和可吸入颗粒物等。下列说法不正确的是 ( )
A.大气中的臭氧层对地球有很好的保护作用,所以大气中含有大量O3对人体有益
B.在催化剂作用下,CO和NOx可转化为无毒物质
C.血红蛋白中含有Fe2+,NO、CO容易与血红蛋白结合成稳定物质而使人中毒
D.SO2、NOx的大量排放会导致酸雨的产生
高三化学选择题中等难度题查看答案及解析
-
(13分)
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为________。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于________晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取________杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:__________________。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式________。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有________个。

③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中6个是配位键,请在图中用箭头标示出。
高三化学填空题中等难度题查看答案及解析
-
【化学——选修3:物质结构与性质】空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。请回答下列问题:
⑴ S、N、O的第一电离能由大到小的顺序为 。
⑵ 血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
①写出亚铁离子的基态电子排布式 。
CO有多种等电子体,其中常见的一种为 。
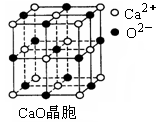
⑶ SO2是一种大气污染物,为减轻SO2污染,火力发电厂生产中常在燃煤中加入CaO以“固硫”。 CaO晶胞如右图所示,其中Ca2+的配位数为 ,CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO-3 401kJ/mol、NaCl-786kJ/mol。CaO晶体的熔点 NaCl晶体的熔点(填“高于”、“等于”或“低于”)。
⑷ 随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是-19.5 ℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65 ℃),甲醇的沸点明显高于甲醛的主要原因是: 。
高三化学填空题简单题查看答案及解析
-
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于________晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取________杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:
__________。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有个。
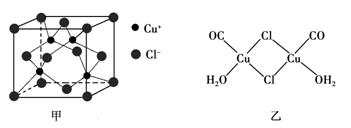
③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中________个是配位键,
高三化学填空题中等难度题查看答案及解析
-
化学与社会、生活密切相关,下列说法中错误的是
A.医用酒精是利用了乙醇使蛋白质变性来杀菌消毒.
B.空气质量日报中计入污染指数的项目为SO2、NOx、CO2
C.双氧水、高锰酸钾溶液消毒原理与漂白粉消毒饮用水的原理相同
D.锅炉水垢中含有的CaSO4可先用饱和碳酸钠溶液浸泡,然后用盐酸除去
高三化学单选题中等难度题查看答案及解析
-
化学与生活、生产密切相关,下列叙述正确的是
A.用含橙色的酸性重铬酸钾溶液的仪器检验酒驾,利用了乙醇的挥发性和还原性。
B.空气污染日报中的空气污染指数的主要项目有可吸入颗粒物、二氧化硫、二氧化氮和二氧化碳
C.为消除碘缺乏症,我国卫生部门规定食盐中必须加碘,其中碘元素以KI形式存在
D.为了获得更好的消毒效果,医用酒精的浓度通常为95%
高三化学单选题简单题查看答案及解析
-
下列叙述错误的是( )
A. 过程的自发性只能用于判断过程的方向性,不能确定过程是否一定会发生和过程发生的速率
B. 空气污染日报中的空气污染指数的主要项目有可吸入颗粒物、二氧化硫、二氧化氮
C. 金属冶炼过程主要是利用金属矿物中的金属离子失去电子变成金属单质所发生的氧化还原反应
D. 糖类和油脂是重要的基本营养物质,并且是人体所需能量的重要来源
高三化学选择题中等难度题查看答案及解析
-
今年入冬以来,银川雾霾天气频繁出现,空气质量很差,严重影响市民的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、S
O2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子
K+
Na+
NH4+
SO42-
NO3-
Cl-
浓度/mol·L-1
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
根据表中数据判断PM25的酸碱性为 ,试样的pH= 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:H2(g)+ 1/2O2(g) =H2O(g) △H=-241.8kJ·mol-1
C(s)+1/2O2(g) =CO(g)△H =-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式: 。
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g)
2NO(g) △H>0。若1mol空气含0.8molN2和0.2molO2,1300oC时在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K= 。汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
②目前,在汽车尾气系统中安装催化转化器可减少CO和NO的污染,反应方程式为 。
高三化学填空题困难题查看答案及解析
-
雾霾天气严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染。
请回答下列问题:
(1)汽车尾气中NOx和CO的生成:已知汽缸中生成NO的反应为:N2(g)+O2(g)
2NO(g)—Q。恒温、恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为1∶1∶2
D.氧气的转化率不再变化
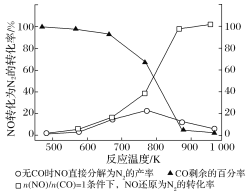
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以Ag—ZSM—5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为___,在
=1的条件下,为更好的除去NOx,应控制的最佳温度在___K左右。
(3)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质
温度(℃)
活性炭
NO
E
F
初始
3.000
0.10
0
0
T1
2.960
0.020
0.040
0.040
T2
2.975
0.050
0.025
0.025
①写出NO与活性炭反应的化学方程式:___。
②若T1<T2,则该反应的Q__0(填“>”“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为___。
高三化学解答题中等难度题查看答案及解析
-
雾霾天气严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此改善能源结构、机动车限号等措施能有效减少PM2.5。SO2、NOx等污染。
请回答下列问题:
(1)将一定量的某PM2.5 样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下测得该试样的组成及其浓度如下表:根据表中数据判断该试样的pH=________。
离子
K+
Na+
NH4+
SO42-
NO3-
CI-
浓度mol/L
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
(2)已知汽车汽缸中NO的生成反应为:N2(g)+ O2(g)
2NO(g) △H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是______________。
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.氧气的转化率不再变化 D.N2、O2、NO的物质的量之比为1: 1: 2
(3)为减少SO2 的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)==H2O(g) △H= -241.8kJ/mol
C(s)+1/2O2(g)==CO(g) △H=-110.5kJ/mol
写出焦炭与水蒸气反应的热化学方程式:__________________________。
②洗涤含SO2的烟气。下列可作为洗涤含SO2烟气的洗涤剂是________。
A.浓氨水 B.碳酸氢钠饱和溶液
C.FeCl2饱和溶液 D.酸性CaCl2饱和溶液
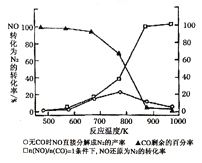
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为____________,在n(NO)/n(CO)=1的条件下,为更好的除去NOx物质,应控制的最佳温度在______K左右。
(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO 和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
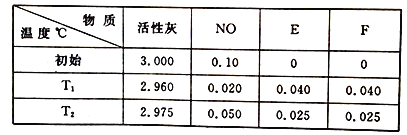
①写出NO与活性炭反应的化学方程式____________________________。
②若T12,则该反应的△H_____________0(填”>”、“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.lmol NO气体,则达到新化学平衡时NO的转化率为___________________。
高三化学综合题中等难度题查看答案及解析