-
(20分)思考下列问题,按要求填空:
(1)某温度下纯水中c(H+) = 2×10-7 mol/L
①此时溶液中的C(OH-) = ___ __。
②若温度不变,向水中滴入稀盐酸使c (H+) = 5×10-6 mol/L,则此时溶液中的C(OH-) =___ __。
(2)已知下列热化学方程式:Zn(s)+ O2(g)===ZnO(s) △H1=-351.1 kJ·mol-1;
O2(g)===ZnO(s) △H1=-351.1 kJ·mol-1;
Hg(l)+ O2(g)===HgO(s) △H2=-90.7 kJ·mol-1
O2(g)===HgO(s) △H2=-90.7 kJ·mol-1
由此可知反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的焓变为___ __。
(3)在稀氨水中存在下述电离平衡NH3+H2O  NH3 ·H2O
NH3 ·H2O  NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?___ __(填“增大”、“减小”或“不变”);平衡移动方向如何?___ __(填“正向”、“逆向”或“不移动”)。
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?___ __(填“增大”、“减小”或“不变”);平衡移动方向如何?___ __(填“正向”、“逆向”或“不移动”)。
| 加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c(OH-)的变化 | | 减小 | |
| 平衡移动方向 | 逆向 | | 逆向 |
(4)如图所示,装置B中两电极均为石墨电极,试回答下列问题:
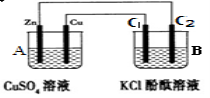
①判断装置的名称:A池为____ ____。
②锌极为___ ___极,电极反应式为_____ _______;
③当C2极析出224 mL气体(标准状况下),锌的质量减少_ _g
-
按要求回答下列问题
(1)某温度下,纯水中c (H+)=2.0×10-7mol•L-1,则此时c (OH-)=______mol•L-1;0.9mol•L-1NaOH溶液与0.1mol•L-1HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH=______.
(2)向0.020mol•L-1的HCN溶液中加入0.020mol NaCN固体,溶液pH增大,主要原因是______;已知该混合溶液中c (Na+)>c (CN-),则c (HCN)______c (CN-)(用“>”、“<”、“=”符号填空).
(3)向1L 0.10mol•L-1的HCN溶液中加入0.08molNaOH固体,得到混合溶液,则______和______两种粒子的物质的量之和等于0.1mol;写出该混合溶液中存在的所有平衡的表达式______.
-
按要求回答下列问题
(1)某温度下,纯水中c (H+)=2.0×10-7 mol·L-1,则此时c (OH-) =________mol·L-1
0.9mol·L-1NaOH溶液与0.1mol·L-1HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH=_____。
(2)向0.020 mol·L-1的HCN溶液中加入0.020 mol NaCN固体,溶液pH增大,主要原因是________;已知该混合溶液中c (Na+) > c (CN-),则c (HCN)________c (CN-)(用“>”、“<”、“=”符号填空)。
(3)向1L 0.10 mol·L-1的HCN溶液中加入0.08molNaOH固体,得到混合溶液,则_________和__________两种粒子的物质的量之和等于0.1mol;写出该混合溶液中存在的所有平衡的表达式________。
-
(10分)按要求填空。
(1)某温度下,纯水中c (H+)=4.0×10-7 mol·L1,则此时c (OH-)= mol·L-1。若温度不变,滴入稀硫酸使c (H+)=8.0×10-6 mol·L1,则c (OH-) = mol·L-1。
(2)某温度时,水的离子积常数KW=10-12,则该温度_______(选填“大于”“小于”或“等于”)25℃。若将此温度下pH=10的NaOH溶液aL与pH=1的稀硫酸bL混合,(设混合后溶液体积的微小变化忽略不计),若所得混合液为中性,则a:b=_______;若所得混合液pH=2,则a:b=_______。
-
请按要求回答下列问题:
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=__mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为__,由水电离出的c(OH-)=___mol·L-1。
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数___(填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是___。
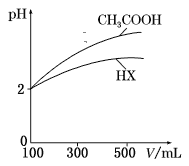
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___。(用a、b、c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___。
③25℃时,等浓度的HCN和NaCN混合溶液显___性。(酸、碱、中)
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
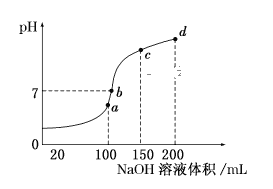
试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
-
应用化学反应原理知识解决下列问题
(1)某温度下纯水中c (H+) = 2.0×10-7 mol·L-1,则此纯水中的c (OH-) =________。
(2)将某CH3COOH溶液稀释10倍,则稀释后的溶液中c(H+)________原来的十分之一(填“大于”、“小于”或“等于”)。
(3)0.1 mol·L-1的下列溶液①HCl、②CH3COOH、③CH3COONa、④FeCl3、⑤NaOH,其中pH最大的是________(填序号);实验室配制的氯化铁溶液显弱酸性的原因:(用离子方程式表示)。
(4)一定条件下22g二氧化碳气体与足量氢气反应生成气态甲醇(CH3OH)和水蒸气时,放出247.5kJ热量,其反应的热化学方程式为。
-
电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol·L-1, 在该温度下,0.05mol/L的Ba(OH)2溶液的pH=________;
(2)在NaHS溶液中物料守恒:_________
(3)将AgCl分别放入:①5 mL水②40 mL 0.3mol·L-1 盐酸溶液中溶解至溶液饱和③10mL0.1 mol·L-1 MgCl2溶液④20 mL 0.5mol·L-1 NaCl溶液 ,各溶液中Ag+的浓度分别为a、b、c、d,它们由大到小的排列顺序是_________(用字母表示)。
(4)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质中最适宜采用的是________(填选项字母)
A.KMnO4 B.H2O2 C.氯水 D.HNO3
(5)如图所示,是原电池的装置图。请回答:
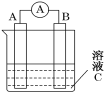
若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为______;反应进行一段时间后溶液C的pH将________(填“变大”、“变小”或“基本不变”)。
-
电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol·L-1, 该温度下,pH=10的Ba(OH)2溶液的物质的量浓度为_________ mol·L-1。
(2)25℃时,将 a mol·L-1 的醋酸和 b mol·L-1 的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=__________ mol·L-1,a_______ b(填“﹥”、“﹤”或“=”)。
(3)工业上采取用氨水除去SO2,已知25 ℃,NH3• H2O的Kb=1.8×10-5,H2SO3的 Ka1=1.3 × 10一2,Ka2=6.2 × 10一8。若氨水的浓度为2.0 mo1/ L,溶液中的c(OH-)=_____ mo1/ L;将SO2通入该氨水中,当c(OH-)降至2.0 × 10一6mo1/ L时,溶液中的 =_____________。
=_____________。
(4)将AgCl分别放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液③40 mL 0.3mol·L-1 盐酸溶液中溶解至溶液饱和 ④20 mL 0.5mol·L-1 NaCl溶液 ,各溶液中Ag+的浓度分别为a、b、 c、d,它们由大到小的排列顺序是____________(用字母表示)。
-
电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol·L-1, 该温度下,pH=10的Ba(OH)2溶液的物质的量浓度为_________ mol·L-1。
(2)25℃时,将 a mol·L-1 的醋酸和 b mol·L-1 的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=__________ mol·L-1,a_______ b(填“﹥”、“﹤”或“=”)。
(3)工业上采取用氨水除去SO2,已知25 ℃,NH3• H2O的Kb=1.8×10-5,H2SO3的 Ka1=1.3 × 10一2,Ka2=6.2 × 10一8。若氨水的浓度为2.0 mo1/ L,溶液中的c(OH-)=_____ mo1/ L;将SO2通入该氨水中,当c(OH-)降至2.0 × 10一6mo1/ L时,溶液中的 =_____________。
=_____________。
(4)将AgCl分别放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液③40 mL 0.3mol·L-1 盐酸溶液中溶解至溶液饱和 ④20 mL 0.5mol·L-1 NaCl溶液 ,各溶液中Ag+的浓度分别为a、b、 c、d,它们由大到小的排列顺序是____________(用字母表示)。
-
电解质在水溶液中存在各种行为,如电离、水解等,据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6 mol/L,则该温度下,pH=10的Ba(OH)2溶液的物质的量浓度为_________。
(2)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中,c(CH3COO—)—c(Na+) =_____________。(填准确数值)
O2(g)===ZnO(s) △H1=-351.1 kJ·mol-1;
O2(g)===HgO(s) △H2=-90.7 kJ·mol-1
NH3 ·H2O
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?___ __(填“增大”、“减小”或“不变”);平衡移动方向如何?___ __(填“正向”、“逆向”或“不移动”)。



