-
下列叙述中,不正确的是( )
A. 久置在空气中的NaOH溶液,加盐酸时有气体产生
B. 50 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,生成Cl2的量小于0.15 mol
C. 在常温下,浓H2SO4不与Cu反应,是因为铜被钝化
D. 用浓氨水可检验氯气管道是否漏气
高一化学单选题中等难度题查看答案及解析
-
下列叙述正确的是( )
A. 久置在空气中的NaOH溶液,加盐酸时有气体产生
B. 50 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,生成0.15 mol Cl2
C. 在常温下,浓H2SO4不与Cu反应,是因为铜被钝化
D. CO2通入浓的CaCl2溶液中产生白色沉淀
高一化学单选题中等难度题查看答案及解析
-
下列叙述正确的是( )
A. 久置在空气中的NaOH溶液,加盐酸时有气体产生
B. 50 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,生成0.15 mol Cl2
C. 在常温下,浓H2SO4不与Cu反应,是因为铜被钝化
D. CO2通入浓的CaCl2溶液中产生白色沉淀
高一化学单选题中等难度题查看答案及解析
-
下列叙述中,不正确的是( )
A.久置在空气中的NaOH溶液,加盐酸时有气体产生
B.50 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,生成Cl2的量小于0.15 mol
C.在常温下,浓H2SO4不与Cu反应,是因为铜被钝化
D.用浓氨水可检验氯气管道是否漏气
高一化学单选题中等难度题查看答案及解析
-
(12分)在两份体积相同的NaOH溶液中,分别通入CO2气体,充分反应后,在所得溶液A、B中分别加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示,试填写下列空白:

⑴两份NaOH溶液A和B的物质的量浓度之比为,通入CO2气体的体积之比是(相同条件)。
⑵与盐酸反应前,A溶液中的溶质是,其物质的量之比是________。
⑶与盐酸反应前,B溶液中的溶质是,其物质的量之比是________。
高一化学填空题简单题查看答案及解析
-
有50mL NaOH溶液,向其中逐渐通入一定量的CO2,随后向溶液中逐滴加入0.1mol/L的盐酸,产生的CO2气体体积(标准状况)与所加入的盐酸的体积之间的关系如图所示:
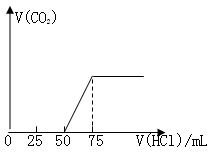
试计算:
(1)向NaOH溶液中通入CO2气体后,所得溶液
中的溶质是________,其物质的量之比为________。
(2)产生的CO2气体体积(标准状况)是________L。
(已知:Na2CO3与HCl反应分步进行,第一步:Na2CO3+HCl=NaHCO3+NaCl;
第二步:NaHCO3+HCl=NaCl +CO2↑+H2O)
高一化学填空题简单题查看答案及解析
-
向50mL NaOH溶液中通入一定量的CO2(假设溶液体积不变),随后取溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol•L﹣1的盐酸,产生CO2气体的体积(标准状况下)与所加盐酸的体积关系如图所示。
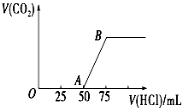
(1)写出OA段所发生反应的离子方程式: .
(2)NaOH在吸收CO2后,所
得溶液的溶质为 ,其物质的量浓度之比为 .
(3)产生的CO2体积(标准状况下)为 .
(4)原NaOH溶液的物质的量浓度为 .
高一化学填空题极难题查看答案及解析
-
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示。
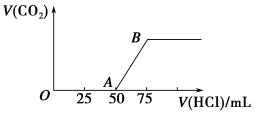
(1)写出OA段所发生反应的离子方程式:_________________________________。
(2)NaOH在吸收CO2后,所得溶液的溶质为___________________________,其物质的量浓度之比为________。
(3)产生的CO2体积(标准状况下)为___________________________________________。
(4)原NaOH溶液的物质的量浓度为________。
高一化学填空题困难题查看答案及解析
-
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1盐酸,产生CO2气体的体积(标准状况下)与所加入盐酸的体积关系如下图所示。
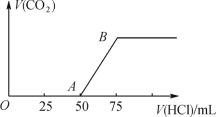
(1) 写出OA段所发生反应的离子方程式:______________。
(2)NaOH在吸收CO2后,所得溶液的溶质为____,其物质的量浓度之比为____。
(3)产生CO2的体积(标准状况下)为____。
(4)原NaOH溶液的物质的量浓度为___。
高一化学填空题困难题查看答案及解析
-
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是

A.OA段所发生反应的离子方程式: H++OH-=H2O;CO32-+H+=HCO3-
B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1
C.产生的CO2体积(标准状况下)为0.056 L
D.原NaOH溶液的物质的量浓度为0.5 mol·L-1
高一化学选择题极难题查看答案及解析