硫化氢裂解制取氢气的反应为2H2S(g)2H2(g)+S2(g)。向恒容密闭容器中充入一定量的H2S气体,测得体系中气体的平衡组成与温度的关系如图所示。下列说法正确的是

A. 该反应平衡常数随温度升高而增大
B. M点时容器内气体总压强比N的大
C. M点时,H2S的平衡转化率为50%
D. 维持M点温度不变,向容器中再充入0.2molH2S、0.2molH2、0.1molS2(g),则v(正) = v(逆)
高二化学多选题中等难度题
硫化氢裂解制取氢气的反应为2H2S(g)2H2(g)+S2(g)。向恒容密闭容器中充入一定量的H2S气体,测得体系中气体的平衡组成与温度的关系如图所示。下列说法正确的是

A. 该反应平衡常数随温度升高而增大
B. M点时容器内气体总压强比N的大
C. M点时,H2S的平衡转化率为50%
D. 维持M点温度不变,向容器中再充入0.2molH2S、0.2molH2、0.1molS2(g),则v(正) = v(逆)
高二化学多选题中等难度题
硫化氢裂解制取氢气的反应为2H2S(g)2H2(g)+S2(g)。向恒容密闭容器中充入一定量的H2S气体,测得体系中气体的平衡组成与温度的关系如图所示。下列说法正确的是

A. 该反应平衡常数随温度升高而增大
B. M点时容器内气体总压强比N的大
C. M点时,H2S的平衡转化率为50%
D. 维持M点温度不变,向容器中再充入0.2molH2S、0.2molH2、0.1molS2(g),则v(正) = v(逆)
高二化学多选题中等难度题查看答案及解析
硫化氢分解制取氢气和硫磺的原理为2H2S(g)S2(g)+2H2(g),在2.0 L恒容密闭容器中充入0.1 mol H2S,不同温度下测得H2S的转化率与时间的关系如图所示。下列说法正确的是
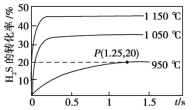
A. 该反应的正反应为放热反应
B. 图中P点:v(正)>v(逆)
C. 950 ℃时,0~1.25 s生成H2的平均反应速率为0.016 mol·L-1·s-1
D. 950 ℃时,该反应的平衡常数值小于3.125×10-4
高二化学单选题困难题查看答案及解析
硫化氢分解制取氢气和硫磺的原理为:2H2S(s)S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,不同温度下测得H2S的转化率与时间的关系如图所示.下列说法正确的是

A.图中P点:v(正)<v(逆)
B.正反应为放热反应
C.950℃时,0~1.25s生成H2的平均反应速率为:0.008mol•L-1•s-1
D.950℃时,该反应的平衡常数的值小于3.125×10-4
高二化学选择题中等难度题查看答案及解析
硫化氢气体在资源利用和环境保护等方面均有重要应用。
(1)工业采用高温分解H2S制取氢气,2H2S(g) 2H2(g) + S2(g),在膜反应器中分离出H2。在容积为 2L 的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为 1mol,实验过程中测得H2S的转化率如图所示。曲线 a 表示H2S的平衡转化率与温度的关系,曲线 b 表示不同温度下反应经过相同时间时H2S的转化率。
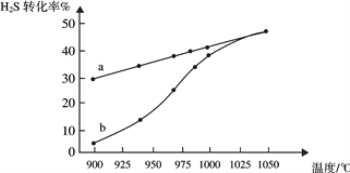
①反应2H2S(g) 2H2(g) + S2(g)的ΔH_________(填“>”“<”或“=”)0。
②985℃时,反应经过5 s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2) =___________。
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是___________。
(2)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。

①在图示的转化中,化合价不变的元素是____________。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有____________。

(3)工业上常采用上图电解装置电解K4[Fe(CN)6]和KHCO3混合溶液,电解一段时间后,通入H2S 加以处理。利用生成的铁的化合物K3[Fe(CN)6]将气态废弃物中的H2S 转化为可利用的S,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为___________。
②当有16 g S析出时,阴极产生的气体在标准状况下的体积为___________。
高二化学综合题困难题查看答案及解析
在两个容积均为2L恒温密闭容器中,起始时均充入amolH2S,控制不同温度和分别在有、无Al2O3催化时进行H2S的分解实验[反应为:2H2S(g)2H2(g)+S2(g)]。测得的结果如下图所示(曲线Ⅱ、Ⅲ表示经过相同时间且未达到化学平衡时H2S的转化率)。
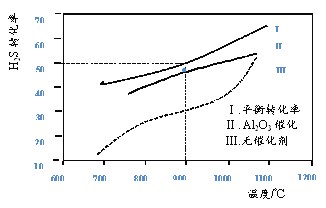
下列说法不正确的是
A. H2S分解为放热反应
B. 加入Al2O3 可提高H2S的平衡转化率
C. 900℃反应2H2S(g)2H2(g)+S2(g)的平衡常数K=0.125a
D. 约1100℃曲线Ⅱ、Ⅲ几乎重合,说明Al2O3可能几乎失去催化活性
高二化学多选题中等难度题查看答案及解析
为研究温度对反应2H2S(g)2H2(g) +S2(g)的影响,兴趣小组进行如下探究:向三个体积均为2L的恒容密团容器(A1、A2、A3)中分别加入等量的H2S,进行H2S分解实验。在T1、T2、T3,下测得H2的物质的量与时间的关系如下图所示:
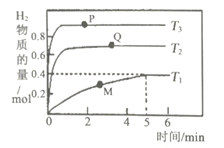
(1)该反应的△H____0(填“>”“<”或“=”,下同),T2、T3温度下的平衡常数K2______K3。
(2)T1温度下,前5min用S2(g)表示的反应速率为_____。
(3)图中P、Q、M三点逆反应速率由小到大的顺序是_____。
(4)已知v正=k正c2(H2S),v逆=k逆c2(H2)c(S2), 温度为T1时,k逆=3.4k正。则该温度下的化学平衡常数的值为___(保留小数点后两位数字)。
(5)在A容器中,下列选项中能标志反应2H2S(g)2H2(g) +S2(g)达到平衡的是___(填写序号)。
a v正(H2S)=2v逆(S2) b H2和S2的浓度之比为2;1
c 密度不再变化 d 平均相对分子质量不再发生变化
高二化学综合题简单题查看答案及解析
H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) ∆H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法正确的是( )
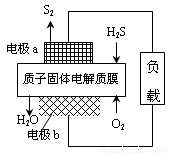
A. 电池工作时,电流从电极a经负载流向电极b
B. 电极a上发生的电极反应为:2H2S - 4e-= S2 + 4H+
C. 当反应生成64gS2时,电池内部释放632kJ热能
D. 当电路中通过4mol电子时,有4mol H+经质子膜进入负极区
高二化学选择题困难题查看答案及解析
硫化氢是一种急性剧毒气体,回收硫化氢解决了环境污染问题也可变废为宝。其反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632 kJ·mol-1。在酸性固体电解质环境下,硫化氢的处理原理图如图所示。下列说法正确的是
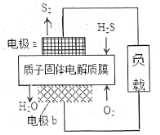
A.电极a的电极反应式为2H2S-4e-=S2+4H+
B.电子由电极a经质子固体电解质膜流向电极b
C.1 mol的H2S气体完全反应得到固体S2和水蒸气放热316kJ
D.负载中电流的方向自上而下
高二化学单选题中等难度题查看答案及解析
恒温时,某固定容积的密闭容器中发生可逆反应:H2(g) + I2(g)2HI(g),下列一定处于平衡状态的是
A.混合气体颜色不再改变时
B.氢气的消耗速率等于碘化氢的消耗速率时
C.氢气的浓度等于碘蒸气的浓度时
D.混合气体的平均相对分子质量不变时
高二化学选择题中等难度题查看答案及解析
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g)2H2(g)+O2(g)△H = +484kJ·mol—1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反应过程中能量转化形式为光能转化为 能,达平衡过程中至少需要吸收光能为 kJ。
(2)现有反应:CO(g)+ H2O(g) CO2(g)+ H2(g) △H<0,在相同温度和相同体积下进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
| 物质的量 | CO | H2 O | CO2 | H2 |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 0mol | 0 mol | 2a mol | a mol |
| 丙 | 0 mol | 0 mol | a mol | a mol |
| 丁 | a mol | a mol | a mol | a mol |
上述四种情况达到平衡后,甲、乙、丙、丁容器中n(CO)的大小顺序为 。
(3)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3得金属钨,总反应为WO3 (s) + 3H2 (g)W (s) + 3H2O (g)。请回答下列问题:
①某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为 。
②上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为 。
③钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) WI4 (g)。下列说法正确的有 (填字母)。
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
高二化学填空题极难题查看答案及解析