-
按要求回答下列问题:
Ⅰ、稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的离子反应方程式_________________________________。
Ⅱ、常温下,向20mL 0.2mol•L﹣1H2A溶液中滴加0.2mol•L﹣1NaOH溶液.有关微粒的物质的量变化如下图(Ⅰ代表H2A,Ⅱ代表HA﹣,Ⅲ代表A2﹣)
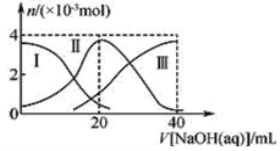
(1)H2A在水中的电离方程式为_________________________。
(2)当V(NaOH)=20 mL时,写出H2A与NaOH反应的离子方程式_________________。此时溶液中所有离子浓度大小关系:__________________。
(3)向NaHA溶液中加水,HA﹣的电离度_________、溶液的pH________。(填增大、减小、不变、无法确定)。
(4)V(NaOH)=30 mL时,溶液中存在如下关系:2c(H+)﹣2c(OH﹣)________2c(A2﹣)﹣3c(H2A)﹣c(HA﹣)(填“<”“>”或“=”)。
(5)某校研究性学习小组开展了题为“H2A是强酸还是弱酸的实验研究”的探究活动。该校研究性学习小组设计了如下方案:你认为下述方案可行的是_______(填编号);
A.测量浓度为0.05 mol/L H2A溶液的pH,若pH大于1,则可证明H2A为弱电解质
B.可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.比较中和等体积、等物质的量浓度的硫酸和H2A溶液所需氢氧化钠的量多少,可证明H2A是强酸还是弱酸。
-
回答下列有关Na2S溶液的问题。
(1)Na2S溶液盛装在带橡胶塞的试剂瓶中,仔细闻有臭鸡蛋气味,请用离子方程式解释:
________,________。
(2)将Na2S溶液加入AlCl3溶液中,有白色沉淀和臭鸡蛋气味的气体生成,发生的离子反应为:
________。
(3)将Na2S溶液加入AgCl的浊液中,生成的黑色沉淀是(写化学式)。
-
(1)某同学想把AlCl3溶液和Na2S溶液混合制取A12S3,但最后得到一种白色絮状沉淀,而且混合液中有臭鸡蛋气味的气体放出。试写出该反应的离子方程式_____________。
(2)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4C1溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。则:B是_____溶液,C是_____溶液
(3)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2,pH由大到小的顺序为:____(用序号表示)
(4)物质的量浓度相同的五种溶液①(NH4)2SO4 ②氨水③NH4HSO4④NH4HCO3⑤NH4NO3,c(NH4+)由大到小的顺序是_____;(用序号表示)
(5)常温下的pH=5 NH4Cl溶液 和pH=5 醋酸溶液,其中水电离出 c(H+)之比为_____。
-
21、(4分)某同学设计用AlCl3溶液和Na2S溶液反应制取硫化铝(Al2S3)固体,你认为他能达到目的吗?________原因是(用离子方程式表示):________。配制Na2S溶液时,为了防止水解,常向溶液中加入少量________,用离子方程式表示Na2S的水解________。
-
在100mL MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH物质的量和所得沉淀的物质的量的关系如图所示。回答下列问题。
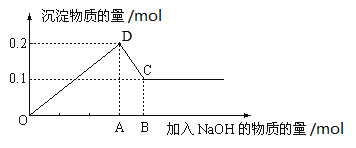
(1)图中CD段反应的化学方程式为___________;C点存在的固体物质为________。
(2)A点的数据为_______;混合液中,MgCl2的浓度为_______。
-
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验操作、现象、结论或解释正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 向Na2S溶液中滴加盐酸 | 有臭鸡蛋气味的气体产生 | 氯的非金属性比硫的强 |
| B | 向Ba(NO3)2溶液中通入SO2气体 | 产生白色沉淀 | 沉淀是BaSO3 |
| C | 将0.1mol/L ZnSO4溶液加入1mol/LNa2S溶液至不再有沉淀产生,再滴加0.1mol/L CuSO4溶液 | 先有白色沉淀生成后变为黑色沉淀 | Ksp(CuS) > Ksp(ZnS) |
| D | 向某溶液中滴加K 3[Fe(CN)6] (铁氰化钾) 溶液 | 有蓝色沉淀产生 | 该溶液中一定含有Fe2+ |
A. A B. B C. C D. D
-
盐在化学工业中有重要的应用,请回答下列问题
(1)用离子方程式表示FeCl3可作净水剂的原因:___________________ 。
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为_____ , 向Na2S溶液中加入AlCl3溶液时,产生白色沉淀和有臭鸡蛋味的气体,其离子方程式为:_________________。
(3)c(NH4+)相等的下列溶液① NH4Cl ②NH4HSO4 ③(NH4)2SO4 ④CH3COONH4
⑤NH3 H2O,溶液的物质的量浓度由小到大的顺序是__________ (用序号表示)
(4)已知t ℃时AgCl的Ksp=2×10-10 ;(2)在t ℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列正确的是 _______
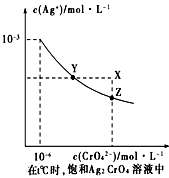
A.在t ℃时,Ag2CrO4的Ksp为1×10-9
B.t ℃时,在饱和Ag2CrO4溶液中加入K2CrO4 可使溶液由Y点到X点
C.在t ℃时,以0.01mol/L AgNO3溶液滴定20mL0.01 mol/L KCl和0.01 mol/L的K2CrO4的混合溶液,Cl-先沉淀
D.在t ℃时,AgCl的溶解度大于Ag2CrO4
(5)已知某温度时:Ksp[Fe(OH)3]=1×10-38,Ksp[Cu(OH)2]=1×10-20。在该温度下向Fe3+、Cu2+均为0.01mol•L-1的溶液中逐滴加入NaOH溶液,要Fe3+完全沉淀,而Cu2+不产生沉淀,溶液中PH应控制的范围是_______。(当离子浓度小于1×10-5mol/L时,认为完全沉淀)。
-
下列事实不能用勒夏特列原理解释的是
A.将Na2S 溶液加入到含Hg2+的废水中,可生成HgS 沉淀
B.将 AlCl3 溶液加热、蒸干、灼烧,最终得到 Al2O3
C.工业合成氨选择高压而不是常压作为反应条件
D.用稀H2SO4 洗涤 BaSO4 沉淀,可减少沉淀损失量
-
下列指定反应的离子方程式正确的是
A.Na2S溶液中S2-的水【解析】
S2-+2H2O=H2S↑+2OH-
B.用石墨作电极电解NaCl溶液:2Cl-+2H+ Cl2↑+H2↑
Cl2↑+H2↑
C.AlCl3溶液中加入足量氨水:Al3++3OH-=Al(OH)3↓
D.Fe2(SO4)3溶液中加入足量Cu粉:Cu+2Fe3+=Cu2++2Fe2+
-
下列反应的离子方程式错误的是
A. H2S通入CuSO4溶液中:H2S+Cu2+==CuS↓+2H+
B. AlCl3溶液与Na2S溶液混合生成沉淀::2 Al3++3S2-==Al2S3↓
C. 用惰性电极电解BaCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D. 用TiCl4制备TiO2的第一步反应:Ti4++ (x+2) H2O(过量) TiO2·xH2O↓+ 4H+
TiO2·xH2O↓+ 4H+


