-
实验是化学的基础.某学习小组设计并进行了下述两个实验.
(1)探究KI溶液和FeCl3溶液反应存在一定的限度.
可选试剂:①0.1mol•L-1KI溶液 ②0.1mol•L-1 FeCl3溶液 ③FeCl2溶液 ④盐酸⑤KSCN溶液 ⑥CCl4
实验步骤:
①取5mL 0.1mol•L-1 KI溶液,滴加5~6滴0.1mol•L-1FeCl3溶液;
②充分反应后,将溶液分成两份;
③取其中一份,滴加CCl4,充分振荡,静置,CCl4层呈紫红色,说明反应生成碘.
④另取一份,滴加试剂______,现象______,说明______.
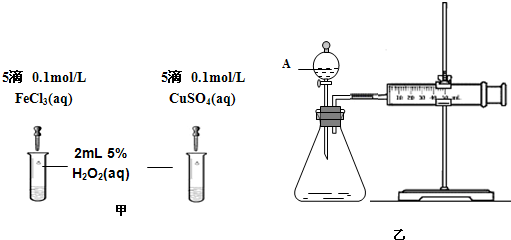
(2)为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验.请回答下列问题:
①定性分析:如图甲可通过观察______,定性比较得出结论;有同学提出将CuSO4改为CuCl2更为合理,其理由是______.
②定量分析:如图乙所示,实验时均以生成40mL气体为准,实验中需要测量的数据是______.
-
(10分)(1)某化学课外研究小组,设计实验探究KI溶液和FeCl3溶液反应存在一定的限度。已知该反应为:2Fe3+ + 2I- = 2Fe2+ + I2。请完成相关的实验步骤和现象。
可选试剂:①0. 1mol·L -1KI溶液;②0. 1mol·L -1 FeCl3溶液;③FeCl2溶液;④盐酸;⑤KSCN溶液;⑥CCl4。
实验步骤:
①取5mL 0. 1mol·L -1 KI溶液,再滴加5~6滴(约0.2ml)0. 1mol·L-1FeCl3溶液
②充分反应后,将溶液分成三份
③取其中一份,滴加试剂CCl4,用力振荡一段时间,CCl4层出现紫红色,说明反应生成碘。
④另取一份,滴加试剂________(填试剂序号),若现象为________,则说明该反应有一定的限度。
(2)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
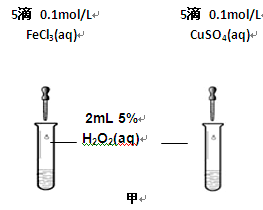
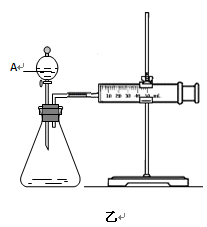
①定性分析:如图甲可通过观察________(填现象),定性比较得出结论。有同学提出将FeCl3溶液改为Fe3+浓度相同的Fe2(SO4)3溶液更为合理,其理由是。
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中一定需要测量的数据是________(填序号)。
①收集40ml气体所需要的时间 ②CuSO4溶液和FeCl3溶液的浓度 ③过氧化氢溶液的浓度
-
(1)某化学课外研究小组,设计实验探究KI溶液和FeCl3溶液反应存在一定的限度.请完成相关的实验步骤和现象.
可选试剂:①0.1mol•L-1KI溶液;②0.1mol•L-1 FeCl3溶液;③FeCl2溶液;④盐酸;⑤KSCN溶液;⑥CCl4.
实验步骤:
①取5mL 0.1mol•L-1 KI溶液,再滴加5~6滴0.1mol•L-1FeCl3溶液
②充分反应后,将溶液分成三份
③取其中一份,滴加试剂CCl4,用力振荡一段时间,CCl4层出现紫红色,说明反应生成碘.
④另取一份,滴加试剂______,现象______,说明______.
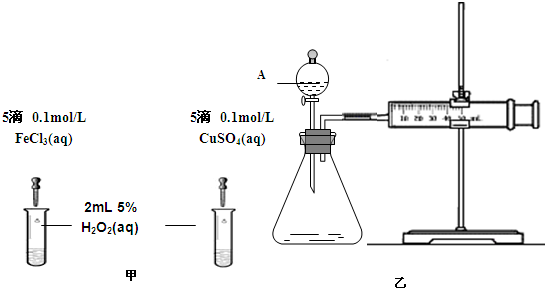
(2)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
①定性分析:如图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3 更为合理,其理由是______.
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.实验中需要测量的数据是______.
-
为了探究KI与FeCl3的反应为可逆反应,且有一定的限度,某化学小组进行了两组实验:
(1)请写出KI溶液与FeCl3溶液反应的离子反应方程式:______;
实验I:探究KI与FeCl3的反应为可逆反应
步骤1:设计如下图原电池装置,接通灵敏电流计,指针向左偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
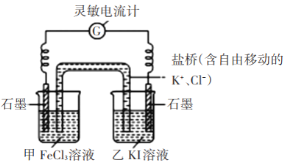
步骤2:当指针读数变零后,向甲中加入少量FeCl2固体,向乙中加入少量碘固体;
(2)若灵敏电流计出现_________(答现象),则证明该反应为可逆反应。实验结论:该反应为可逆反应。
(3)根据以上实验结论解释步骤1中“最后读数变为零”的原因_______;
(4)加入FeCl2和碘固体后,正极的电极反应式为______;
实验II:证明KI与FeCl3的反应有一定限度。
步骤3:取5 mL 0.1 mol/L的KI溶液于试管,滴加0.1 mol/L的FeCl3溶液2 mL,振荡;
步骤4:取少量反应后的溶液,向其中加入几滴淀粉溶液,充分振荡;
(5)观察到的现象是________;
步骤5:另取少量反应后的溶液,滴加0.1 mol/L的AgNO3溶液,振荡,产生黄色沉淀,则证明该反应有一定限度。
(6)但有同学认为步骤5现象不能证明得出的结论,原因是______,修正实验方案后得到结论:该反应有一定的限度。
-
实验是学习和研究化学的基础。某课外兴趣小组设计了下列装置,验证二氧化碳与过氧化钠反应时需要有水存在。
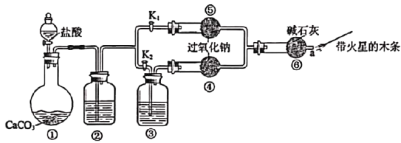
回答下列问题:
I.二氧化碳的制备及纯化:
(1)装置①中反应的离子方程式是___。
(2)装置②中的试剂是___;装置③中的试剂是___。
II.实验验证:
步骤1:打开阀门K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开阀门K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是___。
(4)过氧化钠与二氧化碳反应的化学方程式为___。
III.实验反思:
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠与二氧化碳发生了化学反应。”其理由是___。
-
为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5 mL 0.5 mol•L-1 KI溶液,滴加0.1 mol•L-1 FeCl3溶液5~6滴,充分反应。下列实验操作能验证该反应是否存在限度的是( )
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察有否白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变血红色
-
为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5 mL 0.5 mol·L-1 KI溶液,滴加0.1 mol·L-1 FeCl3溶液5~6滴,充分反应。下列实验操作能验证该反应是否存在限度的是
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
-
为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5 mL 0.5 mol•L-1 KI溶液,滴加0.1 mol•L-1 FeCl3溶液5~6滴,充分反应。下列实验操作能验证该反应是否存在限度的是
A.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
B.再滴加AgNO3溶液,观察是否有黄色沉淀产生
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察有否白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变血红色
-
某同学为探究FeCl3与KI反应是否存在反应限度,设计了如下实验方案(FeC13溶液、KI溶液浓度均为0.1mo1・L-1),最合理的方案是
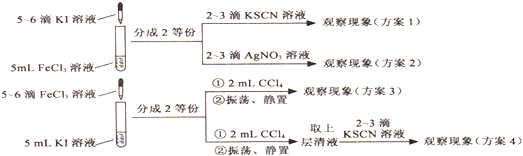
A. 方案1 B. 方案2 C. 方案3 D. 方案4
-
某研究性学习小组探究Na与CO2的反应,设计了如下装置进行探究。
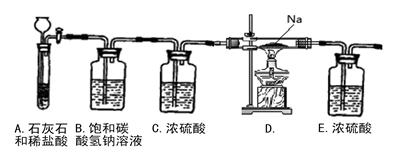
(1)从试剂瓶中取出的金属钠,须经过必要的操作,方可进行后续的实验,该必要的操作是________。该装置B中饱和碳酸氢钠溶液的作用是________,装置E中浓硫酸的作用是________
(2)放进玻璃管中的金属钠在加热之前,必须先打开活塞,通入CO2, 这样操作的原因是________
(3)用酒精灯给玻璃管加热,Na在充满CO2气体的玻璃管里剧烈地燃烧,产生大量的白烟。玻璃管中有黑色物质生成。玻璃管冷却后,玻璃管壁上附着一层白色物质。将玻璃管内物质转移至烧杯中, 加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往滤液中加CaCl2溶液,溶液变白色浑浊;再滴入稀盐酸,溶液中有气泡出现,则玻璃管壁上附着的白色物质是________。另将滤纸上的黑色物质干燥,点燃,其燃烧产物无色无味且能使澄清石灰水变浑浊,则玻璃管中的黑色物质是________。
(4)Na与CO2的反应的方程式为________







