-
已知A、B、C、D、E、F、G七种元素的原子序数依次递增,前四种元素为短周期元素
位于元素周期表s区,电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每轨道中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F位于第四周期d区,最高能级的原子轨道内只有2个未成对电子;E的一种氧化物具有磁性;C与G同主族。
(1)
基态原子的价电子轨道排图为______,B2A2的电子式为_______,CD3-的空间构型为______ .
(2)F(BD)n的中心原子价电子数与配体提供电子总数之和为18(1个BD分子可提供的电子数为2),则
______
根据等电子原理,B、D 分子内
键与
键的个数之比为______ .
(3)FXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为
,若晶体中的F分别为F2+、F3+,此晶体中F2+与F3+的最简整数比为______ .
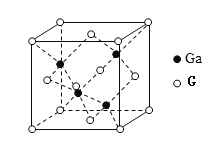
(4)G元素与Ga可形成原子晶体GaG,其晶胞结构如图所示,密度为
,Ga和G的摩尔质量分别为M1g·mol-1和M2g·mol-1原子半径分别为r1pm和r2pm,阿伏伽德罗常数值为
,则该晶胞中原子的体积占晶胞体积的百分率为______.(写出用M1、和M2、r1、r2、ρ表示的计算式)
高二化学综合题困难题查看答案及解析
-
Q、R、X、M、Y、Z是周期表前四周期的五种元素,原子序数依次递增。已知:
①Z位于ds区,最外能层有单电子,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn ,M的基态原子2p能级有1个单电子
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。回答下列问题:
(1)基态Z2+的价电子排布式是 。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的 形成配位键。
(3)Q和Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4) 写出由R、X两元素组成的与N3-互为等电子体的微粒(分子和离子各一种) 。
(5)X、M两元素形成的化合物XM2的VSEPR模型名称为 ,已知XM2分子的极性比水分子的极性弱,其原因是
高二化学填空题简单题查看答案及解析
-
Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于ds区,最外能层没有单电子,其余的均为短周期主族元素;
②Y原子价电子排布为msnmpn(m≠n);
③M的基态原子2p能级有1个单电子;
④Q、X原子p轨道的未成对电子数都是2。
用化学术语回答下列问题:
(1)Z在周期表中的位置______________。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为__________ (用对应元素的符号填写)。
(3)X、M两元素形成的化合物XM2的VSEPR模型名称为_________,已知XM2分子的极性比水分子的极性弱,其原因是__________________。
(4)分析下表中两种物质的键能数据(单位:kJ/mol)。
A—B
A=B
A≡B
QX
357.7
798.9
1 071.9
R2
154.8
418.4
941.7
①结合数据说明QX比R2活泼的原因:________________________。
②QX与R2互为等电子体,QX的结构式为(若有配位键请用→表示)______。Fe易与QX形成配合物,化学式遵循18电子规则:中心原子的价电子数加上配体提供的电子数之和等于18,则此配合物化学式为_______。
高二化学推断题困难题查看答案及解析
-
(16分)已知A、B、C、D、E、F六种元素的原子序数依次递增,都位于前四周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。F处于周期表中第9列。
(1)B、C、D三种元素的氢化物的沸点高低顺序为________,稳定性顺序为________。
(2)同时含有A、B、D三种元素的化合物M是此类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为________,B原子的杂化类型为,M能和水以任意比混溶的原因是________。
(3)C的最高价含氧酸根的空间构型为________,E的基态原子的价电子排布式为________
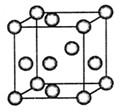
(4)“生物金属”E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图。则E晶胞中E的配位数为________,若该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,E原子的摩尔质量为M g/mol,则E原子的半径为________cm
(5)F可形成分子式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生的现象是;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为。
高二化学填空题简单题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数比为1∶1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的基态原子的外围电子排布式为___。
(2)由A、B、C形成的ABC分子中,含有___个σ键,___个π键。
(3)B、C、D三种元素的第一电离能由小到大的顺序为___。
(4)在浓的ECl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为ECl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配离子的化学式为___。
高二化学推断题中等难度题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D元素是地壳中含量最多的元素.E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同.
请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的基态原子的外围电子排布式为______.
(2)由A、B、C形成的ABC分子中,含有______个σ键,______个π键;
(3)E的一种氧化物Q,其晶胞结构如图所示,则Q的化学式为______,该晶体中氧原子的配位数为______.
(4)B、C、D三种元素的第一电离能由小到大的顺序为______.
(5)在浓的ECl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为ECl3•6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配离子的化学式为______.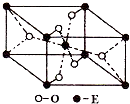
高二化学解答题中等难度题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同; D原子的核外成对电子数是未成对电子数的3倍。同时含有A、B、D三种元素的化合物M是一种居室污染气体,其分子中所有的原子共平面。A、B两种元素组成的原子个数比为1︰1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)下列叙述正确的是____________(填字母)。
A.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
B.M和二氧化碳分子中的中心原子均采用sp2杂化
C.N分子中含有6个σ键和3个π键
D.N分子中所有原子共面
(2)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水,其中Fe为+2价) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式
__________________________________,_________________________________。
(3)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别
是_______、_______。两者沸点的关系为X_____Y(填 > 或 < )。
高二化学简答题困难题查看答案及解析
-
(8分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子对数与未成对电子数之比为3:1。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
(1)D元素在元素周期表中的位置为第 周期 族。
(2)下列叙述正确的是 (填写序号)。
a.水的沸点比M高得多,是因为水分子间能形成氢键,而M分子间不能形成氢键
b.M的中心原子采用sp3杂化
c.N分子中含有6个σ键和1个大π键
d.BD2晶体的熔点、沸点都比二氧化硅晶体的低
(3)已知C2D是一种麻醉剂,根据等电子原理可推知C2D的空间构型为 。
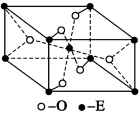
(4)E的一种氧化物Q,其晶胞结构如图所示,则Q的化学式为 。
高二化学填空题困难题查看答案及解析
-
已知A、B、C、D、M、W六种元素的原子序数依次递增,都位于前四周期。其中A、D原子的最外层电子数均等于其周期序数,且D原子的电子层数是A的3倍;B原子s轨道电子数是p轨道电子数的两倍;C原子L层上有2对成对电子。M和W均有“生物金属”之称,M4+和氩原子的核外电子排布相同;W处于元素周期表中第8列。请回答下列问题:
⑴1 mol B2A2分子中含σ键的数目是________。
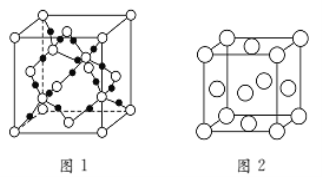
⑵BC2在高温高压下所形成的晶体其晶胞如图1所示。则该晶体的类型属于________晶体(填“分子”、“原子”);该晶体中B原子轨道的杂化类型为________。
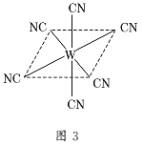
⑶“生物金属”M的晶胞如图2所示。则晶胞中一个M原子与_____个M原子紧邻;若该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NAmol-1,M原子的摩尔质量为Mrg·mol-1,则该晶胞的“边长”为________cm。
⑷“生物金属”W元素应用广泛,如人体内W元素的含量偏低,则会影响O2在体内的正常运输。已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图3所示。
①W元素基态原子价电子排布式为________。
②1个CN-中π键数目为________。
⑸光谱证实单质D与强碱溶液反应有[D(OH)4]-生成,则[D(OH)4]-中存在________(填字母)。
a 共价键 b 配位键 c σ键 d π键
高二化学综合题中等难度题查看答案及解析
-
(14分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A元素不与B、C、D三种元素同周期,且原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体;A、B二种元素组成的原子个数比为1︰1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。
请回答下列问题:(答题过程中涉及到A、B、C、D、E元素时,用所对应的元素符号表示)
(1)B、C、D三种元素的第一电离能由小到大的顺序为___________________;BD2的结构式为___________________;A3D+离子的VSEPR模型为___________________;B、C的气态氢化物分子中,键角的大小关系为B_____C(填“>、= 或 <”)。
(2)E元素在元素周期表分区中属于_______区元素,该元素基态原子的外围电子排布式为________。
(3)下列叙述正确的是________。(填字母)
A.A元素位于元素周期表的s区,且在元素周期表的所有元素中电负性最小
B.M和N分子中的B原子均采用sp2杂化
C.N分子中含有6个σ键和1个π键
D.BA4为最简单的有机物
(4)某离子化合物R的化学式为CA5 ,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,则R的电子式为____________。
(5)在浓的ECl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6 ,组成为ECl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1︰5,则该配离子的化学式为________。
高二化学填空题简单题查看答案及解析