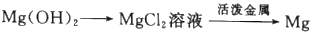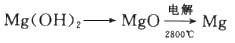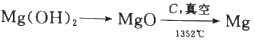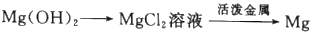-
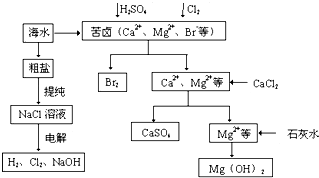
工业上对海水资源综合开发利用的部分工艺流程如图所示.
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性.请写出加入Na2CO3溶液后相关化学反应的离子方程式:______、______.
(2)从海水中提取溴,主要反应为2Br-+Cl2=Br2+2Cl-,下列说法错误的是______(填序号).
A.溴离子具有氧化性 B.氯气是还原剂
C.该反应属于复分解反应 D.Br2是氧化产物
(3)本工艺流程中先后制得Br2、CaSO4、Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备?______(填“能”或“否”),原因是______.
-
(10分)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
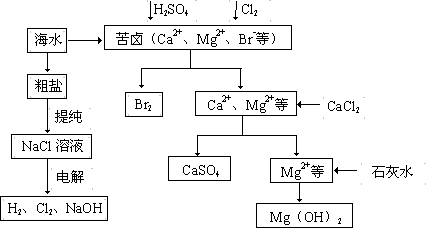
⑴ 粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出加入Na2CO3溶液后相关化学反应的离子方程式:
________、________。
⑵ 从海水中提取溴,主要反应为2Br- + Cl2 = Br2 + 2Cl-,下列说法错误的是________(填序号)。
A. 溴离子具有氧化性 B. 氯气是还原剂
C. 该反应属于复分解反应 D. Br2是氧化产物
⑶ 本工艺流程中先后制得Br2、CaSO4、Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备?
________(填“能”或“否”),原因是________。
-
海洋是巨大的资源宝库,下面是海水资源综合利用的部分流程图。
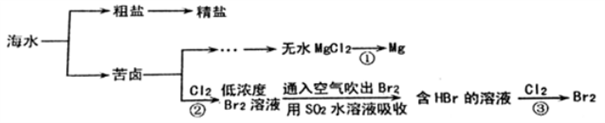
(1)从海水中获得粗盐的方法是____________________。
(2)粗盐中含有Ca2+、Mg2+、SO42- 等杂质离子,制取精盐的过程中需依次除去这些离子,所加除杂试剂依次是氢氧化钠溶液、_________________和________________。
(3)①中反应的化学方程式是________________。
(4)③中反应的离子方程式是________________________,生成1molBr2转移电子________mol。
(5)由以上过程可知,Cl2、SO2、Br2的氧化性由强到弱的顺序是________________。
-
海水中有取之不尽的化学资源,从海水中可提取多种化工原料。如图是某工厂综合利用海水资源的示意图。
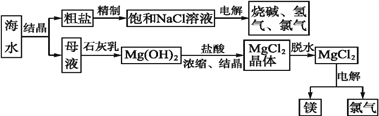
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得饱和NaCl溶液。精制过程中所用试剂有a、BaCl2溶液、b、Na2CO3溶液、c、 NaOH溶液、d、盐酸。加入试剂顺序正确的是____________;
A、a.b.c.d B、c.b.a.d C、b.a.d.c D、a.c.b.d
(2)写出电解饱和食盐水方程式________________________________________,产生的Cl2和烧碱反应能生成____________(填商品名称),反应方程式________。
(3)海水中提取食盐后的母液中含有K+、Na+、Mg2+等。从离子反应的角度考虑,向母液中加入石灰乳的作用是_________________________。
(4)电解熔融的氯化镁所得的镁蒸气冷却后即为固体镁,可以冷却镁蒸气的气体氛围为_____。
A.H2 B.CO2 C.空气 D.Ar
-
海水是巨大的资源宝库,海水开发利用的部分过程如图所示。

(1)操作1的名称是____,进行该操作时所需的玻璃仪器为烧杯、____;
(2)上述流程所得粗盐中含有的少量Ca2+、Mg2+、SO42-等杂质离子常用①Na2CO3溶液②BaCl2溶液③NaOH溶液④稀盐酸来进行除去,试剂的加入顺序为③____(填试剂序号);
(3)上述流程所得苦卤中通入Cl2后的溶液中溴的浓度极低,所以工业上一般要向该溶液中通入热空气,吹出的溴蒸气用二氧化硫水溶液吸收,再向吸收液中通入氯气得到较高浓度的溴水,写出溴与二氧化硫水溶液反应的化学方程式____________。
-
海水中含有非常丰富的化学资源,从海水中可提取多种化工原料.下图是某化工厂对海水资源综合利用的示意图.(注:母液中含有Mg2+)
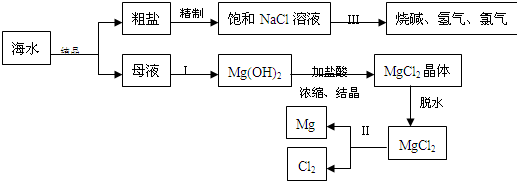
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得饱和NaCl溶液,精制时通常在溶液中加入以下物质,最后使溶液呈中性.
①过量的Na2CO3溶液、②盐酸、③过量的NaOH溶液、④过量的BaCl2溶液则,加入的顺序是______.
(2)写出加入最后一种试剂后可能发生的化学反应的离子方程式______、______.
(3)①写出反应Ⅱ的化学方程式______ Mg+Cl2↑
-
海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
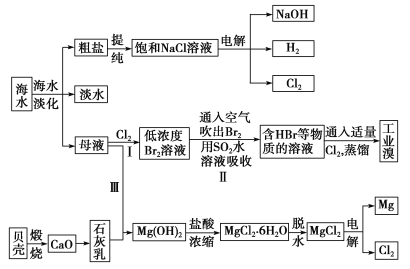
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是________(填编号)。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_____________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_______________________。
(3)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入MgCl2溶液,充分搅拌后经________(填操作方法)可得纯净的Mg(OH)2。
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________(填字母)。
A.H2 B.CO2 C.N2 D.O2 E.水蒸气
-
根据如图海水综合利用的工业流程图,判断下列说法正确的是

A. 除去粗盐中杂质Mg2+、SO42-、Ca2+,加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. 从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
C. 从第③步到第⑤步的目的是为了浓缩
D. 在过程④中SO2被氧化
-
海水中有取之不尽的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源的综合利用的示意图。
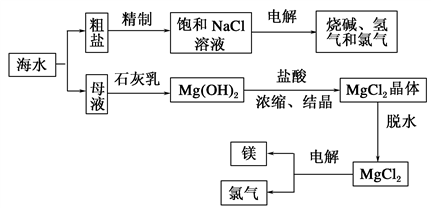
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
①粗盐溶液中加入过量的Na2CO3溶液:____________________;_____________________。
②滤液中加入盐酸至溶液呈中性:________________________;_______________________。
(2) 母液中含有K+、Na+、Mg2+等阳离子,从以上流程可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是_____________________;若加入石灰乳后所制取的产品中还混杂着熟石灰,那么将熟石灰从该产品中除去的方法是________________________。
②电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是________(填字母序号)。
A.H2 B.CO2 C.O2 D.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新的母液中加入一种常见的气态氧化剂,又抽取了重要的化工原料溴单质。
①生成溴单质的化学反应的离子方程式是___________________________________;生产中利用溴单质的挥发性将溴单质从化合物中分离出来的方法是________________________。
②以下是对生产溴单质所用的气态氧化剂寻找供货源的设想,其中合理的是_________(填字母序号)。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
③从多种经营、综合开发、打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是_________________________________。
-
海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
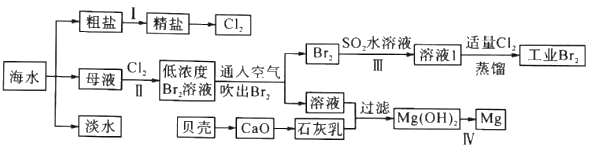
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________、_________。
(2)步骤Ⅱ中已获得Br2,步骤Ⅲ中又将Br2还原为Br-,其目的是_________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A. 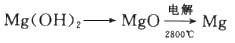
B.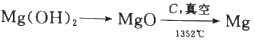
C.
D.