A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H++O2+4e-=2H2O
D.电池工作时,1mol二甲醚被氧化时就有6mol电子转移
高三化学选择题中等难度题

高三化学选择题中等难度题
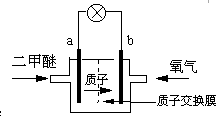
日本茨城大学研制了一种新型的质子交换膜二甲醚燃料电池(DDFC),该电池有较高的安全性。电池总反应为:CH3OCH3 +3O2 =2CO2 +3H2O , 电池示意如图,下列说法不正确的是:
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H+ + O2 + 4e- = 2H2O
D.电池工作时,1mol二甲醚被氧化时就有6mol电子转移
高三化学选择题中等难度题查看答案及解析

高三化学选择题中等难度题查看答案及解析
下图是一种新型的质子交换膜二甲醚燃料电池(DDFC)。电池总反应为:CH3OCH3+3O2=2CO2+3H2O,下列说法不正确的是
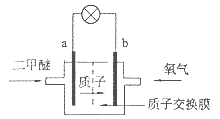
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H++O2+4e-=2H2O
D.电池工作时,1 mol二甲醚被氧化时就有6 mol电子转移
高三化学选择题中等难度题查看答案及解析
二甲醚(CH3OCH3)燃料电池的工作原理如右图,有关叙述正确的是

A. 该装置能实现化学能100%转化为电能
B. 电子移动方向为:a极→b极→质子交换膜→a极
C. a电极的电极反应式为:CH3OCH3+3H2O=2CO2+12e-+12H+
D. 当b电极消耗22.4LO2时,质子交換膜有4moIH+通过
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200oC左右供电。电池总反应为:C2H5OH+3O2→2CO2+3H2O,右图是该电池的示意图,下列说法正确的是
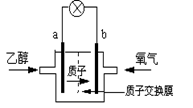
A.a极为电池的正极
B.电池工作时电流由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
高三化学选择题中等难度题查看答案及解析
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200oC左右供电。电池总反应为:C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是
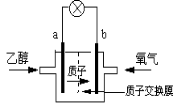
A.a极为电池的正极
B.电池工作时电流由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
高三化学选择题中等难度题查看答案及解析
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:
C2H5OH +3O2 =2CO2 +3H2O,电池示意如图,下列说法不正确的是

A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H+ + O2 + 4e- =2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
高三化学选择题中等难度题查看答案及解析
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。
(1) 写出甲醚燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)== 2CH3OCH3(g)的反应热为 ;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g)CH3OCH3(g)+ 3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是 (选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将 (填“变大”、“变小”或“不变”)。
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式的其中一个产物是CO32-,请写出该反应的负极反应式 ;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500 mL NaCl溶液,装置如图所示:
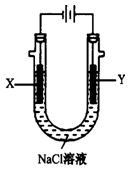
请写出电解过程中Y电极附近观察到的现象是 ;当燃料电池消耗2.8 LO2(标准状况下)时,计算此时:NaCl溶液的pH= (假设溶液的体积不变,气体全部从溶液中逸出)。
高三化学填空题简单题查看答案及解析
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。
(1)写出甲醚燃烧的热化学方程式________________________________________;已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)= 2CH3OCH3(g)的反应热为_______________________;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g)CH3OCH3(g)+ 3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是______(选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将_____________ (填“变大”、“变小”或“不变”)。
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池负极反应式的其中一个产物是CO32-,请写出该反应的负极反应式__________________;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500 mL NaCl溶液,装置如图所示:
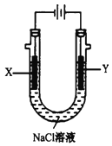
请写出电解过程中Y电极附近观察到的现象是_______________________;当燃料电池消耗2.8 LO2(标准状况下)时,计算此时:NaCl溶液的pH=_______________________(假设溶液的体积不变,气体全部从溶液中逸出)。
高三化学填空题简单题查看答案及解析