-
下列有关热化学方程式的评价合理的是( )
实验事实
热化学方程式
评价
A
已知H+(aq)+OH-(aq)===H2O(l) ΔH=
-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合
H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+2H2O(l)
ΔH=-114.6 kJ·mol-1
正确
B
醋酸与稀氢氧化钠溶液混合
CH3COOH(l)+NaOH(aq)===CH3COONa(aq)+H2O(l)
ΔH=-57.3 kJ·mol-1
不正确;因为醋酸状态为“aq”,而不是“l”
C
160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ
SO3(g)+H2O(l)===H2SO4(aq) ΔH=-130.3 kJ·mol-1
不正确;因为反应热为ΔH=-260.6 kJ·mol-1
D
已知25 ℃、101 kPa下,120 g石墨完全燃烧放出热量3 935.1 kJ
C(s)+O2(g)===CO2(g)
ΔH=-393.51 kJ·mol-1
不正确;同素异形体要注名称:C(石墨)
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
下列有关热化学方程式的评价合理的是( )
实验事实
热化学方程式
评价
A
已知H+(aq)+OH-(aq)===H2O(l) ΔH=
-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合
H2SO4(aq)+Ba(OH)2(aq)
===BaSO4(s)+2H2O(l)
ΔH=-114.6 kJ·mol-1
正确
B
已知25 ℃、101 kPa下,120 g石墨完全燃烧放出热量3 935.1 kJ
C(s)+O2(g)===CO2(g)
ΔH=-393.51 kJ·mol-1
不正确;同素异形体要注名称:
C(石墨,s)
C
160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ
SO3(g)+H2O(l)===
H2SO4(aq)
ΔH=-130.3 kJ·mol-1
不正确;因为反应热为ΔH=-260.6 kJ·mol-1
D
醋酸与稀氢氧化钠溶液混合
CH3COOH(l)+NaOH(aq)
===CH3COONa(aq)+H2O(l)
ΔH=-57.3 kJ·mol-1
不正确;因为醋酸状态为“aq”,而不是“l”
A. A B. B C. C D. D
高二化学选择题中等难度题查看答案及解析
-
下列有关热化学方程式的评价合理的是
实验事实
热化学方程式
评价
A
已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合
H2SO4(aq)+Ba(OH)2(aq)= BaSO4(s)+ 2H2O(l)
△H=-114.6 kJ·mol-1
正确
B
醋酸与稀氢氧化钠溶液混合
CH3COOH(aq)+NaOH(aq)=NaCl(aq)+H2O(l)
△H=-57.3kJ·mol-1
不正确;因为醋酸状态为“aq”,而不是“l”。
C
160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ
SO3(g)+H2O(l)=H2SO4(aq) △H=-130.3 kJ·mol-1
不正确;因为反应热为△H=-260.6 kJ·mol-1
D
已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ
C(s)+O2(g)=CO2(g)
△H=-393.51 kJ·mol-1
不正确;同素异形体要注名称:C(石墨)
高二化学选择题中等难度题查看答案及解析
-
下列有关热化学方程式的评价合理的是( )
实验事实 热化学方程式 评价 A 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1,将稀硫酸与 稀氢氧化钡溶液混合 H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)
△H=-114.6 kJ•mol-1
正确B 稀醋酸与稀氢氧化钠溶液混合 CH3COOH(aq)+NaOH(aq)=NaCl(aq)+H2O(l)
△H=-57.3k J•mol-1不正确;因为醋酸状态为“l”,而不是“aq”. C 160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ SO3(g)+H2O(l)=H2SO4(aq)△H=-130.3 kJ•mol-1 不正确;因为反应热为△H=-260.6 kJ•mol-1 D 已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ C(s)+O2(g)=CO2(g)
△H=-393.51 kJ•mol-1不正确;同素异形体要注名称:C(石墨,S)
A.A
B.B
C.C
D.D高二化学选择题中等难度题查看答案及解析
-
下列有关热化学方程式的评价合理的是( )
实验事实
热化学方程式
评价
A
已知H+(aq)+OH-(aq)=H2O(l)
△H=-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合
H2SO4(aq)+Ba(OH)2(aq)
=BaSO4(s)+ 2H2O(l)
△H=-114.6 kJ·mol-1
正确
B
醋酸与稀氢氧化钠溶液混合
CH3COOH(aq)+NaOH(aq)
=CH3COONa(aq)+H2O(l)
△H=-57.3kJ·mol-1
不正确;因为醋酸状态为“aq”,而不是“l”。
C
160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ
SO3(g)+H2O(l)=H2SO4(aq) △H=-130.3 kJ·mol-1
不正确;因为反应热为△H=-260.6kJ·mol-1
D
已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ
C(s)+O2(g)=CO2(g)
△H=-393.51 kJ·mol-1
不正确;同素异形体要注名称:C(石墨)
高二化学选择题中等难度题查看答案及解析
-
下列有关热化学方程式的评价合理的是
实验事实
热化学方程式
评价
A
已知H+(aq)+OH-(aq)= H2O(l) △H=-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合
H2SO4(aq)+Ba(OH)2(aq)= BaSO4(s)+ 2H2O(l)
△H=-114.6 kJ·mol-1
正确
B
醋酸与稀氢氧化钠溶液混合
CH3COOH(aq)+NaOH(aq)=NaCl(aq)+H2O(l)
△H=-57.3kJ·mol-1
不正确;因为醋酸状态为“aq”,而不是“l”。
C
160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ
SO3(g)+H2O(l)=H2SO4(aq) △H=-130.3 kJ·mol-1
不正确;因为反应热为△H=-260.6 kJ·mol-1
D
已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ
C(s)+O2(g)=CO2(g)
△H=-393.51 kJ·mol-1
不正确;同素异形体要注名称:C(石墨)
高二化学选择题简单题查看答案及解析
-
下列有关热化学方程式的评价合理的是( )
选项
实验事实
热化学方程式
评价
A
若H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,将稀硫酸和NaOH溶液混合
H2SO4(aq)+2NaOH(aq)=== Na2SO4(aq)+2H2O(l)
ΔH=-57.3 kJ·mol-1
正确
B
醋酸和稀NaOH溶液混合
CH3COOH(aq)+NaOH(aq)===
CH3COONa(aq)+H2O(l)
ΔH=-57.3 kJ·mol-1
不正确,因为醋酸的状态为“l”,而不是“aq”
C
160 g SO3气体与足量液体水反应生成H2SO4放出热量260.6 kJ
SO3(g)+H2O(l)===H2SO4(aq)
ΔH=-130.3 kJ·mol-1
不正确:因为反应热ΔH=-260.6kJ·mol-1
D
1 mol C8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出534 kJ的热量
2C8H18(l)+25O2(g)===16CO2(g)+18H2O(l)
ΔH=-1 068 kJ·mol-1
正确
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
(1)事实证明,原电池中发生的反应通常是放热反应。利用下列化学反应可以设计成原电池的是 。
A.C(s)+H2O(g)
CO(g)+H2(g) ΔH>0
B.NaOH(aq)+HCl(aq)
NaCl(aq)+H2O(l) ΔH<0
C.2H2(g) +O2(g)
2H2O(l) ΔH<0
D.CaCO3(s)+2HCl(aq)
CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
E.CH4(g)+2O2(g)
CO2(g)+2H2O(l) ΔH<0
(2)有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等物质的量浓度的盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出。据此判断A、B、C、D的活动性由强到弱的顺序是 。
高二化学填空题中等难度题查看答案及解析
-
下表中有关离子方程式的评价合理的是( )
选项 化学反应及离子方程式 评价
A AlCl3溶液中加入过量氨水:
Al3++3NH3·H2O=Al(OH)3¯+3NH4+ 错误,铝元素的产物应该是AlO2﹣
B 过量氯气通入溴化亚铁溶液中:
3Cl2+2Fe2++4Br- =6Cl- +2Fe3++2Br2 正确
C 用氨水吸收过量二氧化硫:
2NH3·H2O+SO2=2NH4++SO32-十H2O 正确
D 氯化铵溶于水:
NH4+ + 2H2O == H3O+ + NH3·H2O 错误,氯化铵溶解于水是物理变化,不能写离子方程式
高二化学选择题困难题查看答案及解析
-
下列有关中和热概念、中和热测定实验(如图)的说法正确的是
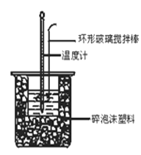
A.已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有
H2SO4(aq)+
Ba(OH)2(aq)=
BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
B.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ·mol-1,则该反应的中和热为114.6 kJ·mol-1。
C.中和热测定实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.酸碱混合时,量筒中的NaOH溶液应分多次倒入已装有盐酸的小烧杯中,并不断用环形玻璃搅拌棒搅拌。
高二化学单选题简单题查看答案及解析