-
下列说法不正确的是( )
A.化学反应的实质是旧键的断裂,同时新键的生成
B.CH4、CF4、CCl4、CBr4熔、沸点逐渐升高,原因是分子间作用力逐渐增大
C.NH3和H2O间可以形成氢键,这也是氨极易溶于水的原因之一
D.NH5中含有离子键、极性键、非极性键
高一化学单选题简单题查看答案及解析
-
下列说法不正确的是( )
A.化学反应的实质是旧键的断裂,新键的生成
B.CH4、CF4、CCl4、CBr4 熔、沸点逐渐升高,原因是分子间作用力逐渐增大
C.NH3 和 H2O 分子间都可以形成氢键
D.NH4H 是离子化合物,其含有离子键、极性键、非极性键
高一化学单选题中等难度题查看答案及解析
-
下列说法不正确的是( )
A. 化学反应的实质是旧键的断裂,新键的生成
B. CH4、CF4、CCl4、CBr4熔沸点逐渐升高,原因是分子间作用力逐渐增大
C. NH3和H2O间可以形成氢键,这也是氨极易溶于水的原因之一
D. NH4H中含有离子键、极性键、非极性键
高一化学单选题简单题查看答案及解析
-
下列说法不正确的是
A. 化学反应的实质是旧键的断裂,新键的生成
B. CH4、CF4、CCl4、CBr4熔沸点逐渐升高,原因是分子间作用力逐渐增大
C. NH3和H2O间可以形成氢键,这也是氨极易溶于水的原因之一
D. NH4Cl中含有离子键、极性键、非极性键
高一化学单选题简单题查看答案及解析
-
下列说法不正确的是( )
A.化学反应的实质是旧键的断裂,新键的生成
B.CH4、CF4、CCl4、CBr4熔沸点逐渐升高,原因是分子间作用力逐渐增大
C.NH3和H2O间可以形成氢键,这也是氨极易溶于水的原因之一
D.NH4H中含有离子键、极性键、非极性键
高一化学单选题简单题查看答案及解析
-
下列各组物质中,按熔点由低到高排列正确的是( )
A. O2、I2、Hg B. CBr4、CCl4、CF4
C. CO2、KCl、SiO2 D. SiC、NaCl、SO2
高一化学选择题中等难度题查看答案及解析
-
在化学反应中,反应物转化成生成物,必然发生能量的变化。
(1)下列说法正确的是 。
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然发生能量的变化
B.所有的放热反应都能设计成一个原电池
C.放热反应发生时不一定要加热,但吸热反应必须要加热才能发生
D.可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应不再进行
(2)25 ℃、101 kPa条件下,16g液态N2H4与双氧水充分反应生成氮气和气态水放出320.8 kJ热量,写出热化学方程式 。
(3)101 kPa条件下,氮气和氢气反应生成氨气的能量变化如下图示意:
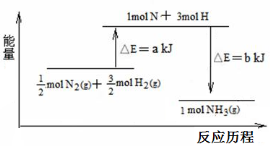
又已知:①b=1219;
②25 ℃、101 kPa下N2 (g)+3H2 (g)
2 NH3 (g)△H =-184 kJ·mol-1 ,则a= 。
高一化学简答题极难题查看答案及解析
-
下面有关物质熔点的排序不正确的是( )
A. CF4<CCl4<CBr4<CI4 B. 正戊烷>异戊烷>新戊烷
C. 金刚石>纯铁>生铁>干冰 D. 金刚石>二氧化硅>碳化硅>晶体硅
高一化学单选题中等难度题查看答案及解析
-
(1)下列说法正确的是
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁生锈腐蚀时,铁被氧化
C.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在 101 kPa 时,2g H2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为 ;
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)
CH3OH(g) +H2O(g);
下图表示该反应进行过程中能量的变化。(单位为:kJ·mol-1)该反应是 (填“吸热”或“放热”)反应。ΔH 0(填“>”或“<”)。
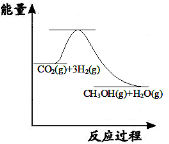
(4)比较下面各组热化学方程式,ΔH1<ΔH2的是 。
A.2H2(g)+O2(g)=2H2O(g)ΔH1;2H2(g)+O2(g)=2H2O(1)ΔH2
B.S(g)+O2(g)=SO2(g)ΔH1;S(s)+O2(g)=SO2(g)ΔH2
C.C(s)+1/2O2(g)=CO(g)ΔH1;C(s)+O2(g)=CO2(g)ΔH2
D.H2(g)+Cl2(g)=2HCl(g)ΔH1;1/2H2(g)+1/2Cl2(g)=HCl(g)ΔH2
(5)101 kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图示意:
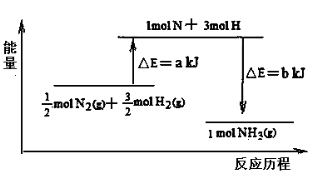
又已知:①已知b=1173;②25 ℃、101 kPa下N2(g)+3H2 (g)
2 NH3 (g) ΔH =-92 kJ·mol-1则a = 。
高一化学填空题中等难度题查看答案及解析
-
(共11分)(1)下列说法正确的是
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁的电化腐蚀中,吸氧腐蚀和析氢腐蚀的负极反应都为:Fe-2e- = Fe2+
C.可逆反应在一定条件下,有一定的限度,当反应进行到最大限度后,反应物就不再转化为生成物
D.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在 101 kPa 时,2g H2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为 ;
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)
CH3OH(g) +H2O(g);
下图表示该反应进行过程中能量的变化。(单位为:kJ·mol-1)该反应是 (填“吸热”或“放热”)反应。△H 0(填“>”或“<”)。
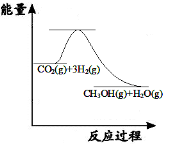
(4)比较下面各组热化学方程式,△H1<△H2的是 (即前一反应放热较多的是) 。
A.2H2(g) + O2(g) = 2H2O(g ) △H1 2H2(g) + O2(g) = 2H2O(1) △H2
B.S(g) + O2(g) = SO2(g ) △H1 S(s) + O2(g) = SO2(g ) △H2
C.C(s) + 1/2O2(g) =CO (g ) △H1 C(s) +O2(g) =CO2 (g ) △H2
D.H2(g) + Cl2(g) =2HCl(g ) △H1 1/2H2(g) +1/2 Cl2(g) =HCl(g ) △H2
(5)101 kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图示意:

又已知:①已知b=1173;
②25 ℃、101 kPa下N2(g)+3H2 (g)
2 NH3 (g) △H =-92 kJ·mol-1
则a = 。
高一化学简答题极难题查看答案及解析