取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是

A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
高三化学选择题中等难度题
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是

A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
高三化学选择题中等难度题
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是

A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
高三化学选择题中等难度题查看答案及解析
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是
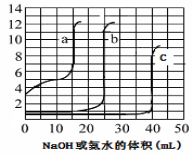
A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
高三化学选择题困难题查看答案及解析
(7分)实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。请完成下列填空:
取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
| 实验 编号 | NaOH溶液的浓度 (mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
| 1 | 0.10 | 22.50 | 20.00 |
| 2 | 0.10 | 25.80 | 20.00 |
| 3 | 0.10 | 22.62 | 20.00 |
(1)滴定达到终点的标志是 。
(2)根据上述数据,可计算出该盐酸的浓度约为______________(保留两位有效数字)。
(3)排去碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
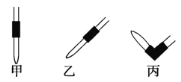
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______(填选项字母)。
A.滴定终点读数时俯视
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
高三化学实验题中等难度题查看答案及解析
在25 ℃时,用0.125 mol·L-1的标准盐酸溶液滴定25.00 mL未知浓度的NaOH溶液所得滴定曲线如图所示,图中K点代表的pH为( )

A.13 B.12 C.10 D.11
高三化学选择题中等难度题查看答案及解析
在25 ℃时,用0.125 mol/L的标准盐酸滴定25.00 mL未知浓度的NaOH溶液所得滴定曲线如图所示,图中K点代表的pH为

A.13 B.12 C.10 D.11
高三化学选择题中等难度题查看答案及解析
已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
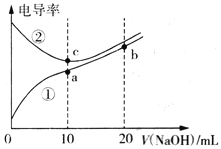
A. 曲线①代表滴定盐酸的曲线
B. 滴定醋酸的过程应该选择甲基橙作为指示剂
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
高三化学单选题困难题查看答案及解析
已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线①代表滴定盐酸的曲线
B. 滴定醋酸的过程应该选择甲基橙作为指示剂
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
高三化学单选题困难题查看答案及解析
用标准盐酸溶液滴定未知浓度的NaOH溶液,所测数据如下:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.20 | 20.22 |
| 第二次 | 25.00 | 0.56 | 24.54 |
| 第三次 | 25.00 | 0.42 | 20.40 |
测得NaOH溶液的物质的量浓度为
A.0.0853mol/L B.0.1000mol/L C.0.0800mol/L D.0.1250mol/L
高三化学单选题中等难度题查看答案及解析
(8分)
Ⅰ.醋酸是常见的弱酸。用0.1 mol•L—1NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol•L—1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH体积而变化的两条滴定曲线。
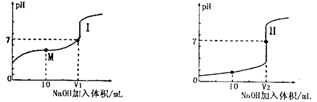
(1)滴定醋酸的曲线是 (填“I”或“Ⅱ”)。
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的溶液名称是 。
(3)V1和V2的关系:V1 V2(填“>”、“=”或“<”)
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
Ⅱ.草酸钴是制备钴的氧化物的重要原料。下图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。

(1)通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225 ℃~300 ℃发生反应的化学方程式: 。
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比 。
高三化学填空题极难题查看答案及解析
室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,
下列说法正确的是
A.起始时盐酸和醋酸溶液PH相同
B.V(NaOH)=10.00 mL 时,<1
C.pH=7时,两种酸所用NaOH溶液体积不相等,醋酸用的体积多
D.V(NaOH)=20 .00 mL 时,c(Cl‾)>c(CH3COO—)
高三化学选择题中等难度题查看答案及解析