-
乙酸是一种重要的有机原料,在化工生产和生活中有广泛的用途。某小组组装下列装置由乙醇、冰醋酸和浓硫酸为原料制备乙酸乙酯,回答下列问题。
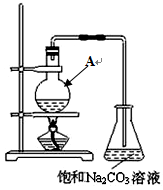
(1)仪器A的名称是 。往仪器A中加入原料的正确顺序及操作是 。
(2)在仪器A中生成乙酸乙酯的化学反应方程式为 。
(3)欲提高乙酸的转化率,可采取的措施有 、 等。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子(H+)液体可用作该反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 |
| 反应温度/℃ | 转化率 (%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性 (%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 |
| | | | | |
根据表中数据,下列 (填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
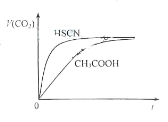
(5)常温下,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,由图分析:反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是 ,反应结束后所得两溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)。
(6)设计一个简单的实验证明醋酸是弱酸 。
-
(15分)乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为 。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯

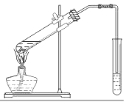
某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是 。
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止 。
③相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
根据上表数据有同学提出可用水替代小试管中的Na2CO3溶液,你认为可行吗?说明理由: 。④分离小试管中的乙酸乙酯应使用的仪器名称是________ ________________________________________;
⑤分离时,乙酸乙酯应该从仪器________________ ________________________________________________(填“下口放” 或“上口倒出”)。
⑥兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |
表中数据X的范围是________________________ ________________________________;实验a与实验e探究的目的是________________________ ________ 。
-
下列有关实验原理或操作正确的是
A.选择合适的试剂,用图1所示装置可分别制取少量


B.制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并虑干
D.用广泛 试纸测得
试纸测得 溶液的
溶液的
-
下列有关实验原理或操作正确的是
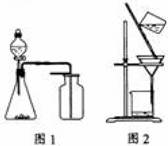 A.选择合适的试剂,用图1所示装置可分别制取少量
A.选择合适的试剂,用图1所示装置可分别制取少量
B.制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干
D.用广泛 试纸测得0.10mol·L
试纸测得0.10mol·L NH4Cl溶液的
NH4Cl溶液的
-
有机酸种类繁多,广泛分布于中草葯的叶、根、特别是果实中,是有机合成、工农业生产的重要原料,请回答下列有关问题:
(1)乙酸是合成乙酸乙酯的重要原料,制备原理如下:
CH3COOH(l)+ C2H5OH(l) CH3COOHC2H5(l)+H2O(l) △H=-8.62kJ/mol
CH3COOHC2H5(l)+H2O(l) △H=-8.62kJ/mol
已知:CH3COOH、C2H5OH和CH3COOC2H5的沸点依次为118℃、78 ℃和77℃。在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示:
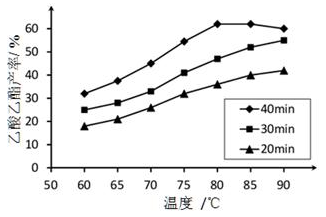
①该研究小组的实验目的是________________。60℃下反应40min与70℃下反应20min相比,前者的平均反应速率___________后者(填“小于”、“等于”或“大于”)。
②如图所示,反应时间为40min、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________;
③利用此原理制得的乙酸乙酯粗品中常含有一定量的乙酸、乙醇以及微量的硫酸,提纯时可向粗品中加入__________溶液进行充分洗涤,分离出有机层,并加入无水硫酸钠干燥,最后经过__________、_______两步操作即可得到纯品。
(2)乙二酸俗名草酸(二元弱酸,结构简式:HOOC—COOH),被广泛的应用于抗生素类药物的合成。
①实验室中经常利用酸性KMnO4溶液滴定法测其纯度。已知草酸与酸性KMnO4溶液反应过程有无色无味气体产生,且KMnO4溶液紫色褪去,写出草酸与酸性KMnO4溶液反应的离子方程式_____________________;
②资料表明:25℃时草酸的电离平衡常数Ka1=6.0×10-2;Ka2=6.4×10-5;据此分析,室温时草酸氢钾(KHC2O4)的水解反应平衡常数Kh=________(单位省略,计算结果保留两位有效数字),其溶液中c(H2C2O4)________c(C2O42-)(填“小于”、“等于”或“大于”)。
-
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。
(1)写出实验室制备乙酸乙酯的化学方程式____________。
(2)乙醇、乙酸和浓硫酸的加入顺序是___________。
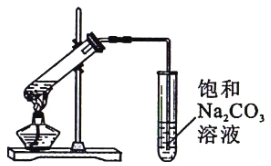
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
| 实验编号 | 试管I中的试剂 | 试管II中的试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL18mo/L浓硫酸 | | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 饱和碳酸钠溶液 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL3mol/L硫酸 | | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | | 1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_____mL和_____mol/L。
②分析实验_______(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是___________。
(4)饱和碳酸钠溶液的作用是溶解没有反应的乙醇,除去没有反应的乙酸和降低乙酸乙酯的溶解度。如何检验酯层中没有乙酸____________。
(5)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是_______________。
(6)分离碳酸钠溶液和乙酸乙酯的方法是_________,操作过程为__________。
-
二氧化硫是重要的化工原料,用途非常广泛。
实验一:SO2可以抑制细菌滋生,具有防腐功效。某实验小组欲用下图所示装置测定某品牌葡萄酒中(葡萄酒中含有乙醇、有机酸等)的SO2含量。
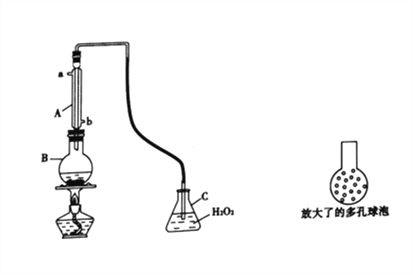
(1)仪器A的名称是________;使用该装置主要目的是____________________。
(2)B中加入 300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,C中化学方程式为_________________________________________。
(3)将输入C装置中的导管顶端改成具有多孔的球泡(如图所示)。可提高实验的准确度,理由是_______________________________________。
(4)除去C中的H2O2 然后用0.09mol·L-1NaOH标准溶液滴定。
①用碱式滴定管量取0.09mol·L-1NaOH标准溶液前的一步操作是___________________________;
②用该方法测定葡萄酒中SO2的含量偏高,主要原因是__________________________________,利用现有的装置,提出改进的措施是_______________________________________________。
(5)利用C中的溶液,有很多实验方案测定葡萄酒中SO2的含量。现有0.1mol·L-1BaCl2溶液,实验器材不限,简述实验步骤:________________________________。
-
硝基苯是重要的化工原料,用途广泛。制备反应如下:

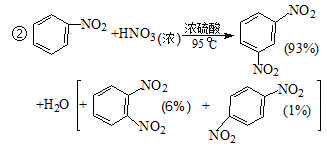
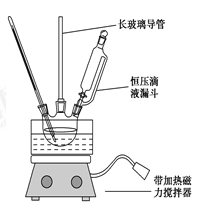
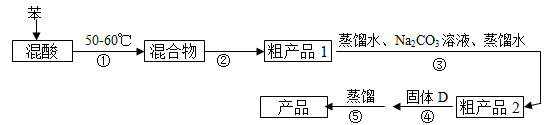
组装如右上图反应装置。 制备、提纯硝基苯流程如下:
可能用到的有关数据列表如下:
| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20 ℃)/g · cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | — | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | — | 338 | 1.84 | 易溶于水 |
请回答下列问题:
(1)配制混酸应在烧杯中先加入 ;实验装置中长玻璃管最好用________代替(填仪器名称);恒压滴液漏斗的优点是 。
(2)反应温度控制在50~60 ℃的原因是 ;反应结束后产物在 层(填“上”或者“下”),步骤②分离混酸和产品的操作名称是 。
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净? 。
(4)固体D的名称为 。
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为 。
-
某课外小组设计的实验室制取乙酸乙酯的装置如下图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。
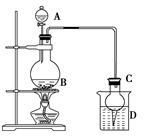
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点如下:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:_____________________________________________________________________。
(2)球形干燥管C的作用是______________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)__________________________________________;
反应结束后D中的现象是_______________________________________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________;再加入________(此空从下列选项中选择),然后进行蒸馏,收集77 ℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰
C.无水硫酸钠 D.生石灰
-
(8分)某研究性小组同学在学习相关有机基础知识后,决定试用类似制乙酸乙酯的装置,以环己醇为主要原料制备环己烯。

已知: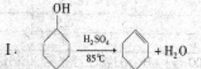
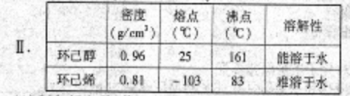
(1)制备粗产品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。请回答有关问题:
①A中碎瓷片的作用是_______________,导管B除了导气外还具有的作用是____________;
②试卷C置于冰水浴中的目的是_______________.
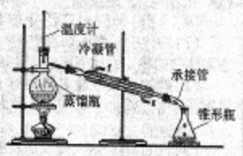
(2)制备精品
①环己烯粗品长含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用_______________(填写编号)洗涤;
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按如图装置蒸馏,冷却水从_________口进入(填“g”或“f”)。收集产品时,温度应控制在______℃左右,实验制得的环己烯制品质量低于理论产量,可能的原因是______________________.




 A.选择合适的试剂,用图1所示装置可分别制取少量
A.选择合适的试剂,用图1所示装置可分别制取少量










