-
现有下列10种物质:
①NaHCO3;②NH4HCO3;③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH; ⑨HCl; ⑩NaOH。
(1)其中属于非电解质的是_____________(填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是_____________。
(2)NaHCO3溶液显________性(填“酸”、“碱”或“中”),原因是(结合离子方程式表示)
________。
(3)常温时有四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液。(已知常温时醋酸的电离常数为1.75×10-5)
下列有关叙述正确的是________。(忽略溶液混合时的体积变化)
A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多
B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的1/2
C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7
D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ
(4)常温时某HCl溶液中由水电离出的C(H+)=1×10-amol/L,而相同pH的AlCl3溶液中由水电离出的C(H+)=1×10-bmol/L (已知a, b均为小于14的正整数),则a和b之间满足的关系为________ ,________(用一个等式和一个不等式表示)。
高三化学填空题中等难度题查看答案及解析
-
Ⅰ:现有下列7种物质:①NaHCO3②CH3COOH③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水.其中属于强电解质的是 (填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是 .
II:现有一瓶浓度为0.2mol/L的某酸溶液,可能为醋酸、盐酸、硫酸中的一种,为了确定该酸溶液的组成进行实验:取20.00mL该酸溶液,逐滴加入0.2mol/L的氢氧化钠溶液,恰好反应完全时所需碱液体积为20.00mL,请用化学用语回答:
(1)该酸不可能是 ;
(2)用pH试纸测得反应后所得溶液呈碱性,根据此现象说明该酸溶液为 ,用离子方程式说明溶液呈碱性的原因 ;
高三化学填空题中等难度题查看答案及解析
-
现有下列10种物质:①Na2CO3 ②AlCl3 ③HCl ④NH4HCO3 ⑤C2H5OH ⑥Al ⑦食盐水 ⑧石墨 ⑨冰醋酸 ⑩二氧化碳
(1)上述物质中属于强电解质的是__;属于非电解质的是__;能导电的是__。(填序号)
(2)既能跟盐酸反应又能跟NaOH溶液反应的是__(填序号)。
高三化学填空题简单题查看答案及解析
-
现有以下物质:①NaCl晶体;②液态SO3;③纯硫酸;④汞;⑤BaSO4固体;⑥葡萄糖(C6H12O6);⑦酒精(C2H5OH);⑧熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是 。
(2)以上物质中属于电解质的是 。
(3)以上物质中属于非电解质的是 。
(4)以上物质中溶于水后形成的水溶液能导电的是 。
高三化学填空题中等难度题查看答案及解析
-
现有下列浓度均为0.1 mol/L的电解质溶液:
①Na2CO3、② NaHCO3、③
、④CH3COONH4、⑤ NH4HCO3
(1)上述5种物质的溶液既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)已知溶液④呈中性,该溶液中离子浓度由大到小的顺序是 。
(3)已知溶液⑤呈碱性,比较④、⑤两溶液的酸碱性,可以得出的结论是 。
高三化学填空题中等难度题查看答案及解析
-
18.(共6分)现有下列浓度均为0.1 mol/L的电解质溶液:
① Na2CO3、② NaHCO3、③
、④ CH3COONH4、⑤ NH4HCO3
(1)上述5种物质的溶液既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)已知溶液④呈中性,该溶液中离子浓度由大到小的顺序是 。
(3)已知溶液⑤呈碱性,比较④、⑤两溶液的酸碱性,可以得出的结论是 。
高三化学填空题中等难度题查看答案及解析
-
现有下列8种物质:①Na2CO3、②NaHCO3、③HCl、④NH4HCO3、⑤C2H5OH、⑥Al、⑦食盐水、⑧CH3COOH。
(1)上述物质中属于强电解质的是_________________(填序号),既能跟盐酸反应又能跟NaOH溶液反应的是______________(填序号)。
(2)上述②的水溶液呈碱性的原因是(用离子方程式表示)__________________________。
(3)④与足量的NaOH浓溶液在加热条件下反应的离子方程式_______________________。
高三化学填空题中等难度题查看答案及解析
-
下列物质中不含离子键的是( )
①NH4HCO3
②NH3
③BaSO4;
④CH3COONa•3H2O
⑤Ba(OH)2
⑥H2SO4.
A.①④⑥ B.②③⑤ C.④⑤ D.②⑥
高三化学选择题简单题查看答案及解析
-
常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体。下列指定溶液中微粒浓度大小比较正确的是( )
A. 原NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+)
B. 原NH4HCO3溶液中:c(OH-)=c(H+)-c(CO32-)-c(NH3·H2O)+c(H2CO3)
C. 析出晶体后的溶液中:c(Cl-)=c(NH4+),c(Na+)=c(HCO3-)
D. 析出晶体后的溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3·H2O)
高三化学选择题困难题查看答案及解析
-
(10分) NaHCO3是重要的化工原料,在实验室里可通过下列两个步骤得到:
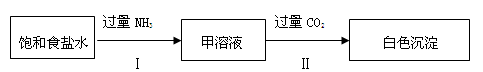
已知一些物质在20℃、30℃时溶解度数据:
溶解度(g)
温度(℃)
NH4Cl
NH4HCO3
NaHCO3
NaCl
Na2CO3
(NH4)2CO3
20
28.7
21.7
9.6
31.5
21.5
100
30
41.1
27.0
11.1
36.3
39.7
>100
请回答:
(1)步骤Ⅰ反应的化学方程式是 。
(2)若将NH3和CO2两种气体通入顺序互换后没有沉淀,原因是 。
(3)步骤Ⅱ所得白色沉淀中一定有NaHCO3,原因是 。
(4)步骤Ⅱ生成NaHCO3的离子方程式是 。
(5)根据气体物质溶解性及上列溶解度数据,简述上述两过程在较低温度下进行时效果更好的原因 。
高三化学实验题中等难度题查看答案及解析