-
I .合成氨工业在现代农业、国防工业中,有着重要的地位
己知:N2 (g) +3H2 (g)  2NH3 (g) △H=-92 kJ·mol-1
2NH3 (g) △H=-92 kJ·mol-1
(1)下列有关该反应速率的叙述,正确的是(选填序号)____________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,但可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量—定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
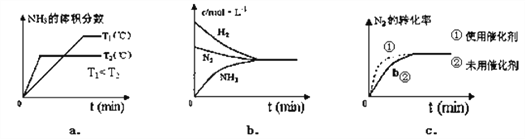
(2)对于合成氨反应而言,如图有关图象一定正确的是(选填序号) ______________。
II.向2L的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:
①2NO(g) + O2(g) =2NO2 (g) ②2NO2 (g) ==N2O4 (g)
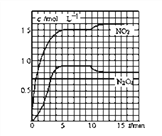
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。
(1)计算前5min N2O4反应的平均速率为________________________。
(2)计算T1℃时反应②的化学平衡常数为_______________________。
(3)若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,判断T1℃时反应②进行的方向_____(正向、逆向、不移动),并计算达到平衡时N2O4的物质的量为_____mol。
-
合成氨工业在现代农业、国防工业中,有着重要的地位。已知:N2(g)+3H2(g) 2NH3(g)ΔH=-92kJ·mol-1。
2NH3(g)ΔH=-92kJ·mol-1。
(1)下列有关该反应速率的叙述,正确的是 。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,但可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)该反应的化学平衡常数表达式为K=_________________。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的K= (用分数表示)。
(4)对于合成氨反应而言,下列有关图像一定正确的是_____________。
a. b.
b. c.
c.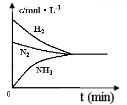
-
I.合成氨工业在现代农业、国防工业中,有着重要的地位。
己知:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ·mol-1
2NH3(g) △H=-92 kJ·mol-1
(1)下列有关该反应速率的叙述,正确的是(选填序号)____________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,但可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量—定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)对于合成氨反应而言,如图有关图象一定正确的是(选填序号)_______。

II.向2L的密闭容器中充入7.6molNO和3.8molO2,发生如下反应:
①2NO(g)+O2(g)=2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。
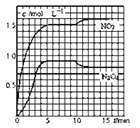
(1)计算前5minN2O4反应的平均速率为____________。
(2)计算T1℃时反应②的化学平衡常数为___________。
(3)若起始时向该容器中充入3.6molNO2和2.0molN2O4,判断T1℃时反应②进行的方向_____(正向、逆向、不移动)。
-
氮及其化合物在工农业生产、生活中有着重要作用。完成下列填空:
合成氨工业中:N2(g)+3H2(g) 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
(1)试比较K1、K2的大小,K1________ K2(填写“>”、“=”或“<”)
(2)400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数的值为_____________。当测得NH3和N2、H2的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应υ(N2)(正)___________υ(N2)(逆)(填写“>”、“=”或“<”)
N2(g)+3H2(g)的化学平衡常数的值为_____________。当测得NH3和N2、H2的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应υ(N2)(正)___________υ(N2)(逆)(填写“>”、“=”或“<”)
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是____________。
a.υ(N2)(正)=3υ(H2)(逆)b.混合气体的密度保持不变
c.容器内压强保持不变d.N2、H2、NH3的浓度之比为1∶3∶2
(4)化工生产为做到又“快”又“多”采用多种方法,试写出两项合成氨工业中为实现“多”所采取的措施:__________________________,__________________________。
(5)0.1mol/L的(NH4)2SO4水溶液中各离子浓度由大到小的顺序是_____________________,在该溶液中加入少量明矾固体,溶液中 的浓度_______(填“增大”、“减小”或“不变”),其原因是___________________。
的浓度_______(填“增大”、“减小”或“不变”),其原因是___________________。
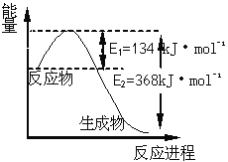
(6)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_____________________________________________。
-
(11分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,氨是最重要的氮肥,是产量最大的化工产品之一.其工业合成原理为:N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.4kJ•mol﹣1.在密闭容器中,使2mol N2和6mol H2混合发生以上反应。
(1)当反应达到平衡时,N2和H2的浓度比是 ,N2和H2的转化率比是
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量 (填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气并保持压强不变,平衡将 (填“正向”“逆向”或“不”)移动
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将 (填“向左移动”“向右移动”或“不移动”).达到新平衡后,容器内温度 (填“大于”“小于”或“等于”)原来的2倍.
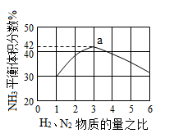
(5)下图表示工业500℃、60.0MPa条件下合成氨,原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数:___ ___。
(6)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH)=c(Cl-);用含a的代数式表示NH3·H2O的电离常数Kb=_________________。
-
氨气是重要化工原料,在国民经济中占重要地位。工业合成氨的反应为:N2(g)+3H2(g) ⇌2NH3(g) △H<0
(1)图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程 曲线图,t1、t3、t4 时刻分别改变某一外界条件,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是___________(填写下列序号)
曲线图,t1、t3、t4 时刻分别改变某一外界条件,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是___________(填写下列序号)
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
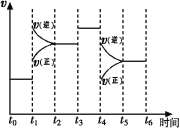
t4时改变的条件是________________。
现进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如表:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
(2)反应在0—10分钟内以氮气浓度变化表示的反应速率为___________,该温度下,此反应的平衡常数K=____________。
(3)该温度下,若向同容积的另一容器中投入的N2、H2、NH3的浓度分别为3mo/L、3mol/L、3mo/L,则此时V正_____V逆 (填“>”“<”或“=”)。
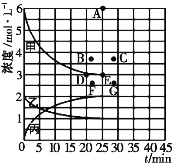
(4)由上表中的实验数据计算得到“浓度一时间”的关系可用右图中的曲线表示,表示c(N2)-t的曲线是______(填“甲”“乙”或“丙”)。在此温度下,若起始充入4molN2和12 molH2,则反应刚达到平衡时,表示c(H2)-t的曲线上相应的点为_________。
-
氨气是重要化工原料,在国民经济中占重要地位。工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g) △H<0进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3) 与反应时间t的关系如下表:
2NH3(g) △H<0进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3) 与反应时间t的关系如下表:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2) /mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3) /mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
(1)反应速率最快的时间段是__________
A.0min-5min B .5min-10min C.10min-15min D. 15min-20min
(2)该温度下,若向同容积的另一容器中投入的N2、H2、NH3的浓度分别为3mol/L、3mol/L、3mol/L,则此时v正 __________v逆 (填 “>”“<”或“=”)。
(3)NH3合成常见的化肥尿素【化学式为CO(NH2)2】分为三步,其中第一步为:2NH3(g)+CO2(g) NH2COONH4(s) △H=-160kJ/mol, 对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出128kJ的热量,NH3 的转化率为__________若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时。c(NH3)为__________。
NH2COONH4(s) △H=-160kJ/mol, 对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出128kJ的热量,NH3 的转化率为__________若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时。c(NH3)为__________。
(4)以氨气代替氢气研发氨燃料电池是当前科研的一个热点。
①氨燃料电池使用的电解质溶液是4mol·L-1的KOH溶液,电池反应为: 4NH3+3O2=2N2+6H2O。该反应每消耗3.4g NH3转移的电子数目为__________;
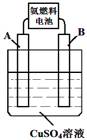
②氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,然后向所得溶液中加入19.6gCu(OH)2固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为__________L。
-
Ⅰ、氨气是重要化工原料,在国民经济中占重要地位。工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g) △H<0。右图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,t1、t3、t4时刻分别改变某一外界条件,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)_______,化学平衡常数最大的一段时间是________。
2NH3(g) △H<0。右图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,t1、t3、t4时刻分别改变某一外界条件,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)_______,化学平衡常数最大的一段时间是________。
a. t0→t1 b.t2→t3 c.t3→t4 d.t5→t6
t4时改变的条件是_______________。

Ⅱ、已知反应:Fe(s)+CO2(g)  FeO(s)+CO(g) H=akJ·mol-1测得在不同温度下,该反应的平衡常数K值随温度的变化如下表所示:
FeO(s)+CO(g) H=akJ·mol-1测得在不同温度下,该反应的平衡常数K值随温度的变化如下表所示:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(1)若在500℃2L密闭容器中进行该反应,CO2起始量为4mol,5min后达到平衡状态,则这段时间内,用CO表达的反应速率为__________.(填写计算所得数值及单位)
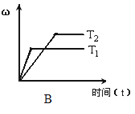
(2)下列图像符合该反应的是_____________(填序号)(图中v代表速率、ω代表混合物中CO的含量,T代表温度)。

(3)下列能说明此反应在500℃达到平衡状态的是___________
①CO的体积分数不变
②固体质量不变
③恒压条件下,气体的体积不变
④恒容条件下,容器内压强不再改变
⑤c(CO)=c(CO2)
-
氨在国民生产中占有重要的地位。工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
(1)反应进行到2小时时放出的热量为____________kJ。
(2)此条件下该反应的化学平衡常数K=____________(保留两位小数)。
(3)有两个密闭容器A和B,A容器保持恒容,B容器保持恒压,起始时向容积相等的A、B中分别通入等量的NH3气体,均发生反应:2NH3(g) 3H2(g)+N2(g)。则:
3H2(g)+N2(g)。则:
①达到平衡所需的时间:t(A)_____t(B),平衡时,NH3的转化率:a(A)______a(B) (填“>”、“=”或“<”)。
②达到平衡后,在两容器中分别通入等量的氦气。A中平衡向_________移动,B中平衡向_________移动。(填“向正反应方向”、“向逆反应方向”、“不”)。
(4)在三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数[φ(NH3)]随时间变化的曲线如图所示.下列说法中正确的是_____(填字母,下同)。
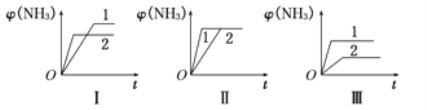
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
-
尿素(H2NCONH2)是有机态氮肥,在农业生产中有着非常重要的作用。
(1)工业上合成尿素的反应分两步进行:
第一步:2NH3(l)+CO2 H2NCOONH4(氨基甲酸铵)(l) △H1
H2NCOONH4(氨基甲酸铵)(l) △H1
第二步:H2NCOONH4 (l)  H2O+ H2NCONH2(l) △H2
H2O+ H2NCONH2(l) △H2
某化学学习小组模拟工业上合成尿素的条件,在体积为1 L的密闭容器中投入4 mol NH3和1 mol CO2,实验测得反应中各组分的物质的量随时间的变化如下图I所示。
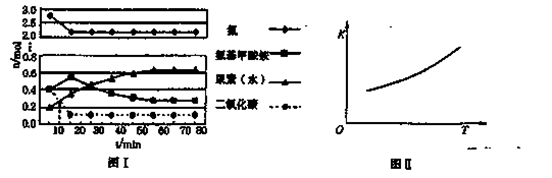
已知总反应的快慢是由较慢的一步反应决定的。则合成尿素总反应的快慢由第______步反应决定, 总反应进行到______min时到达平衡。
②第二步反应的平衡常数K随温度的变化如上右图II所示,则ΔH2______0(填“>”、“<”或“=”。)
(2)该小组将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变, 固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
 。实验测得不同温度下的平衡数据列于下表:
。实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/Kpa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡状态的标志是____________。
A.2V(NH3)=V(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0°C时该分解反应的平衡常数为______(保留小数点后一位)。
(3)已知:
N2(g)+O2(g)=2NO(g) △H1=+180.6KJ/mol
N2(g)+3H2(g)=2NH3(g) △H2=-92.4KJ/mol
2H2(g)+O2(g)=2H2O(g) △H3=-483.6KJ/mol
则4NO(g)+4NH3(g) +O2(g)= 4N2(g)+6 H2O(g)的△H=___kJ • mol-1。
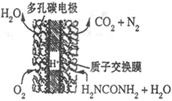
(4)尿素燃料电池的结构如图所示。其工作时 负极电极反应式可表示为______。
2NH3 (g) △H=-92 kJ·mol-1


 b.
b. c.
c.













