-
某同学查阅资料得知,①草酸晶体(H2C2O4·2H2O)在175℃时受热分解,同时熔化且熔融时易挥发。②草酸晶体易溶于水,而草酸钙难溶于水。
为验证草酸分解的产物,该同学选择如下仪器和试剂中的部分完成此实验。
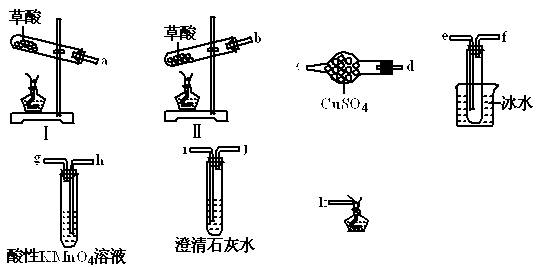
(1)草酸晶体受热分解的方程式为________。
(2)草酸晶体受热分解时,选择的装置为________,理由是________。
(3)若只验证CO2气体一种产物时,除气体发生装置外所选择装置的接口顺序为________。
(4)若验证所有的产物时,除气体发生装置外所选择的必要装置的接口顺序为________。
(5)草酸晶体使酸性高锰酸钾溶液褪色的化学方程式为________。
-
某研究性学习小组的同学通过查阅资料得到如下信息:草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,受热脱水、升华,易溶于水,170℃以上分解可得到CO、CO2、H2O,H2C2O4难溶于水。他们欲利用如下装置验证上述产物(加热仪器、夹持仪器省略)。
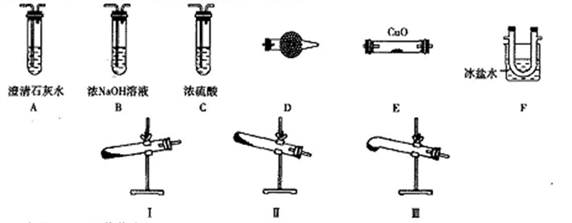
(1)加热草酸晶体使其分解的装置是________(从I、II、III中选取),验证其分解产物的装置依次是______→A→尾气处理装置(用装置字母作答,装置可重复使用)。
(2)D中试剂是_________,证明有CO生成的现象是_______。
(3)实验中有两处需要加热,加热的顺序是_________,写出一种处理尾气的方法:_____________。
(4)若上述实验均产生了预期的现象,写出草酸分解的化学方程式:_________________。
(5)设计一种方案证明草酸是弱酸_________。
-
(14分)某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物(水除外),他们设计的实验装置如下图所示:
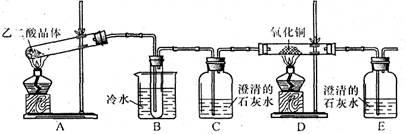
查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:;
(2)装置B的作用是________;指出上述装置中的不足之处:________。
(3)实验结束后向装置B的试管中加入少量酸性高锰酸钾溶液,可以观察到的实验现象是溶液由褪色,反应的离子方程式为________。
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物。实验小组进一步探究:
①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是________。
②取该红色固体与足量的稀硝酸反应,写出反应的化学方程式________。
-
某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物(水除外),他们设计的实验装置如下图所示:
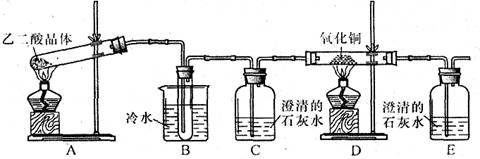
查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:;
(2)装置B的作用是;指出上述装置中的不足之处:。
(3)实验结束后向装置B的试管中加入少量酸性重铬酸钾溶液,可以观察到的实验现象是溶液由橙色变为绿色(Cr3+),反应的离子方程式为________。
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物。实验小组进一步探究:
①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是________。
②取该红色固体与足量的稀硝酸反应,写出反应的化学方程式。
-
草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)查阅资料知:草酸晶体175℃分解成CO2、CO、H2O,请写出草酸晶体分解的化学反应方程式:_____。
(2)请用下列的装置(图中加热装置已略去)分解草酸晶体以制备少量CO气体,最佳的连接顺序为:________。(填字母序号)
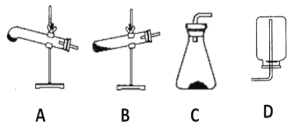
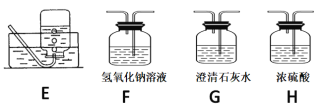
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________(填序号)。
A.室温下,测0.1mol/L的H2C2O4溶液与H2SO4溶液的pH,硫酸溶液的pH比草酸的小;
B.室温下,取pH=3的H2C2O4溶液稀释100倍后,测其pH<5;
C.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL。
(4)现需要配制900mL1mol/L的草酸溶液。
①需要的仪器有托盘天平(带砝码)、钥匙、烧杯、量筒、胶头滴管、_________、__________(填仪器名称)。
②下列操作会使所配溶液浓度偏低的是__________。(填字母)
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.H2C2O4·2H2O晶体失去了部分结晶水
D.定容时,仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(5)用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①滴定过程中反应的离子方程式为_____________________________________________。
②量取KMnO4样品溶液应选用__________(填“酸式”或“碱式”)滴定管;若量取KMnO4样品溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将________(填“偏大”、“偏小”或“不变”)。
③现取KMnO4粗品10g,配成100mL溶液,取25.0 mL用(4)中配制的草酸溶液滴定,并进行3次平行实验,所用的草酸溶液的体积分别为23.00 mL、20.02 mL、19.98 mL,请问KMnO4粗品的质量分数为______________。(已知:KMnO4的摩尔质量为158g/mol)
-
某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如下图所示:
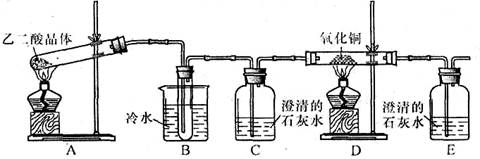
查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:;
(2)装置B的作用是________;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是________;________。
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是________。
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物。实验小组进一步探究:
①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是________。
②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L。则红色固体中含单质铜的质量分数是________。
-
草酸(乙二酸)存在于自然界的植物中,是一种重要的化工原料。草酸晶体(H2C2O4·2H2O)易溶于水,其熔点为101℃,易升华,在175℃时受热分解。草酸钙是难溶于水的白色固体。
I. 用硝酸氧化法制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去)。
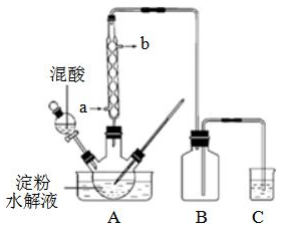
实验具体流程如下:
①糖化:先将淀粉水解为葡萄糖。
②氧化:在淀粉水解液中加入混酸(质量比为3:2的65%HNO3与 98%H2SO4 的混合物),55~60℃水浴加热,发生的主要反应为:C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。
③结晶、蒸发、干燥:反应液经冷却,减压过滤后再重结晶、干燥即得草酸晶体。
(1)装混酸的仪器名称为______,冷凝水的进口为_____(填a或b),装置B的作用为______。
(2)流程①中,检验淀粉是否水解完全的方法是____________。
(3)流程②中,水浴加热的优点为____________。
II. 证明草酸晶体受热分解得到的产物中有 CO2。
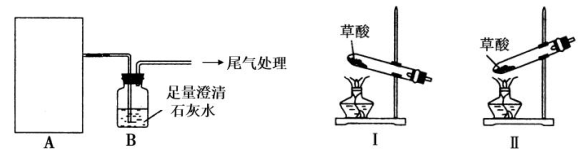
(1)甲同学选择装置A和B组合完成验证实验,装置A应选_______( “I” 或“ II” )。
(2)甲同学依据B中澄清石灰水变浑浊,证明产物中含CO2,乙同学认为此结论不正确,理由是________, 改进方案是__________。
-
某实验研究小组欲检验草酸晶体分解的产物并测定草酸溶液的浓度(杂质不发生反应)。查阅资料:草酸晶体(H2C2O4·2H2O)在100 ℃开始失水,101.5 ℃熔化,150 ℃左右分解产生H2O、CO和CO2。下面是可供选择的实验仪器(图中某些加热、夹持装置已略去),实验所需药品不限。
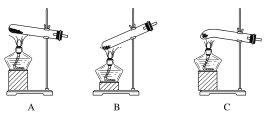
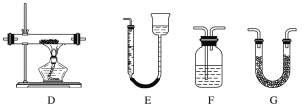
(1)最适宜加热分解草酸晶体的装置是C。若选装置A可能会造成的后果是______________;若选装置B可能会造成的后果是_________________________________。
(2)实验利用装置“G(碱石灰)—F—D(CuO固体)—F”检验CO,则F中盛装的试剂是_______,证明含有CO的现象是_____________________________________________。
(3)可用0.10 mol/L酸性KMnO4标准溶液来滴定未知浓度的草酸溶液。
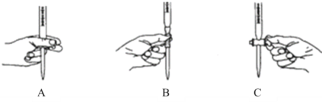
①滴定过程中发生反成的离子方程式为_________________________________________。②滴定过程中操作滴定管的图示正确的是_________。
③判断反应达到滴定终点时的现象为__________________________________________。
-
草酸晶体(H2C2O4·2H2O)无色,熔点为 101℃,易溶于水,受热易脱水、升华,170℃以上分解。 常温下它的电离常数 K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)查阅资料知:草酸晶体 175℃分解成 CO2、CO、H2O,请写出草酸晶体分解的化学反应方程 式:_____。
(2)请用下列的装置(图中加热装置已略去)分解草酸晶体以制备少量 CO 气体,最佳的连接顺序 为:_____。(填字母序号)
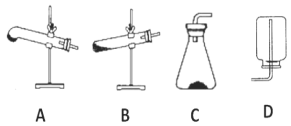
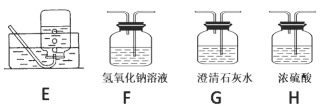
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____(填序号)。
A.室温下,测 0.1mol/L 的 H2C2O4 溶液与 H2SO4 溶液的 pH,硫酸溶液的 pH 比草酸的小;
B.室温下,取 pH=3 的 H2C2O4 溶液稀释 100 倍后,测其 pH<5;
C.标况下,取 0.10mol/L 的 H2C2O4 溶液 100mL 与足量锌粉反应,收集到 H2 体积为 224mL。
(4)现需要配制 900mL1mol/L 的草酸溶液。
①需要的仪器有托盘天平(带砝码)、钥匙、烧杯、量筒、胶头滴管、________ 、_________ (填仪 器名称)。
②下列操作会使所配溶液浓度偏低的是_____。(填字母)
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.H2C2O4·2H2O 晶体失去了部分结晶水
D.定容时,仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(5)用草酸滴定 KMnO4 溶液的方法可测定 KMnO4 粗品的纯度(质量分数)。
①滴定过程中反应的离子方程式为_____。
②量取 KMnO4 样品溶液应选用_________ (填“酸式”或“碱式”)滴定管;若量取 KMnO4 样品溶液的 滴定管用蒸馏水洗净后未润洗,则最终的测定结果将_______(填“偏大”、“偏小”或“不变”)。
③现取 KMnO4 粗品 10g,配成 100mL 溶液,取 25.0 mL 用(4)中配制的草酸溶液滴定,并进行 3 次 平行实验,所用的草酸溶液的体积分别为 23.00 mL、20.02 mL、19.98 mL,请问 KMnO4 粗品的质量分数 为_____________。(已知:KMnO4 的摩尔质量为 158g/mol)
-
草酸晶体的组成可表示为H2C2O4·xH2O,某研究性学习小组用下图装置进行“草酸晶体受热分解的部分产物的验证”的实验。请回答下列问题。
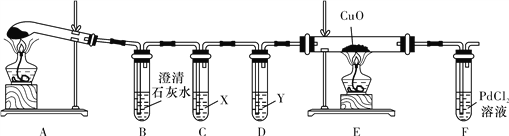
【资料查阅】
①草酸晶体在101 ℃时开始熔化,150 ℃时开始升华,175 ℃时开始分解;
②草酸钙和草酸氢钙均为白色不溶物。
(1)按照如图所示的装置,通过实验检验草酸晶体的部分分解产物,装置B中可观察到有气泡冒出且澄清石灰水变浑浊,由此甲同学判断草酸晶体分解的产物中有CO2。但立即遭到乙同学反对,其反对的理由可能是______________________________________。
(2)丙同学认为草酸晶体分解的产物中含有CO,为进行验证,X应选用________(填化学式)浓溶液,装置D的作用是____________________。
(3)实验过程中涉及如下操作:①点燃装置A处的酒精灯;②熄灭装置A处的酒精灯;③点燃装置E处的酒精灯;④熄灭装置E处的酒精灯。这4步操作由先到后的顺序为____________(填序号)。点燃E处酒精灯前必须要进行的操作是______________。
(4)实验过程中发现装置E中黑色粉末变红色,装置F中有黑色固体生成,经检测装置F中的固体为金属单质,则装置F中发生反应的化学方程式为________________________________________________________________________。
(5)丁同学用滴定法测定草酸晶体中结晶水的含量,进行了下列操作:
步骤一:用分析天平称取3.15 g纯净的该草酸晶体,配制成250 mL溶液。
步骤二:用移液管移取25.00 mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化。
步骤三:取0.100 mol·L-1标准酸性KMnO4溶液,进行滴定,三次结果如下表所示:
| 第一次 | 第二次 | 第三次 |
| 待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
| 标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知滴定反应的离子方程式为:MnO +H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
+H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
①配制草酸溶液的操作步骤依次是:将晶体置于烧杯中,加水溶解,将溶液转移入________,洗涤,定容,摇匀。
②通过计算确定x=________。














