-
卤族元素是非常重要的非金属元素,其单质和化合物有广泛用途,化学性质也非常丰富。
(1)基态氯原子的价电子排布式为__________________,其核外电子占据的最高能层的符号是_________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是___________。
(3)ClO2—的立体结构为_______形,中心氯原子的杂化轨道类型为_________,写出ClO2—一个等电子体的化学式 ______。
(4)下列分子中只存在s-p 键的是_____________。
键的是_____________。
A. H2 B.F2 C.HCl D.HClO
(5)CsICl2不稳定,受热时可能按下列两种方式分解,已知生成物晶格能越大反应越易发生,则CsICl2按下列______方式分解更合理。
A.CsICl2=CsI+Cl2 B. CsICl2=CsCl+ICl
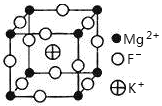
(6)由F、K、Mg三种元素形成的某离子晶体的晶胞结构如下图所示,晶胞边长为a nm(1nm=10—9m)。
①该晶体的化学式为___________________。
②该晶体的密度为____________g•cm—3。(结果保留1位小数)
-
卤族元素是非常重要的非金属元素,其单质和化合物有广泛用途,化学性质也非常丰富。
(1)基态氯原子的价电子排布式为__________________,其核外电子占据的最高能层的符号是_________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是___________。
(3)ClO2—的立体结构为_______形,中心氯原子的杂化轨道类型为_________,写出ClO2—一个等电子体的化学式 ______。
(4)下列分子中只存在s-p 键的是_____________。
键的是_____________。
A. H2 B.F2 C.HCl D.HClO
(5)CsICl2不稳定,受热时可能按下列两种方式分解,已知生成物晶格能越大反应越易发生,则CsICl2按下列______方式分解更合理。
A.CsICl2=CsI+Cl2 B. CsICl2=CsCl+ICl
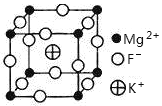
(6)由F、K、Mg三种元素形成的某离子晶体的晶胞结构如下图所示,晶胞边长为a nm(1nm=10—9m)。
①该晶体的化学式为___________________。
②该晶体的密度为____________g•cm—3。(结果保留1位小数)
-
卤族元素及其化合物的用途非常广泛。回答下列问题:
(1)基态氯原子价电子轨道表示式(电子排布图)为___;处于最高能级电子云轮廓图形状为____。
(2) 和
和 的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
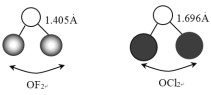
①O-F键的键长比O-Cl键的小,其原因是______。
②键角:∠FOF_____(填“>”、“<”或“=”)∠ClOCl。
(3)①试解释酸性HBrO4>HBrO3的原因_________ 。
②试解释酸性HClO3>HBrO3>HIO3的原因_________ 。
(4) 的熔点为1040℃;
的熔点为1040℃; 的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
(5)氯化亚铜晶胞结构如图所示,晶胞参数a=0.542nm。
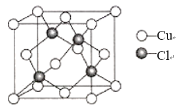
①Cu+的配位数为_____。
②氯化亚铜的密度为____ (用含NA的计算式表示)。
(用含NA的计算式表示)。
-
卤族元素的单质和化合物在生产生活中有重要的用途。
(1)溴原子的价电子排布图为__________。
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是____________。
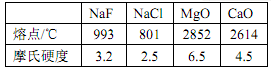
(3)根据下表数据,分析熔点和硬度变化的原因:________________。
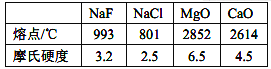
(4)HIO3 的酸性_____(填“>”或“<”)HIO4,原因是_________________。
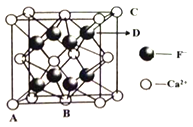
(5)晶胞有两个基本要素:①坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 为(0,0,0);B 为(1/2, 1/2,0);C 为(1,1,1)。则 D 微粒的坐标参数为____。
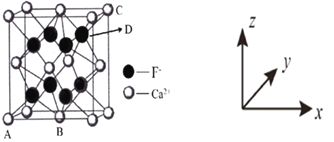
②晶胞参数(即晶胞边长):描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c g•cm3,则晶胞中 Ca2+与离它最近的 F之间的距离为______nm(设 NA 为阿伏加德罗常数的值,用含 c、NA 的式子表示)。
-
卤族元素的单质和化合物在生产生活中有重要的用途。
(1)溴原子的核外电子排布式为[Ar]__________,有_____个未成对电子。
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是____________。
(3)根据下表数据,分析熔点和硬度变化的原因:________________。
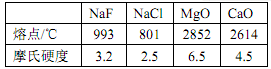
(4)HIO3 的酸性_____(填“强于”或“弱于”)HIO4,原因是_________________。
(5)ClO2中心氯原子的杂化类型为________,ClO3的空间构型为__________。
(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 处为(0,0,0);B 处为( ,
,  ,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。
,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。
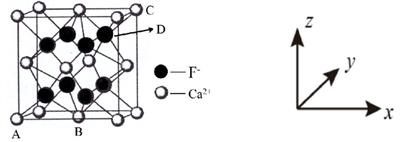
②晶胞参数:描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c g•cm3,则晶胞中 Ca2+与离它最近的 F之间的距离为_________ nm(设 NA 为阿伏加德罗常数的值,用含 c、NA 的式子表示)。
-
卤族元素的单质和化合物在生产生活中有重要的用途。
(1)溴原子的核外电子排布式为[Ar]__________,有_____个未成对电子。
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是____________。
(3)根据下表数据,分析熔点和硬度变化的原因:________________。
(4)HIO3 的酸性_____(填“强于”或“弱于”)HIO4,原因是_________________。
(5)ClO2中心氯原子的杂化类型为________,ClO3的空间构型为__________。
(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 处为(0,0,0);B 处为( ,
,  ,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。
,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。
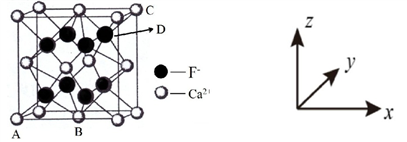
②晶胞参数:描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c g•cm3,则晶胞中 Ca2+与离它最近的 F之间的距离为_________ nm(设 NA 为阿伏加德罗常数的值,用含 c、NA 的式子表示)。
-
【化学—选修3:物质结构与性质】铜是重要的过渡元素,其单质及化合物具有广泛用途。回答下列问题:
(1)铜元素基态原子的价电子排布式________。
(2)铜能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。
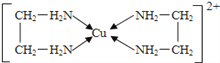
①Cu2+与乙二胺所形成的配离子中含有的化学键是________。
a.配位键 b.离子键 c.  键 d.
键 d.  键
键
②乙二胺分子中氮原子的杂化轨道类型为________,C、N、H三种元素的电负性由大到小顺序是________。
③乙二胺和三甲胺[N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是________。
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是________。
(4)Cu和S形成某种晶体的晶胞如图所示。
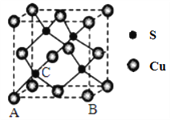
①该晶体的化学式为________。
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为________。
③已知该晶体的密度为d g·cm-3,Cu2+和S2-的半径分别为a pm和b pm,阿伏加德罗常数值为NA。列式表示该晶体中原子的空间利用率________。
-
卤族元素的单质和化合物在生产生活中有重要的用途。
(1)基态溴原子的核外电子排布式为[Ar]_________。
(2)在一定浓度的HF溶液中,氟化氢是以缔合形式(HF)2存在的。使氟化氢分子缔合的作用力是_________。
(3)HIO3的酸性_________(填“强于”或“弱于”) HIO4,原因是_________。
(4)ClO2-中心氯原子的杂化类型为_________,ClO3-的空间构型为_________。
(5)晶胞有两个基本要素:①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为( ,
, ,0);C处为(1,1,1)。则D处微粒的坐标参数为_________。
,0);C处为(1,1,1)。则D处微粒的坐标参数为_________。
②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为cg·cm-3,则晶胞中Ca2+与离它最近的F-之间的距离为_________nm (设NA为阿伏加德罗常数的值,用含C、NA的式子表示;相对原子质量:Ca 40 F 19)。
-
氮是生命物质的重要组成元素之一,氮的单质及其化合物性质多样,用途广泛。
(1)氮原子核外电子排布式为_________,其最外层电子共有_____种不同的伸展方向。
(2)N2分子是一种极具理论研究价值的分子,它的空间结构如图,是一种正四面体结构( ),则N4是一种_____________分子。(填“极性”或“非极性”)
),则N4是一种_____________分子。(填“极性”或“非极性”)
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变为CO2和N2:2NO+2CO  2CO2 + N2+Q ( Q>0),该反应平衡常数K的表达式为___________;温度升高,K值________(选填“增 大”、“减小”、“不变”);若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是_____________________。
2CO2 + N2+Q ( Q>0),该反应平衡常数K的表达式为___________;温度升高,K值________(选填“增 大”、“减小”、“不变”);若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是_____________________。
(4)铁盐可用作氮肥,实验室检验铵盐中的 NH4+时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使___________________,说明有NH4+。
-
铁被称为“第一金属”,硫被称为“生命元素”,它们形成的物质种类非常丰富,在生产、生活中用途广泛。
(1)基态S原子有___种能量不同的电子,其价电子排布图为___。
(2)硫能形成S2O 、SO
、SO 等多种含氧酸根,试推测S2O
等多种含氧酸根,试推测S2O 的空间构型为___,SO
的空间构型为___,SO 的中心原子杂化方式为___。
的中心原子杂化方式为___。
(3)SCN-与Fe3+能发生显色反应,该反应常用作检验Fe3+的存在。
①铁元素位于元素周期表的___区。
②SCN-的三种元素的电负性由大到小的顺序为___(用元素符号表示)。写出与SCN-互为等电子体的分子的分子式___(任写一种)。
③Fe(SCN)3中不存在的化学键有___(填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键 E.σ键 F.π键
(4)部分卤化铁的熔点如下表所示:
| 卤化铁 | FeF3 | FeCl3 |
| 熔点/℃ | 1100 | 306 |
解释表中物质之间熔点差异的原因___。
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B两种方块组成。
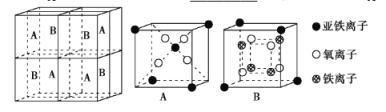
①该氧化物中Fe2+、Fe3+、O2-个数的最简整数比为___。
②己知该晶体的密度为dg·cm-3,阿伏加德罗常数的值为NA,则晶胞参数a为___ nm(用含d和NA的代数式表示)。
键的是_____________。














