-
氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/°C | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是________。
(2)根据-4,合成氨的热化学方程式是________。

(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2  2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=________;该温度下的平衡常数K=________(用分数表示);俗使K增大,可以采取的措施是________。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=________;该温度下的平衡常数K=________(用分数表示);俗使K增大,可以采取的措施是________。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是________(选填序号字母)
a.及时分离出NH3 b.升高温度
c.增大压强 d.使用催化剂
-
氨是一种重要的化工原料,氨的合成与应用是当今重要研究内容之一。不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2起始物质的量之比为1∶3)。
|  压强(Mpa) 压强(Mpa)
 氨的平 氨的平
衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
回答下列有关问题:
(1)利用表中数据推断得出合成氨的反应是__________反应(填“放热”、“吸热”或“无热量变化”)。
(2)根据表中数据,在200℃和100MPa时,平衡体系中NH3的物质的量分数最高,而实际工业生产不选用该条件的主要原因是___________________________________。
(3)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“可能增大也可能减小”):
(4)将1molH2和1molN2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,测得NH3的物质的量为0.3mol,此时若移走0.5molH2和0.5molN2,则反应达到新的平衡时,NH3的物质的量为_____________(选填答案编号)。
A.0.3mol B.0.15mol C.小于0.15mol D.大于0.15mol,小于0.3mol
-
氨在工农业生产中应用广泛。德国人哈伯发明了合成氨反应,其原理为:N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
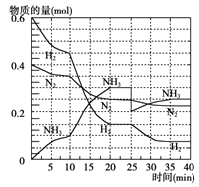
(1)10 min内用NH3表示该反应的平均速率,v(NH3)= 。
(2)在10~20min内NH3浓度变化的原因可能是 (填字母)。
A.加了催化剂 b.降低温度 C.增加NH3的物质的量
(3)该可逆反应达到平衡的标志是__________ (填字母)。
a.3v(H2)正 = 2v(NH3)逆 b.混合气体的密度不再随时间变化
c.容器内的总压强不再随时间而变化 d. N2、H2、NH3的分子数之比为1∶3∶2
e.单位时间生成m mol N2的同时消耗3 m mol H2 f.a mol N≡N键断裂的同时,有6 a mol N—H键合成
(4)第一次平衡时,平衡常数K1= (用数学表达式表示)。NH3的体积分数是 (保留2位小数)。
(5)在反应进行到25min时,曲线发生变化的原因是________________。
(6)已知:N2(g)+3H2(g)  2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。
2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。
(7)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如右图所示:
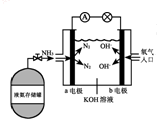
① a电极的电极反应式是______________;
② 一段时间后,需向装置中补充KOH,请依据反应原理解释原因是_______________。
-
总压强为 3.0×107 Pa 时,N2、H2 混合气体(体积之比为 1∶3)通入合成塔中,反应达平衡时,压强降为 2.5×107 Pa,则平衡时混合气体中 NH3 的体积分数为
A.35% B.30% C.25% D.20%
-
总压强为3.0×107 Pa时,N2、H2混合气体 (体积之比为1:3) 通入合成塔中,反应达平衡时,压强降为2.5×107Pa,则平衡时混合气体中NH3的体积分数为 ( )
A. 35% B. 30% C. 1/4 D. 1/5
-
总压强为3.0×107 Pa时,N2、H2混合气体 (体积之比为1:3) 通入合成塔中,反应达平衡时,压强降为2.5×107Pa,则平衡时混合气体中NH3的体积分数为 ( )
A.35% B.30% C .25% D.20%
-
总压强为3.0×107 Pa时,N2、H2混合气体(体积之比为1:3)通入合成塔中,反应达平衡时,压强降为2.5×107Pa,则平衡时混合气体中NH3的体积分数为( )
A.35%
B.30%
C.25%
D.20%
-
总压强为3.0×107 Pa时,N2、H2混合气体(体积之比为1:3)通入合成塔中,反应达平衡时,压强降为2.5×107Pa,则平衡时混合气体中NH3的体积分数为( )
A.35%
B.30%
C.25%
D.20%
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且使平衡混合物中NH3的体积分数一定增大的是________。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
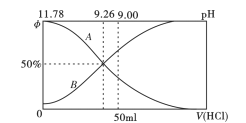
①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
②NH3·H2O的电离常数为_______(已知lg1.8 = 0.26)。
③当加入盐酸体积为50ml时,溶被中c(NH4+)- c(NH3·H2O) =_____mol/L (用数字表示)。
Ⅱ.若液氨中也存在类似水的电离( H2O+H2O H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式_________.
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式__________
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且一定使平衡混合物中NH3的体积分数增大的是________。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3∙H2O的物质的量分数与加入盐酸的体积的关系如图所示,根据图像回答下列问题。
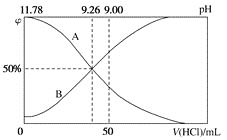
①表示NH3∙H2O浓度变化的曲线是________(填“A”或“B”)。
②NH3∙H2O的电离常数为________(已知lg1.8=0.26)。
③当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3∙H2O)=________mol/L(用数字表示)。
II若液氨中也存在类似水的电离(H2O+H2O⇌H2O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(3)写出液氨的电离方程式:____________________________。
(4)写出碳酸钠溶于液氨后第一级氨解的离子方程式:___________________。
(5)写出碳酸钠的液氨溶液中各离子浓度的大小关系:________________。

2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=________;该温度下的平衡常数K=________(用分数表示);俗使K增大,可以采取的措施是________。



