-
某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液.
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
滴定次数
盐酸体积
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
回答下列问题:
(1)步骤①中,量取20.00mL待测液应使用________(填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果 ______(填“偏大”、“偏小”或“无影响”).
(2)步骤②中,滴定时眼睛应注视_______(填仪器名称),判断到达滴定终点的依据是_____________________________________________________________
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次,其可能的原因是(填字母)___
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡 B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成 D.滴定终点时,俯视读数
(4)根据上表记录数据,通过计算可得该盐酸的浓度为________ mol/L
高二化学实验题中等难度题查看答案及解析
-
(16分)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液。
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
滴定次数
盐酸体积
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
请回答下列问题:
(1)步骤①中,量取20.00mL待测液应使用________ (填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果__________(填“偏大”、“偏小”或“无影响”)。
(2)判断到达滴定终点的现象是___________________________________________。
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次的体积,其可能的原因是___________________(填字母)
A.滴定前滴定管尖嘴有气泡,滴定结束时无气泡
B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成
D.滴定终点时,俯视读数
(4)由以上数据,该盐酸的物质的量浓度为________,若要计算盐酸溶液中盐酸的质量分数还缺少的物理量是:;(请注明单位)。如缺少的数据用字母a表示,则盐酸溶液中盐酸的质量分数为;
(5)下列操作会使结果偏高的是________(多选倒扣分)
A.碱式滴定管用蒸馏水洗净后,即注入标准NaOH溶液
B.用酸式滴定管取用待测酸液前,尖嘴部分有气泡,取用过程中气泡消失
C.滴定前,读碱液体积时仰视;滴定后,读碱液体积时俯视
D.滴定前,盛放盐酸的锥形瓶不干燥
高二化学实验题简单题查看答案及解析
-
(12分)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度以上
② 固定好滴定管并使滴定管尖嘴充满液体
④ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
填空:(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果__________。(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记录滴定管液面读数时,滴定管尖嘴有气泡,导致测定结果____________。(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:________ ;
(4)如下图是某次滴定时的滴定管中的液面,其读数为 ________mL
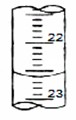
(5)根据下列数据:请计算待测盐酸溶液的浓度:mol·L-1
滴定次数
待测液体积(mL)
标准烧碱体积(mL)
滴定前读数
滴定后读数
第一次
20.00
0.40
20.40
第二次
20.00
4.00
24.00
第三次
20.00
2.00
24.10
高二化学实验题简单题查看答案及解析
-
某学生用0.2000mol/L NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(A)移取15.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗碱式滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准NaOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)(B)-(___)-(___)-(___)-(A)-(___);
(2)三次滴定消耗NaOH溶液的体积如下:
实验序号
1
2
3
消耗NaOH溶液的体积(mL)
20.05
20.00
19.95
则该盐酸溶液的准确浓度为_____________。(保留小数点后4位)
(3)用标准的NaOH溶液滴定未知浓度的盐酸,下列情况可能造成测定结果偏高的是:____________。
A. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确。
B. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗。
C. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液。
D. 碱式滴定管用蒸馏水洗净后,未用标准液润洗。
高二化学实验题中等难度题查看答案及解析
-
某学生用0.1000 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3 cm;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)______________________________。
(2)上述B步骤操作的目的是_______________________________________。
(3)实验中用左手控制活塞,眼睛注视___________________,直至滴定终点。判断到达终点的现象是________________________________。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定次数
待测溶液的体积(mL)
0.100 0 mol·L-1NaOH的体积(mL)
滴定前刻度
滴定后刻度
溶液体积(mL)
第一次
20.00
0.00
26.11
26.11
第二次
20.00
1.56
30.30
28.74
第三次
20.00
0.22
26.31
26.09
依据上表数据列式计算该盐酸溶液的物质的量浓度为__________
(5)用0.1000 mol·L-1 NaOH溶液滴定0.1000 mol·L-1盐酸,如达到滴定的终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH等于____________
(6)下列哪些操作会使测定结果偏高(填序号)(_____)
A.锥形瓶中溶液的颜色刚刚由无色变为浅红色即停止滴定 B.碱式滴定管用蒸馏水洗净后立即注入标准液
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失 D.滴定前读数正确,滴定后俯视滴定管读数
E.实验中,用待盛装的溶液润洗锥形瓶
高二化学实验题中等难度题查看答案及解析
-
某学生用0.10mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂。重复上述滴定操作2~3 次,记录数据如下。
(1)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A.滴定前平视读数,终点读数时仰视读数
B.锥形瓶水洗后未用待测盐酸润洗
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.标准液漏滴在锥形瓶外一滴
E.滴定前仰视读数 ,终点滴定后俯视读数
F.碱式滴定管尖嘴部分有气泡,滴定后消失
(2)若在达到滴定终点时,不慎多加了一滴NaOH溶液(一滴溶液体积约为0.05mL)继续加水到50 mL,所得溶液的pH为 。
(3)如图是向20mL的盐酸中逐渐加入0.1mol/L NaOH溶液时,溶液的pH变化图像,当滴加NaOH溶液为10mL时,该混合液的pH= ,(含lg表达式),若用该NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是 。
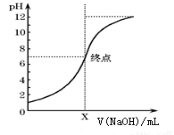
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(4)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
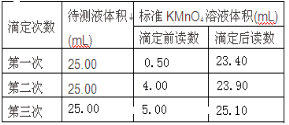
①滴定时,滴定终点时滴定现象是_____________。
②该草酸溶液的物质的量浓度为_____________。
高二化学实验题困难题查看答案及解析
-
某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“ 0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2-3次;
请回答下列问题:
(1)以上步骤有错误的是(填编号)_____________,该错误操作会导致测定结果_________ (填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用________________ (填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视_______________________;判断到达滴定终点的依据是_______。
(4)以下是实验数据记录表
滴定次数
盐酸体积(mL)
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是(______)
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视读数
(5)根据上表记录数据,通过计算可得,该盐酸浓度为____________mol·L-1
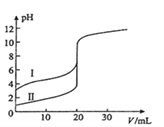
(6)室温下,用0.100mol/L NaOH溶液分别滴定20.00mL0.100mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是(______)
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗V(NaOH)小于20mL
C.V(NaOH) =20mL时,c( Cl- )=c(CH3COO- )
D.V(NaOH) =10mL时,醋酸溶液中:c( Na+ )> c(CH3COO-)> c( H+ )> c(OH-)
高二化学实验题中等难度题查看答案及解析
-
某学生用0.2000mol-L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol-L-1标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
⑥重复以上滴定操作2-3次.
请回答:
(1)以上步骤有错误的是(填编号)_____________,该错误操作会导致测定结果______ (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用_____________(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果___________(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视_______________;判断到达滴定终点的依据是:______________.
(4)以下是实验数据记录表
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是___________
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据上表记录数据,通过计算可得,该盐酸浓度为:___________mol-L-1.
高二化学实验题困难题查看答案及解析
-
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol•L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
⑥重复以上滴定操作2-3次.
请回答:
(1)以上步骤有错误的是(填编号)______,该错误操作会导致测定结果______ (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用______(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果______(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视______;判断到达滴定终点的依据是:______.
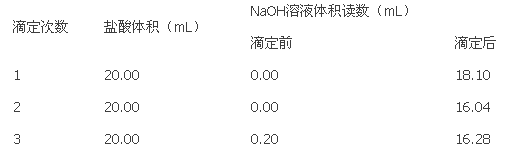
(4)以下是实验数据记录表
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是______滴定次数 盐酸体积(mL) NaOH溶液体积读数(mL) 滴定前 滴定后 1 20.00 0.00 18.10 2 20.00 0.00 16.04 3 20.00 0.20 16.28
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据上表记录数据,通过计算可得,该盐酸浓度为:______mol•L-1.高二化学解答题中等难度题查看答案及解析
-
(11分)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步: ①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答:
(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果_________
(填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用__________________(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视 _______________________________判断到达滴定终点的依据是:__________________________________________________。
(4)以下是实验数据记录表
滴定次数
盐酸体积(mL)
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是( )
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5) 根据上表记录数据,通过计算可得,该盐酸浓度为:____________mol·L-1
高二化学实验题简单题查看答案及解析